-
1、在下图中选择适合的仪器,回答问题。
 (1)、写出下列仪器的名称:b.;h.;e.;g.。(2)、取用粉末试剂时用;量取28mL的液体用;吸取和滴加少量液体时,所用的仪器是;加热试管里的试剂应使用。(填字母序号)
(1)、写出下列仪器的名称:b.;h.;e.;g.。(2)、取用粉末试剂时用;量取28mL的液体用;吸取和滴加少量液体时,所用的仪器是;加热试管里的试剂应使用。(填字母序号) -
2、对比实验是实验探究的重要方法,下列对比实验设计不能达到相应实验目的的是
A
B
C
D

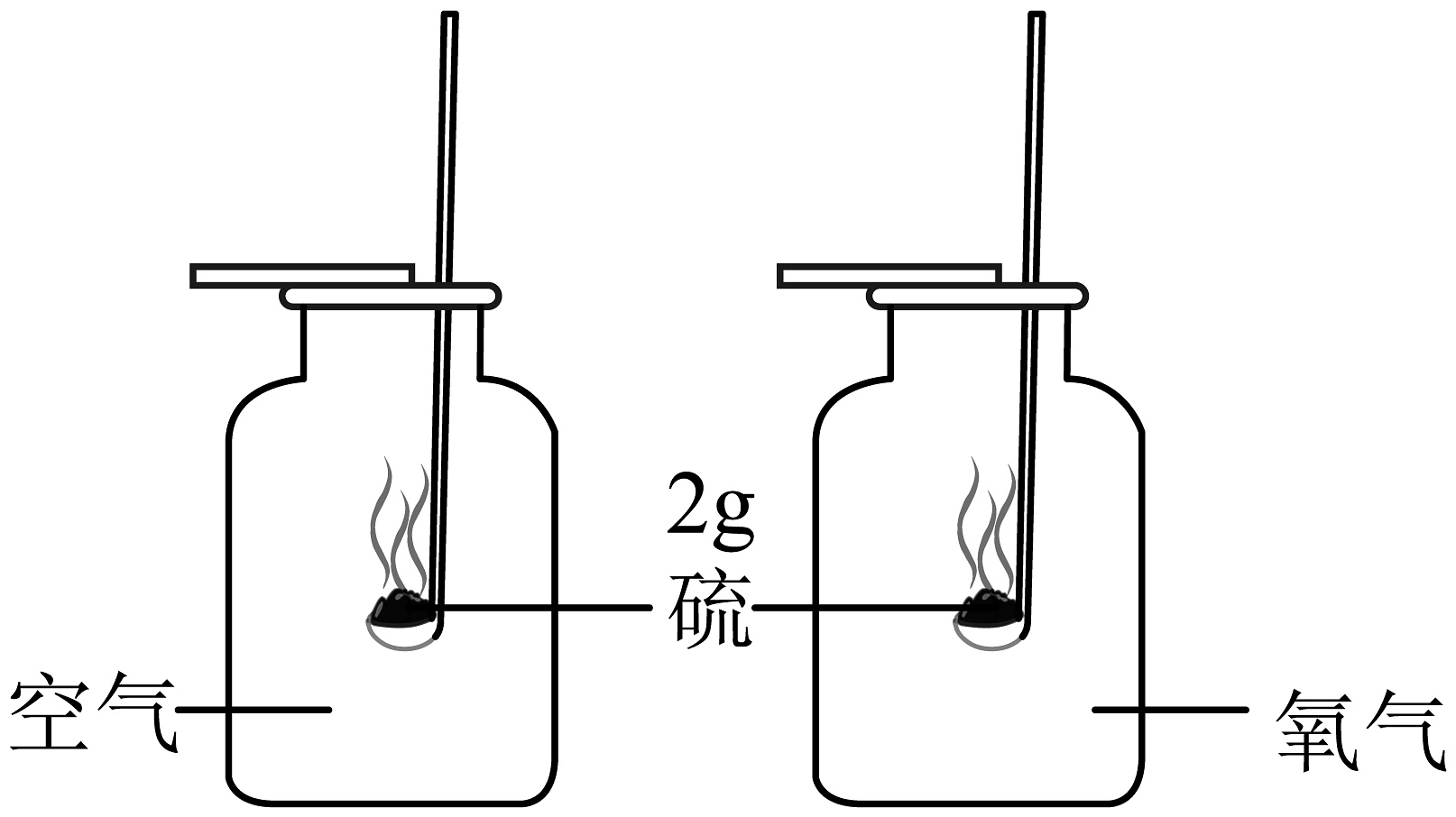


探究温度对分子运动快慢的影响
探究氧气含量对反应剧烈程度的影响
探究空气与呼出气体中二氧化碳的含量
探究反应物浓度对反应速率的影响
A、A B、B C、C D、D -
3、在由SO2和O2组成的混合气体中,测知硫元素的质量分数为20%,则混合气体中SO2和O2的质量比为A、2∶1 B、1∶2 C、2∶3 D、1∶4
-
4、分析推理是化学学习中最常用的思维方法,下列说法正确的是A、元素是指具有相同质子数的一类原子的总称,具有相同质子数的粒子一定是同种元素 B、单质是由同种元素组成的纯净物,由同种元素组成的物质一定是单质 C、分子、原子都是不带电的粒子,所以不带电的粒子一定是分子或原子 D、化学变化中分子可分,故分子发生改变的变化一定是化学变化
-
5、如图所示为制备甲醇(CH3OH)的微观过程,下列说法正确的是
 A、该化学反应生成了三种新物质 B、甲醇分子由3种原子构成 C、参加反应的氢分子和二氧化碳分子数之比为4:1 D、反应中若不使用纳米纤维催化剂,甲醇的总产量会降低
A、该化学反应生成了三种新物质 B、甲醇分子由3种原子构成 C、参加反应的氢分子和二氧化碳分子数之比为4:1 D、反应中若不使用纳米纤维催化剂,甲醇的总产量会降低 -
6、20世纪20年代,就有人预言可能存在由4个氧原子构成的分子,但一直没有得到证实。最近,意大利的科学家首先制造出了这种新型分子,并用质谱仪探测到了它的存在。下列有关它的叙述中正确的是A、是一种新型的化合物 B、一个分子中含有2个氧分子 C、和氧气的性质完全相同 D、和氧气混合后形成的是混合物
-
7、物质的性质决定物质的用途,下列物质的用途主要与其物理性质相关的是A、氦气可用做氦气球 B、氮气用作保护气 C、氧气可供给呼吸 D、天然气用来煮饭
-
8、小李学习了水的有关知识后,自制了如图所示的简易净水器,下列说法正确的是
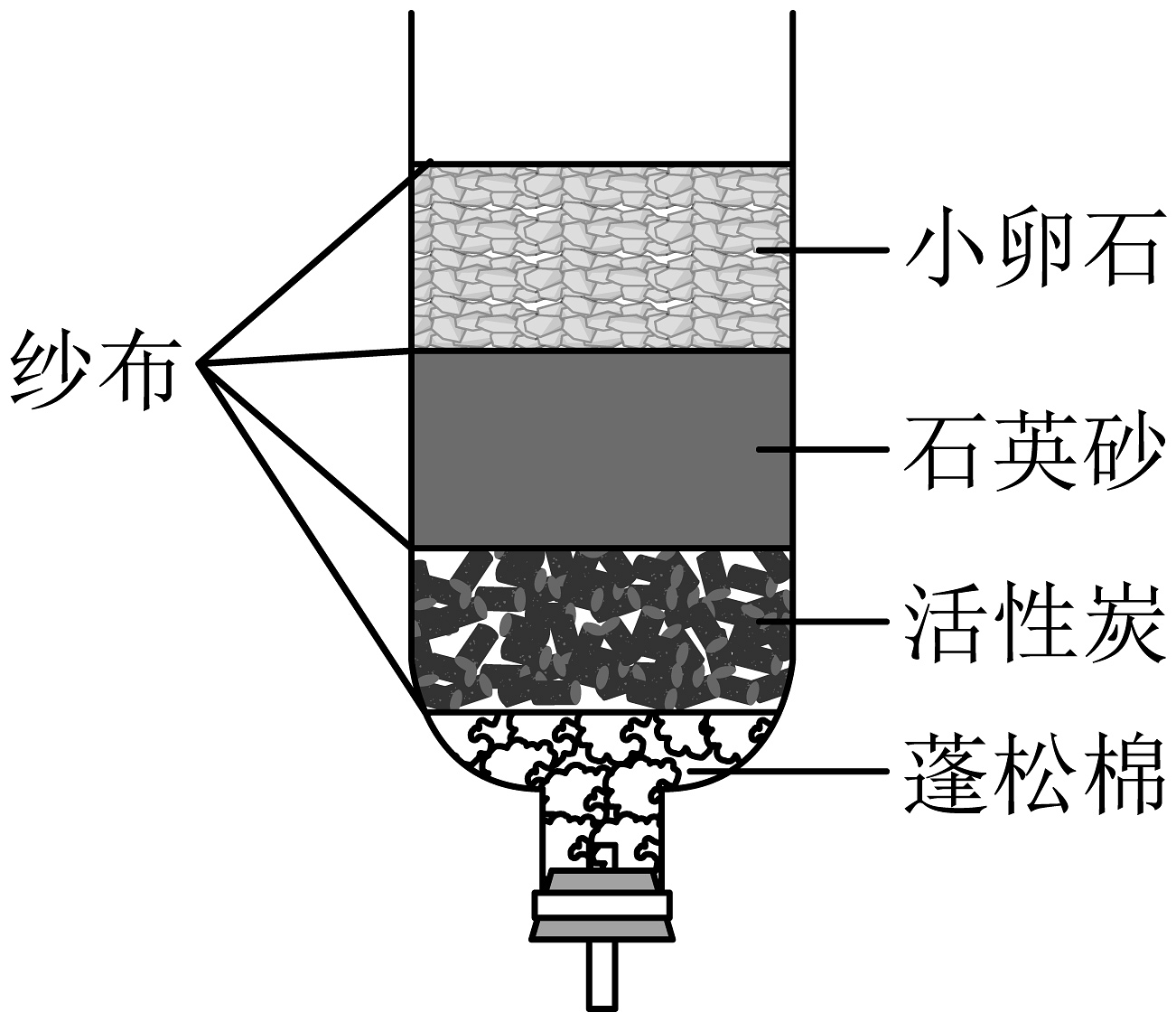 A、该净水器中的活性炭可除异味 B、该净水器可以降低自来水的硬度 C、该净水器能起到杀菌消毒的作用 D、该净水器可将自来水变为蒸馏水
A、该净水器中的活性炭可除异味 B、该净水器可以降低自来水的硬度 C、该净水器能起到杀菌消毒的作用 D、该净水器可将自来水变为蒸馏水 -
9、下列叙述正确的是A、分离液态空气制氧气属于分解反应 B、为了便于储存、运输和使用把氧气加压贮存在蓝色钢瓶中 C、对过氧化氢的分解具有催化作用的物质只有二氧化锰一种 D、要使过氧化氢分解放出氧气必须要加入二氧化锰,否则就不能反应
-
10、下列符号中,只有微观意义的是A、Cl- B、CO2 C、H2 D、Fe
-
11、规范的实验操作是实验安全与成功的关键。下列有关实验室化学试剂取用等规则说法中正确的是A、无毒、无害的块状试剂可以用手直接接触 B、在实验室中用尝味道的方法鉴别食盐和白糖 C、实验后剩余的试剂应放回原试剂瓶,避免浪费 D、块状试剂用镊子取用
-
12、我国的科学家为世界化学的发展作出了卓越贡献。下列科学成果中与中国科学院院士张青莲教授有关的是
 A、提出分子学说 B、测定相对原子质量 C、编制元素周期表 D、测定空气中氧气含量
A、提出分子学说 B、测定相对原子质量 C、编制元素周期表 D、测定空气中氧气含量 -
13、在室温条件下,向4个相同的盛有100g水的大烧杯中分别加入一定量的硝酸钾,充分溶解后,记录数据如下:
实验组别
1
2
3
4
加入硝酸钾质量/g
25
30
35
40
溶液质量/g
125
130
132
a
(1)、若已知第3组实验所得溶液为饱和溶液,则第4组实验中a的值是。(2)、室温下,硝酸钾饱和溶液的溶质质量分数是多少?(书写计算过程)(结果精确至0.1%) -
14、溶液与人类生产、生活密切相关。(1)、下列少量物质分别放入水中,充分搅拌,可以得到溶液的是______(填序号)。A、植物油 B、面粉 C、食盐(2)、下列有关说法正确的是______(填序号)。A、氢氧化钠固体溶于水时温度升高 B、氯化钠溶液中存在的微粒是、和 C、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液(3)、室温下小明做了如图所示对比实验,发现中固体消失而中几乎没有溶解,由此可知影响溶解性的因素有。
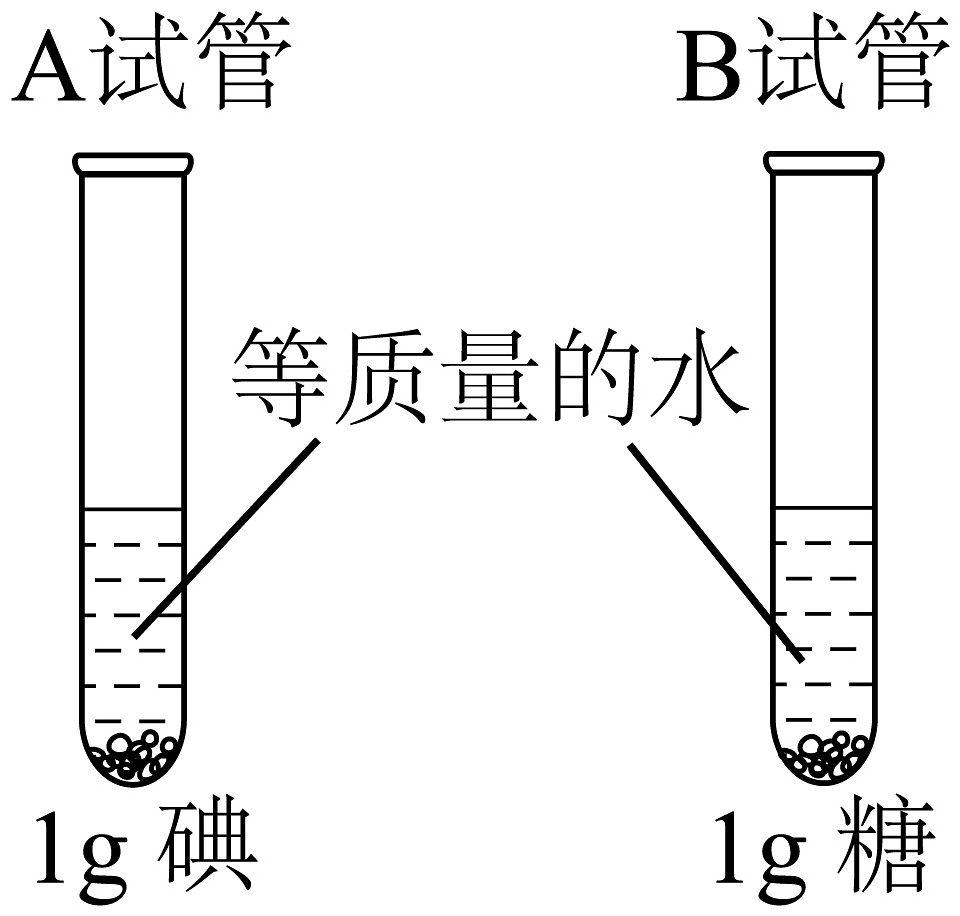 (4)、某同学配制溶质质量分数为的氯化钠溶液,整个操作过程如图所示,回答下列问题:
(4)、某同学配制溶质质量分数为的氯化钠溶液,整个操作过程如图所示,回答下列问题: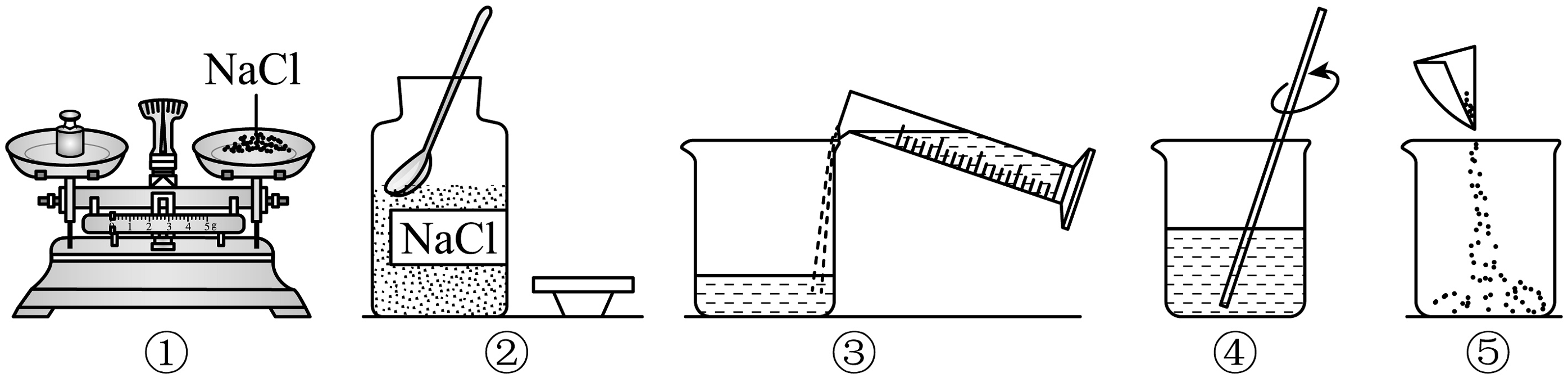
①配制溶液的正确操作顺序为(填字母)。
A.①②③④⑤ B.②①③④⑤ C.②①⑤③④
②配制溶液需要氯化钠固体的质量为。
③该实验操作中错误的是(填序号)。操作④中玻璃棒的作用是。
④经检测,该同学配制的溶液溶质质量分数偏小,可能的原因是(填字母)。
A.氯化钠固体不纯 B.用生锈砝码称量
C.装瓶时有少量溶液洒出 D.溶解前烧杯内壁有水珠
-
15、“见著知微,见微知著”是一种常用的化学思维方法。
如图中A、B、C、D是四种粒子的结构示意图,E是银元素在元素周期表中的信息。
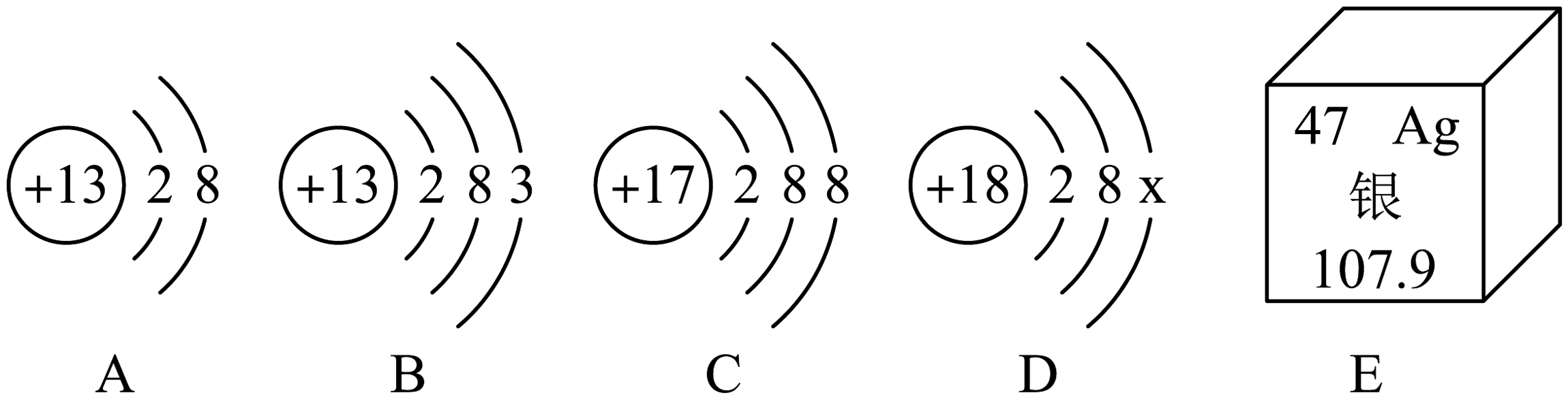
请回答下列问题:
(1)、图中A、B、C、D粒子共表示种元素。属于稀有气体元素的是。(2)、D中x=。(3)、粒子A的化学符号是。A、C形成化合物的化学式是。(4)、B在化学反应中易(填“得到”或“失去”)电子,与元素的化学性质关系最密切的是。(5)、E中银元素原子的相对原子质量为 , 一个银原子质量是一个碳12原子质量的倍。(6)、对于测量元素的相对原子质量贡献较大的中国科学家是______。A、张青莲 B、侯德榜
B、侯德榜 C、拉瓦锡
C、拉瓦锡 D、屠呦呦
D、屠呦呦
-
16、化学与生活、生产、科技息息相关,请运用化学知识回答下列问题。(1)、市场上食用钙片、补铁酱油中的“钙”、“铁”指的是 (填序号)。A、分子 B、原子 C、单质 D、元素(2)、蒸馏水不宜养鱼,是因为蒸馏水中几乎不含 (填序号)。A、氧元素 B、氧原子 C、氧分子 D、氧离子(3)、测体温时水银体温计中汞柱会上升,产生此现象的原因(从粒子角度解释)。(4)、现有的电解海水制氢技术,一般要先将海水进行淡化,然后再进行电解制氢。
①实验室除去水中的可溶性杂质,可采用的方法是。
②电解制氢的反应微观示意图如下,有关说法正确的是。(填序号)
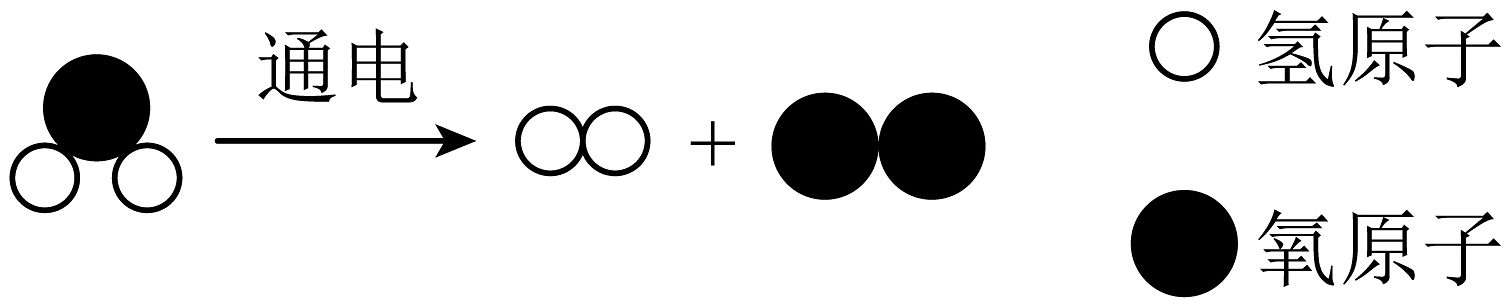
A.反应的符号表达:H2OH2+O2
B.产物中正极产生的气体能燃烧
C.反应的本质是分子分裂成原子,原子重新组合
D.该反应也可证明水是由氢、氧元素组成
(5)、嫦娥奔月“氢”相助。探测器用长征五号运载火箭发射,火箭的芯一级和芯二级采用液氧液氢发动机,液氢作火箭燃料的优点是。 -
17、化学用语是化学学习的重要组成部分,请用正确的化学用语填空:(1)、金刚石;(2)、氦气;(3)、氢氧化铝;(4)、氧化钠中钠元素的化合价为价;(5)、4个铁离子;(6)、相对分子质量最小的氧化物。
-
18、元素周期表中,同周期元素的结构和性质呈现一定的规律性变化。下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出)。下列有关说法不正确的是
元素
①
②
原子的最外层电子数
1
2
3
4
5
6
7
原子半径
③
最高正化合价
最低负化合价
④
⑤
A、⑤处的最高正化合价是 , 最低负化合价是 B、③处的数值介于之间 C、第三周期元素()的最高正化合价数等于其原子的最外层电子数 D、①和②形成的化合物中①显价,②显价,形成的化合物的化学式为 -
19、有的硝酸钾溶液,要使其溶质质量分数增加到 , 可采取的方法是( )A、增加硝酸钾固体 B、溶液温度升高 C、减少一半溶剂 D、蒸发掉的溶剂质量等于溶液质量的一半
-
20、根据微观模拟图所示,说法不正确的是
 A、反应物中有化合物 B、该反应是化合反应 C、生成物中有一种物质 D、参加反应的微粒个数比可能为
A、反应物中有化合物 B、该反应是化合反应 C、生成物中有一种物质 D、参加反应的微粒个数比可能为