-
1、
某研究小组以“食品中的脱氧剂”为主题进行项目式探究学习。
【任务一】认识脱氧剂的作用
(1)食品包装中加入脱氧剂的作用是 (填字母)。
A. 除去氧气,抑制霉菌生长 B. 防止食品因氧化而变色、变质 【任务二】探究脱氧剂的成分
(2)用剪刀剪开一包脱氧剂,倾倒于白纸上,观察到有黑色粉末和少量的白色固体。结合查阅的资料,推测黑色粉末可能是铁粉、活性炭、二氧化锰、四氧化三铁等。
探究过程
探究过程
实验现象
实验结论
①用磁铁靠近该混合物
部分黑色粉末被吸引
粉末可能含有________和 Fe3O4
②取少量磁铁上吸引的黑色
粉末于试管中,加入足量
稀盐酸。
黑色固体完全消失, ________
黑色粉末中含有铁粉;反应的化
学方程式:________。
③另取少量黑色粉末,采用以下装置灼烧。

烧杯内壁________
固体中含有活性炭。
资料还显示,脱氧剂中还含有食盐、生石灰、吸水性树脂等物质。
【任务三】解密脱氧原理
剪开一包脱氧剂,用磁铁靠近,将吸引的黑色粉末装入一个无纺布袋中,滴加 5~6 滴水,封口轻轻揉搓布袋。
(3)打开布袋看到黑色粉末变为红色,表明铁粉发生氧化生锈,其中食盐所起的作用是________。
(4)研究表明,脱氧剂中生石灰能吸收水蒸气,写出生石灰与水反应的化学方程式________。
(5)钢铁生锈腐蚀会造成巨大经济损失,常见的钢铁防腐蚀措施有________(写一种即可)。
-
2、二氧化碳为例,学习科学家研究物质的方法。
 (1)、1630年,海尔蒙特发现二氧化碳,进入久未开启的地窖需要做实验。(2)、1755年,布莱克第一个应用定量方法研究二氧化碳,主要过程如下图。
(1)、1630年,海尔蒙特发现二氧化碳,进入久未开启的地窖需要做实验。(2)、1755年,布莱克第一个应用定量方法研究二氧化碳,主要过程如下图。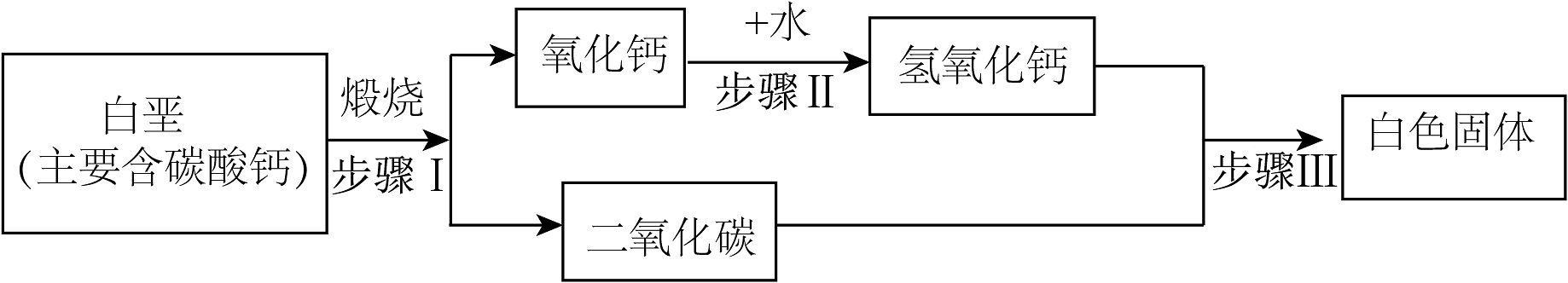
①白垩充分煅烧后(杂质不参与反应),固体减少的质量即为(填化学式)的质量。
②步骤Ⅲ中反应方程式为。
③实验室制取气体部分仪器与装置如下图:
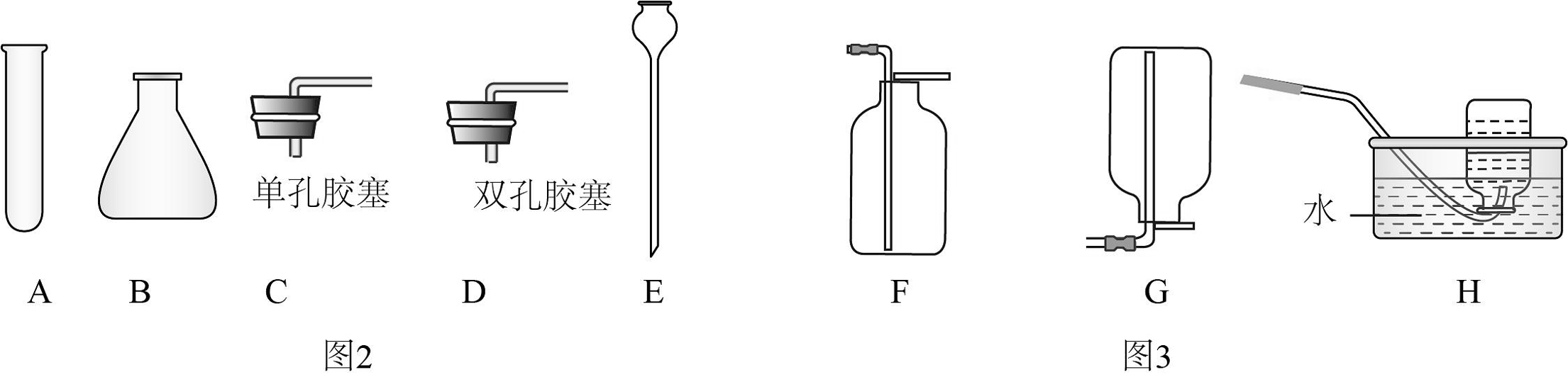
实验室制备二氧化碳的化学方程式是。组装连续产生较多气体的发生装置需选择的仪器为(填标号)。
(3)、1766年,卡文迪许测得:1体积水约能溶解1体积二氧化碳。图4所示针筒内二氧化碳与水充分混合后,针筒内的上液面将停留在mL处。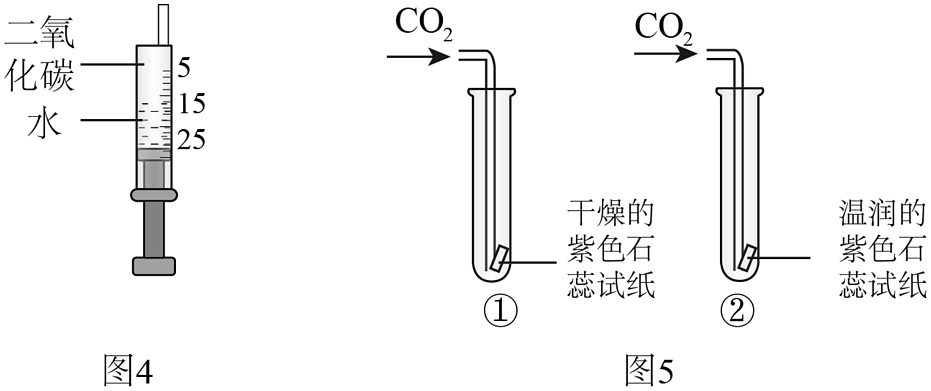 (4)、图5为模拟伯格曼实验,试管②的现象为 , 试管①实验所起的作用是。
(4)、图5为模拟伯格曼实验,试管②的现象为 , 试管①实验所起的作用是。 -
3、火箭推进剂对火箭的性能起着至关重要的作用。偏二甲肼(C2H8N2)-四氧化二氮(N2O4)推进剂混合即反应,完全燃烧产物无毒,但本身有毒性和腐蚀性。煤油-液氧推进剂价格便宜,但易积碳。液氢-液氧推进剂动力大,反应产物无污染,但氢气沸点和密度低,不易储存。甲烷-液氧推进剂兼顾高性能低成本,积碳不突出,是新一代理想推进剂。
火箭常采用分级设计,可减少推进剂用量,推进剂消耗完相应设备会自动分离(如题图所示)。
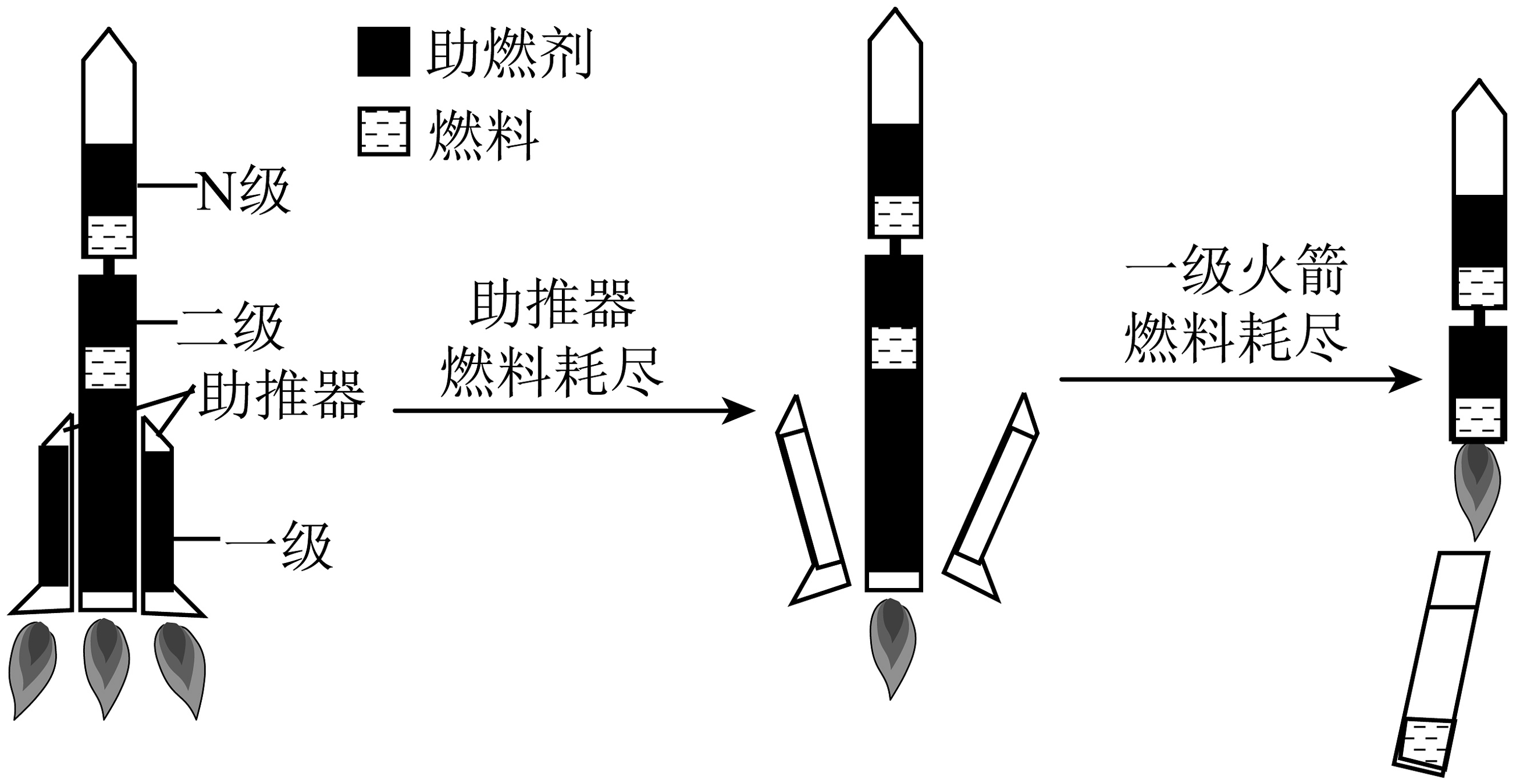
结合上文,回答下列问题。
(1)、火箭向上的推力来自燃料燃烧热量并喷出高温气体,产生反作用力。完全没有积碳(形成碳单质堆积)问题的推进剂为(写一种)。(2)、偏二甲肼燃烧方程式:C2H8N2+2N2O4=2CO2+4H2O+3X,X的化学式为。(3)、分级火箭发射过程中,先于一级火箭分离的设备是;为了减小重力的影响,火箭外壳选用铝合金,最主要是利用了铝合金的优点(填字母)。a.密度小 b.熔点高 c.耐腐蚀
(4)、朱雀二号是全球首枚成功入轨的甲烷-液氧火箭,甲烷燃烧的化学方程式为。请你设计实验证明甲烷中含有碳元素。 -
4、龙是中华民族的图腾。石器时代的“玉龙”、秦代的“青铜龙”、唐代的“鎏金铁芯铜龙”(如图)文物的制造体现了古人的智慧。
 (1)、三件文物中,所含主要材质不属于金属材料的是。(2)、铁芯外表包铜可耐腐蚀,原因是铜的活动性比铁(填“强”或“弱”)。(3)、“取炉甘石,研之细末,和以赤铜,置炭火中煅烧。……熄火取铜,其色如金。”赤铜为Cu2O,其铜、氧元素的质量比为。炉甘石主要成分是ZnCO3 , 煅烧反应生成两种氧化物的化学方程式为 , “熄火取铜”中所得“铜”与纯铜相比,硬度(填“更大”“更小”或“相等”)。(4)、鎏金工艺是指在器物表面涂抹金汞齐(金汞合金),加热祛汞,冷却,器物表面形成金膜。鎏金工艺利用的知识有(多选)。
(1)、三件文物中,所含主要材质不属于金属材料的是。(2)、铁芯外表包铜可耐腐蚀,原因是铜的活动性比铁(填“强”或“弱”)。(3)、“取炉甘石,研之细末,和以赤铜,置炭火中煅烧。……熄火取铜,其色如金。”赤铜为Cu2O,其铜、氧元素的质量比为。炉甘石主要成分是ZnCO3 , 煅烧反应生成两种氧化物的化学方程式为 , “熄火取铜”中所得“铜”与纯铜相比,硬度(填“更大”“更小”或“相等”)。(4)、鎏金工艺是指在器物表面涂抹金汞齐(金汞合金),加热祛汞,冷却,器物表面形成金膜。鎏金工艺利用的知识有(多选)。a.汞的沸点低 b.汞被氧化变成氧化汞 c.金汞合金熔点比组分纯金属低
-
5、已知甲、乙、丙、丁是初中化学常见的四种物质,甲能使澄清石灰石变浑浊,乙能使带火星的木条复燃,丙是人体中含量最多的物质,(“→”表示物质之间的转化,反应条件、部分反应物和生成物已省略)。下列说法不正确的是
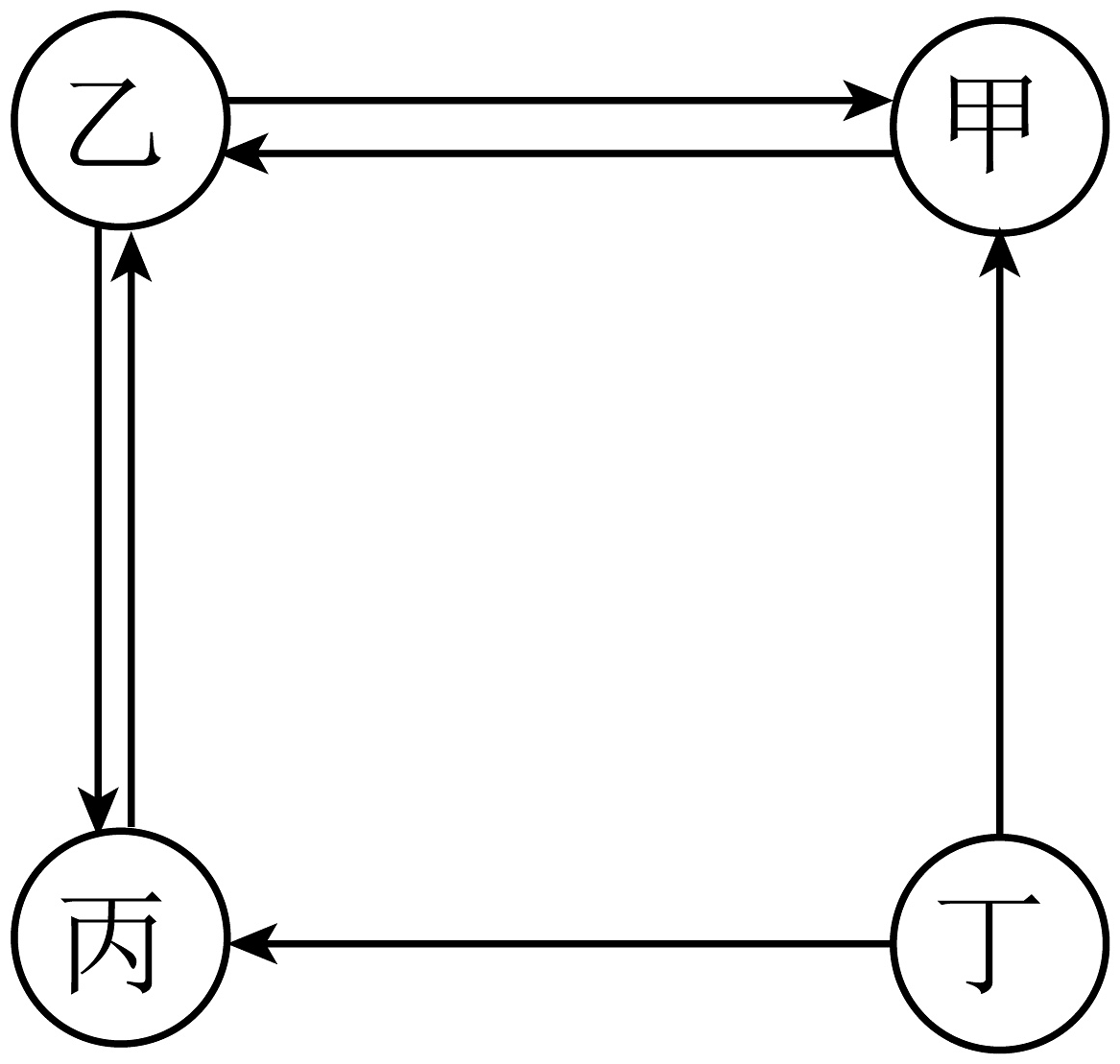 A、甲→乙能通过植物的光合作用来实现 B、若丁是酒精,则甲、乙、丙、丁中可能含有一种相同的元素 C、乙→丙一定是氢气燃烧 D、乙一定是由地壳中含量最多的元素组成的
A、甲→乙能通过植物的光合作用来实现 B、若丁是酒精,则甲、乙、丙、丁中可能含有一种相同的元素 C、乙→丙一定是氢气燃烧 D、乙一定是由地壳中含量最多的元素组成的 -
6、下列实验设计不能达到实验目的的是
选项
实验目的
实验设计
A
除去K2MnO4中的KMnO4
在试管中充分加热
B
除去CuO中少量的C
在空气中充分灼烧
C
鉴别氧气与氮气
将带火星木条分别放入气体中,观察现象
D
鉴别过氧化氢溶液和水
分别加少量二氧化锰粉末,观察现象
A、A B、B C、C D、D -
7、用下图所示四个实验探究二氧化碳能否与水反应,实验中所用的纸花均用石蕊染成紫色并干燥下列说法错误的是
 A、①和④的紫色纸花会变红 B、对比①③,推断④有酸性物质生成 C、对比④纸花放入集气瓶前后的现象,省略②也能得出同样的实验结论 D、综合①②③④可得出的结论是:二氧化碳能与水反应生成碳酸,且碳酸很稳定
A、①和④的紫色纸花会变红 B、对比①③,推断④有酸性物质生成 C、对比④纸花放入集气瓶前后的现象,省略②也能得出同样的实验结论 D、综合①②③④可得出的结论是:二氧化碳能与水反应生成碳酸,且碳酸很稳定 -
8、氘和氚是制造氢弹的原料。氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是
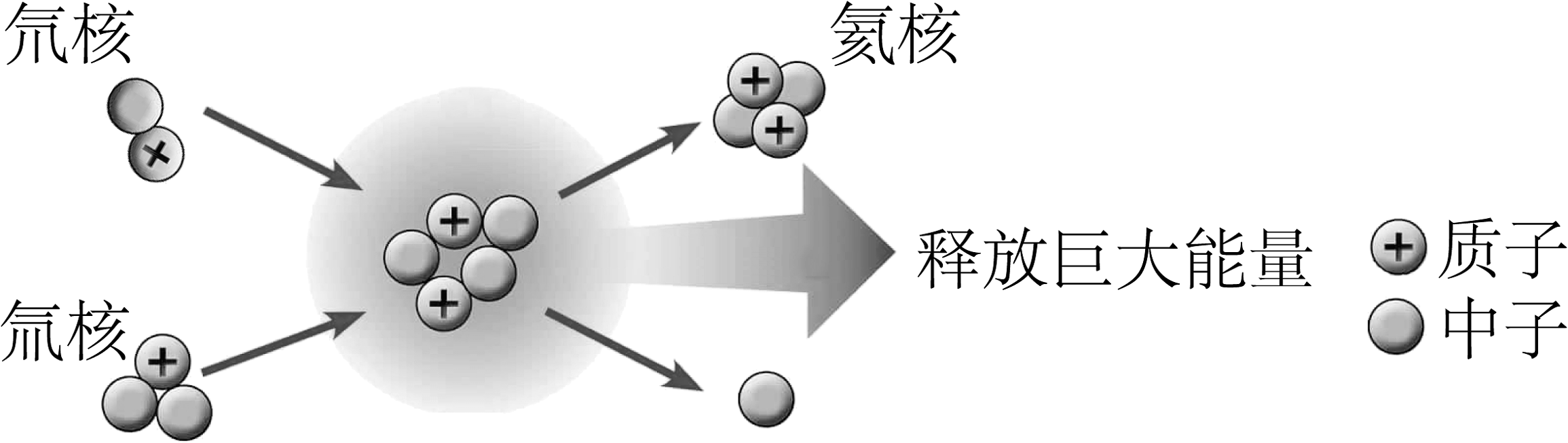 A、该变化属于化学变化 B、氚、氦两种原子的质子数相同 C、该变化涉及的元素有二种 D、氘原子和氚原子的相对原子质量相等
A、该变化属于化学变化 B、氚、氦两种原子的质子数相同 C、该变化涉及的元素有二种 D、氘原子和氚原子的相对原子质量相等 -
9、华为新款智能手机采用“中国芯”。制造芯片的重要材料是硅,如图是工业制取高纯硅部分反应原理的微观示意图。下列说法错误的是
 A、一个甲分子由五个原子构成 B、该反应中乙具有还原性,发生还原反应 C、参加反应的乙和生成的丁的体积比是1∶2 D、该反应的化学方程式为:SiCl4+2H2Si+4HCl
A、一个甲分子由五个原子构成 B、该反应中乙具有还原性,发生还原反应 C、参加反应的乙和生成的丁的体积比是1∶2 D、该反应的化学方程式为:SiCl4+2H2Si+4HCl -
10、下列有关燃烧与灭火的说法错误的是A、物质燃烧时一定伴随着发光、放热 B、吹灭蜡烛的灭火原理是隔绝氧气 C、精密仪器着火可用液态二氧化碳灭火 D、煤气泄漏应先关闭阀门,再开窗通风
-
11、下列化学用语的意义描述正确的是A、2N2:2个氮原子 B、Ba2+:1个钡离子带2个单位正电荷 C、2H:2个氢元素 D、Na+:钠元素的化合价为+1
-
12、变瘪的气球充入氦气,气球鼓胀起来。从分子角度描述球内发生的变化正确的是A、氦气分子的体积变大 B、氦气分子间的间隔变大 C、氦气分子个数增多 D、氦气分子分裂生成了新的分子
-
13、诺贝尔化学奖获得者List曾用有机催化剂脯氨酸(C5H9NO2)研究催化反应,其结构模型如图,有关脯氨酸的说法正确的是
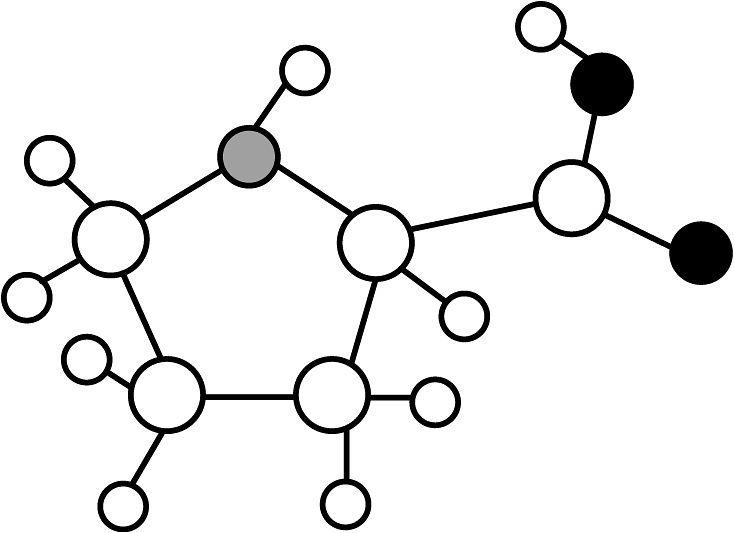 A、脯氨酸由17个原子构成 B、脯氨酸结构中含有NO2分子 C、氢元素的质量分数最小 D、催化剂反应后其化学性质发生改变
A、脯氨酸由17个原子构成 B、脯氨酸结构中含有NO2分子 C、氢元素的质量分数最小 D、催化剂反应后其化学性质发生改变 -
14、空气和水是一切生命体生存所必需的物质。下列关于空气和水的说法,正确的是A、空气中氮气的质量分数约为78% B、氧气可以用于卫星发射的助燃剂 C、为节约用水,直接用工业废水灌溉农田 D、电解水实验中,正极与负极产生气体的质量比约为1:2
-
15、高锰酸钾( KMnO4)常用于实验室制取氧气。高锰酸钾属于A、化合物 B、氧化物 C、单质 D、混合物
-
16、能造成酸雨的气体是A、二氧化碳 B、一氧化碳 C、氮气 D、二氧化硫
-
17、中华文明源远流长,以下我国古代发明或技术应用的原理中发生化学变化的是A、木器涂漆 B、烧制陶瓷 C、炭黑制墨 D、竹编花篮
-
18、氧化亚铜 Cu2O 可用于生产船底防污漆。现将 Cu2O 和 Cu 的固体混合物 20g 放入烧杯中,加入质量分数为 24.5%的稀硫酸 50g,恰好完全反应。已知:Cu2O+H2SO4=CuSO4+Cu+H2O。计算:(1)、所加稀硫酸中溶质的质量为g。(2)、求混合物中 Cu2O 的质量。(写出计算过程)(3)、氧化亚铜可用 2CuSO4+3Na2SO3=Cu2O+3Na2SO4+SO2↑ 原理制备。SO2化学性质与 CO2相似。
①反应过程中产生 SO2可循环利用,因此应该选用溶液来吸收它。
②已知 SO2与水反应生成 H2SO3 , 反应过程中溶液 pH 将(填“变大”“变小”或“不变”),因此制备过程要控制溶液的酸碱度,如果反应时溶液 pH 过小,会导致产品下降,原因是。
-
19、
金属作为一种重要的材料,对生产生活、社会发展有着重要作用。
【活动一】话说金属的冶炼
(1)战国《韩非子•内储说上》提到,早期采金技术均是“沙里淘金”。黄金能以单质形式存在于自然界的原因是。
(2)“胆铜法”(铁与硫酸铜溶液反应)是宋代和元代湿法炼铜的重要方法之一、图1为该反应的微观示意图,其中未参加反应的微观粒子是(用离子符号填空),该反应的实验现象是金属表面 , 溶液由。

(3)明代宋应星所著的《天工开物》中有关“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”此工艺过程分解模拟如图2。(已知:Zn的冶炼温度为904℃,Zn的沸点为906℃。)请结合图文信息,分析思考,解决问题:

①装入原料器之前,将炉甘石敲碎的目的是。
②高温炉内,碳酸锌(ZnCO3)在高温条件下与煤的主要成分碳发生反应生成Zn和CO,反应的化学方程式为 , 属于反应(填基本反应类型)。
【活动二】探究金属活动性顺序
(4)为验证铁、铜、银的金属活动性顺序,同学设计了以下实验(如图3):

欲验证铁、铜、银这三种金属活动性顺序,实验④中X和Y的试剂组合是、。
-
20、
小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性。
【作出猜想】
(1)所得溶液可能呈碱性,也可能呈性,还可能呈性。【实验验证】
(2)填写空白处实验操作
现象
结论
取该溶液1~2 mL置于试管中,滴入1~2滴无色酚酞溶液,振荡
溶液变成
溶液呈碱性
溶液不变色
溶液呈
【分析与思考】
(3)若溶液呈碱性,则溶液中使其呈碱性的离子是(填离子符号)。(4)若溶液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案∶方案一:取样,加入氧化铜粉末,若观察到消失,溶液变 , 则所取溶液呈酸性;若无明显现象,则呈中性。
方案二:取样,加入适量的锌粒,若观察到有产生,则所取溶液呈酸性,反应的化学方程式为;若无明显现象,则呈中性。