-
1、神舟十九号载人飞船于2024年10月30日4时27分在酒泉卫星发射中心发射,飞船采用超宽铝合金薄板,这样做是为了减重需要,铝合金属于A、非金属材料 B、金属材料 C、合成材料 D、复合材料
-
2、空气,这个珍贵的自然资源由氮气、氧气、稀有气体、二氧化碳以及其他微量气体构成。随着人类工业的不断进步,空气质量问题日益受到全球关注。保护空气,减少温室气体排放,已经成为国际社会的共同目标。在这样的背景下,“双碳”战略应运而生。请完成下面小题(1)、地球上的氧气孕育了万物,下列有关氧气的说法正确的是A、氧气的化学性质非常活跃,具有助燃性,能与许多物质发生化学反应 B、为了延长食物的保质期,可以在食物的包装袋中充入氧气 C、在氧气中点燃红磷,能剧烈燃烧,产生大量白色烟雾 D、硫粉在空气中点燃后,发出淡蓝色火焰,生成无色且具有刺激性气味的气体(2)、空气是个宝,人人要保护好。下列有关空气的说法不正确的是A、空气是一种混合物 B、空气中体积含量最多的是氧气 C、二氧化硫和二氧化氮属于空气污染物 D、空气中的氮气可以作为食品的保护气体(3)、引领绿色生活,紧跟“双碳”战略,共筑绿色未来,旨在通过控制温室气体排放,实现环境保护。下列围绕这个主题,对碳氧化物分析不正确的是A、大力发展新能源汽车,减少汽车尾气中CO,NO等有害气体的排放 B、气体可用于灭火,制作碳酸饮料,但会引起酸雨 C、植树造林可以吸收二氧化碳,一氧化碳可用于冶炼金属,两者都涉及化学反应 D、工业上可以通过碱吸收二氧化碳的方法减少二氧化碳的排放
-
3、下列实验操作不规范的是A、
 检查气密性
B、
检查气密性
B、 量筒液体读数
C、
量筒液体读数
C、 点燃酒精灯
D、
点燃酒精灯
D、 测溶液的pH
测溶液的pH
-
4、酒精,作为一种常见的有机化合物,其化学式为 , 在人们的生产生活中有着广泛的应用。在餐桌上,火锅的燃料中常常含有酒精;在诊所中,酒精被用作火罐的燃料,同时也是一中重要的医疗物质。请完成下面小题(1)、根据其化学式为 , 下列说法正确的是A、酒精是由2个碳原子,6个氢原子,1个氧原子构成 B、酒精属于氧化物 C、酒精中氢元素质量分数最小 D、酒精中含有碳,氢,氧三个元素(2)、下列关于酒精的应用中,只涉及物理变化的是A、餐桌上用作火锅燃料 B、诊所中用作火罐的燃料 C、用酒精进行医疗消毒 D、用酒精作为降温剂(3)、人们对酒精的有关认识正确是A、酒精是乙醇的俗名 B、酒精无毒,可以大量饮用 C、酒精的挥发性强,因此不易燃烧 D、酒精是不可再生能源
-
5、阅读下列材料并回答问题。
伴随着国家“双碳”战略的深入实施,枣庄积极抢占锂电产业起飞的“时代风口”,将锂电作为促进城市转型发展的首位产业来培育,昔日能源基地“变身”锂电之都。
锂电池是一种二次电池,具有电压高、能量密度大、循环寿命长、安全性能好、自放电小、充电快速、工作温度范围较宽等优点。某种锂电池结构如图1所示。
锂电池负极材料占成本比例较低,正极材料占成本比例较高,大约占电池成本的30%。目前已批量应用的正极材料除磷酸铁锂外还有钴酸锂、钴镍锰酸锂、锰酸锂等。不同正极材料的性能如下表所示。
正极材料
能量密度(mAh/g)
平均输出电压(V)
循环次数
磷酸铁锂
130-150
3.2-3.3
钴酸锂
135-145
36
钴镍锰酸锂
155-190
3.5-3.6
锰酸锂
100-120
3.7-3.9
锂电池在使用过程中容量会缓慢衰退、不耐受过充过放。储存过程中锂电池的容量也会缓慢衰退,衰退速率可用单位时间容量减小百分率来表示,衰退速率与充电电量和储存温度的关系如图2所示。
随着科学技术的发展,更多性能优良的锂电池将会被广泛应用。
 (1)、锂电池的优点有(任写一点)。(2)、在图1所示的锂电池中,铜能制成超薄材料是因为单质铜具有良好的(选填“导电性”“导热性”或“延展性”)。(3)、由表可知,锂电池正极材料能量密度最高的是。(4)、根据图2分析,下列储存条件最优的是__________(填字母)。A、充电电量50%,储存温度25℃ B、充电电量100%,储存温度40℃ C、充电电量50%,储存温度40℃ D、充电电量100%,储存温度25℃
(1)、锂电池的优点有(任写一点)。(2)、在图1所示的锂电池中,铜能制成超薄材料是因为单质铜具有良好的(选填“导电性”“导热性”或“延展性”)。(3)、由表可知,锂电池正极材料能量密度最高的是。(4)、根据图2分析,下列储存条件最优的是__________(填字母)。A、充电电量50%,储存温度25℃ B、充电电量100%,储存温度40℃ C、充电电量50%,储存温度40℃ D、充电电量100%,储存温度25℃ -
6、 实验小组取一定量的稀盐酸于烧杯中,向其中逐滴加入氢氧化钠溶液,通过数字传感器测得烧杯中溶液的pH和温度变化曲线如图所示。
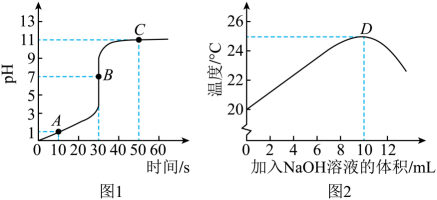 (1)、分析图1的曲线,当反应进行至点时,溶液呈性;若用酚酞溶液作该反应的指示剂,溶液在点时呈色。(2)、分析图1和图2的曲线,可知该反应属于(填“吸热”或“放热”)反应,点对应的时间:第s。(3)、若烧杯中盛放10g溶质质量分数为的稀盐酸,计算恰好完全反应时,消耗氢氧化钠的质量。(写出计算过程)
(1)、分析图1的曲线,当反应进行至点时,溶液呈性;若用酚酞溶液作该反应的指示剂,溶液在点时呈色。(2)、分析图1和图2的曲线,可知该反应属于(填“吸热”或“放热”)反应,点对应的时间:第s。(3)、若烧杯中盛放10g溶质质量分数为的稀盐酸,计算恰好完全反应时,消耗氢氧化钠的质量。(写出计算过程) -
7、 氧气在生产、生活和生命活动中发挥着重要作用。兴趣小组以“氧气的制备”为主题开展了项目式学习活动。
I、实验室制氧气
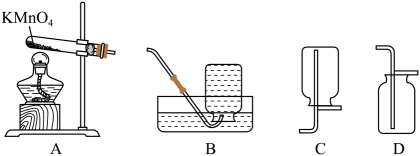 (1)、用A装置制取氧化,反应的化学方程式为 , 基本反应类型为。(2)、若要收集一瓶较为纯净的氧气,应选择的收集装置是(填序号)。
(1)、用A装置制取氧化,反应的化学方程式为 , 基本反应类型为。(2)、若要收集一瓶较为纯净的氧气,应选择的收集装置是(填序号)。Ⅱ、工业制氧气
(3)、利用分离液态空气法制氧气。在低温下加压,使空气转变为液态,当液态空气升温时,由于液氮沸点比液氧沸点 , 液氮先汽化,剩下的主要是液氧。(4)、利用膜分离法制氧气。如下图所示,利用氧分子的体积(填“大于”“小于”或“等于”)氮分子的体积实现分离,从而获得高浓度的氧气。 (5)、Ⅲ、空间站内的氧气再生空间站内电解产生的供航天员呼吸,产生的与航天员呼出的通过“萨巴蒂尔反应”系统转化为和 , 生成的再进行电解,实现的再生。示意图如下。
(5)、Ⅲ、空间站内的氧气再生空间站内电解产生的供航天员呼吸,产生的与航天员呼出的通过“萨巴蒂尔反应”系统转化为和 , 生成的再进行电解,实现的再生。示意图如下。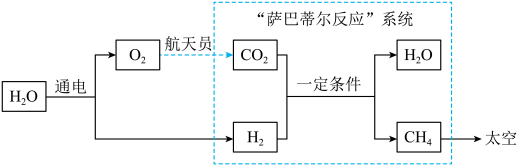
“萨巴蒂尔反应”系统中发生反应的化学方程式为。(6)、电解水的质量为 , “萨巴蒂尔反应”系统中生成水的质量为的原因是。(忽略非反应损耗) -
8、 实验小组对Al和溶液的反应进行探究。
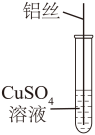 (1)、根据金属活动性顺序AlCu,小组同学一致认为Al和溶液能够发生反应。(2)、小林将铝丝浸入溶液一段时间,没有观察到明显现象。结合铝的化学性质分析,原因是。(3)、小艺对小林的实验操作进行了改进,观察到明显现象。小艺的实验操作是 , 观察到的实验现象是。
(1)、根据金属活动性顺序AlCu,小组同学一致认为Al和溶液能够发生反应。(2)、小林将铝丝浸入溶液一段时间,没有观察到明显现象。结合铝的化学性质分析,原因是。(3)、小艺对小林的实验操作进行了改进,观察到明显现象。小艺的实验操作是 , 观察到的实验现象是。 -
9、 宋代《开宝本草》中记载了的制取过程,“所在山泽,冬月地上有霜,扫取以水淋汁后,乃煎炼而成”。据此回答下列问题。(1)、“地上有霜”,是在“冬月”因温度降低,溶解度(域“增大”“减小”或“不变”)而结晶析出。(2)、“扫取”时常会混入泥沙,“以水淋汁”是进行溶解,再用的方法除去难溶性杂质。(3)、“煎炼”至有晶体析出时,溶液是(填“饱和”或“不饱和”)溶液。(4)、你认为通过以上制取过程能否得到纯净的 , 判断并说明理由:。
-
10、 阅读科普短文,回答下列问题。
内蒙古的特色饮品奶茶是先用砖茶制成茶汤,后加牛奶再撒少许食盐熬制而成。砖茶中含有30多种酚类物质,总称为茶多酚。茶多酚是决定茶叶色、香、味的重要成分,有降血压、抗衰老等保健功能,易溶于温水,在潮湿的空气中易被氧化。
为适应快节奏生活,将制作奶茶的原料加工成奶茶粉,深受现代人们的喜爱。某种奶茶粉冲调时,溶解的茶多酚含量随水温的变化如图1所示。冲调后,恒温下测得溶解的茶多酚含量随搁置时间的变化如图2所示。
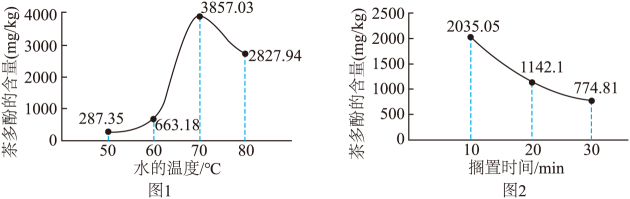
奶茶有补充营养、改善情绪等功效,但是过度饮用会导致糖分、脂肪等摄入过多,引起肥胖,不利于人体健康。
(1)、熬制奶茶的原料中富含蛋白质的物质是。(2)、茶多酚所属的物质类别为(填“混合物”或“纯净物”)。(3)、结合短文,据图1分析,奶茶粉的最佳冲调温度为℃;据图2分析,茶多酚含量随着搁置时间延长逐渐减少,原因可能是。 -
11、 小羽设计如图装置进行“可燃物燃烧条件”的验证实验。将等质量的白磷置于①②③处,观察到①处白磷燃烧,②③处白磷不燃烧。下列说法不正确的是( )
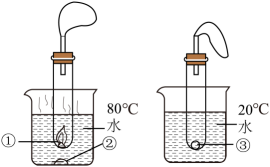 A、对比①③处现象,说明可燃物燃烧需要温度达到着火点 B、对比①②处现象,说明可燃物燃烧需要空气(氧气) C、②③处白磷均不燃烧的原因相同 D、装置中气球可以起到防止污染空气的作用
A、对比①③处现象,说明可燃物燃烧需要温度达到着火点 B、对比①②处现象,说明可燃物燃烧需要空气(氧气) C、②③处白磷均不燃烧的原因相同 D、装置中气球可以起到防止污染空气的作用 -
12、 乙醇是重要的有机溶剂,工业上用乙烯与水在一定条件下制取,该反应的微观示意图如下、下列说法正确的是( )
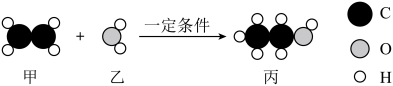 A、反应前后原子种类没有改变 B、反应前后分子数目没有改变 C、该反应中共涉及2种氧化物 D、甲中碳元素和氢元素的质量比是1:2
A、反应前后原子种类没有改变 B、反应前后分子数目没有改变 C、该反应中共涉及2种氧化物 D、甲中碳元素和氢元素的质量比是1:2 -
13、 碳是给人类社会提供能源和材料的主要元素。下列含碳元素物质的性质与用途对应关系不正确的是( )
选项
性质
用途
A
活性炭具有很强的吸附性
可作净水材料
B
石墨具有优良的导电性
可制铅笔芯
C
干冰容易升华
可作制冷剂
D
甲烷具有可燃性且热值高
可作气体燃料
A、A B、B C、C D、D -
14、 超临界水是将水加热到超过并加压到超过219个大气压,使水处于气、液相互交融的状态。超临界水减压转化为水蒸气的过程中,从微观角度分析发生改变的是( )A、分子的间隔 B、分子的大小 C、分子的质量 D、分子的种类
-
15、 镝是一种稀土元素,可用于制造硬盘驱动器和电动汽车引擎。镝元素在元素周期表中的信息如图所示。下列说法不正确的是( )
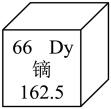 A、镝属于金属元素 B、镝的元素符号为Dy C、镝原子的核电荷数是66 D、一个镝原子的质量为162.5g
A、镝属于金属元素 B、镝的元素符号为Dy C、镝原子的核电荷数是66 D、一个镝原子的质量为162.5g -
16、 兴趣小组开展了“探究土壤酸碱性对植物生长的影响”跨学科实践活动。下列有关实验操作规范的是( )A、
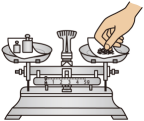 称量土样
B、
称量土样
B、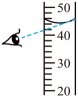 量取蒸馏水
C、
量取蒸馏水
C、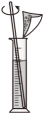 溶解土样
D、
溶解土样
D、 测酸碱度
测酸碱度
-
17、 2025年4月,神舟二十号载人飞船在长征二号F遥二十运载火箭托举下顺利升空,并与中国空间站精准对接。下列相关过程以化学变化为主的是( )A、火箭与飞船合体完成组装 B、引燃推进剂实现火箭发射 C、飞船入轨后展开太阳能帆板 D、导航系统引导飞船精准对接
-
18、下列对宏观事实的微观解释错误的是A、金刚石硬度大而石墨质软——碳原子的排列方式不同 B、变瘪的乒乓球放入热水中能鼓起来——温度升高,分子体积变大 C、氢气和液氢都可作燃料——同种分子的化学性质相同 D、酸具有相似的化学性质——在水中都解离出氢离子
-
19、在中国制造2025计划中,芯片产业是非常重要的环节。氮化镓是制造芯片的材料之一,如图是镓元素(Ga)的原子结构示意图及元素周期表的一部分。下列说法不正确的是
 A、镓属于金属元素,m=3 B、镓与铝的最外层电子数相同 C、镓形成的阳离子为Ga3+ D、锗的最外层电子数为5
A、镓属于金属元素,m=3 B、镓与铝的最外层电子数相同 C、镓形成的阳离子为Ga3+ D、锗的最外层电子数为5 -
20、选用如图装置进行氧气的制取实验。
 (1)、仪器①的名称是 , 实验室用高锰酸钾制取并收集一瓶较干燥的氧气,应选择的装置组合是。(2)、能用向上排空气法收集O2的原因是。(3)、需要收集一瓶氧气用于铁丝在氧气中燃烧的实验,应选择的收集装置是。
(1)、仪器①的名称是 , 实验室用高锰酸钾制取并收集一瓶较干燥的氧气,应选择的装置组合是。(2)、能用向上排空气法收集O2的原因是。(3)、需要收集一瓶氧气用于铁丝在氧气中燃烧的实验,应选择的收集装置是。