-
1、
物质发生化学反应前后,总质量是否发生改变?是增加、减小还是不变?甲同学、乙同学、丙同学按下面的步骤进行探究:

【提出假设】物质发生化学反应前后总质量不变。
【设计并进行实验】甲同学设计的实验装置和选用的药品如图A所示,乙设计的实验装置和选用的药品如图B所示,丙同学设计的实验装置和选用的药品如图C所示,他们在反应前后都进行了规范的操作、准确的称量和细致的观察。
(1)甲同学用图A所示实验,把锥形瓶加热,在加热的过程中气球的变化是;实验时若取用铜粉的量不足,对实验的结果(填“有”或“没有”)影响。写出该过程中发生反应的化学方程式:。
(2)丙同学在实验过程中观察到的现象是。
【结论与解释】
(3)甲和丙同学认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量相等。
乙和丙同学认为:在化学反应中,反应后生成的各物质的总质量与参加反应的各物质的总质量不相等。
你认为导致甲和丙同学的结论正确,乙同学实验结论错误的原因是;请从原子的角度分析,你认为正确的结论的原因:。
【反思与评价】
(4)在探究化学反应中反应物和生成物的质量关系时,若。
-
2、
为探究某塑料的组成元素,设计了实验Ⅰ和Ⅱ。
Ⅰ.制取氧气

(1)仪器①的名称为。
(2)若用一种暗紫色固体制取 , 发生反应的化学方程式为。
(3)欲制取干燥的 , 装置合理的连接顺序:发生装置→C→(填字母)。
Ⅱ.组成探究

(4)定性检测(已知:无水遇水变为蓝色)
实验操作
实验现象
结论
连接装置,检查气密性,装入试
剂并按上图进行实验。通入O2 ,
一段时间后,点燃J处酒精灯
装置K中无水CuSO4变为色
塑料燃烧产物中有H2O
装置L中
塑料燃烧产物中有CO2
由上述实验可知,该塑料一定含有的元素是(填元素符号)。
(5)定量测定
为进一步确定组成,将1.4g该塑料在足量中完全燃烧,共产生了和1.8g , 依据质量守恒定律,可判断该塑料(填“含有”或“不含”)除上述(4)中结论之外的元素。
-
3、阅读材料,回答下列问题:
材料一:1673年,波义耳曾经做过一个实验:在密闭的曲颈瓶中加热金属时,得到了金属灰,冷却后打开容器,称量金属灰的质量,发现与原来金属相比质量增加了。
材料二:1703年,施塔尔提出“燃素学说”,其主要观点:
①燃素是组成物体的一种成分,一般条件下被禁锢在可燃物中;②燃素在可燃物燃烧时会分离出来,且燃素可穿透一切物质。
材料三:1756年,罗蒙诺索夫重做了波义耳的实验。他将金属铅装入容器后密封、称量。然后把容器放到大火上加热,银白色的金属变成了灰黄色,待容器冷却后再次称量,发现容器的总质量没有发生变化。罗蒙诺索夫对此的解释是“容器里原来有一定量的空气,且容器中的空气质量减少多少,金属灰的质量就比金属增加多少,在化学变化中物质的质量是守恒的。”后来,拉瓦锡等科学家经过大量的定量实验,推翻了“燃素学说”,质量守恒定律得到公认。
(1)、波义耳实验中,金属灰增加的质量是。(2)、由“燃素学说”可知,物质燃烧后质量应该减少。请根据所学知识写出一个可以推翻“燃素学说”的事实:。因此要验证质量守恒定律,必须在装置内进行。(3)、罗蒙诺索夫重做波义耳的实验是基于金属加热后,增加的质量并非来自燃素而是来自的假设。由此分析可知,波义耳错过了发现质量守恒定律的一个重要原因是。(4)、小丽认为,蜡烛燃烧后剩下的固体质量比燃烧前减少了,因此该现象不符合质量守恒定律。请你设计一个能说服小丽的简明实验思路:。(5)、质量守恒定律的发现过程,带给我们的启示有_____(填字母)。A、要善于总结前人的成果和经验 B、实验的成功与否,取决于药品的选择 C、定量方法是科学研究的重要方法 -
4、质量守恒定律在生产、生活中的应用。(1)、硝酸是工业上一种常用的强酸。工业上制取硝酸的过程中,会发生一系列化学反应,其中一个反应的化学方程式为。
①X的化学式为 , 你判断的依据是。
②NO是大气污染物之一,但少量NO在人体内具有扩张血管、增强记忆的功能。NO难溶于水,通常条件下极易与氧气反应,生成+4价氮的氧化物,NO在空气中反应的化学方程式是。
(2)、用可以测定空气受CO污染的程度,发生反应的化学方程式为①该反应中属于单质的是。
②从宏观上看:参加反应的CO的质量(填“大于”“小于”或“等于”,下同)生成的CO2的质量。
③从微观上看:参加反应的各物质中的氧原子总数生成物中的氧原子总数。
-
5、下图是O2与其他物质之间的转化关系(“→”表示物质之间可发生转化,部分物质已省略),下列说法正确的是
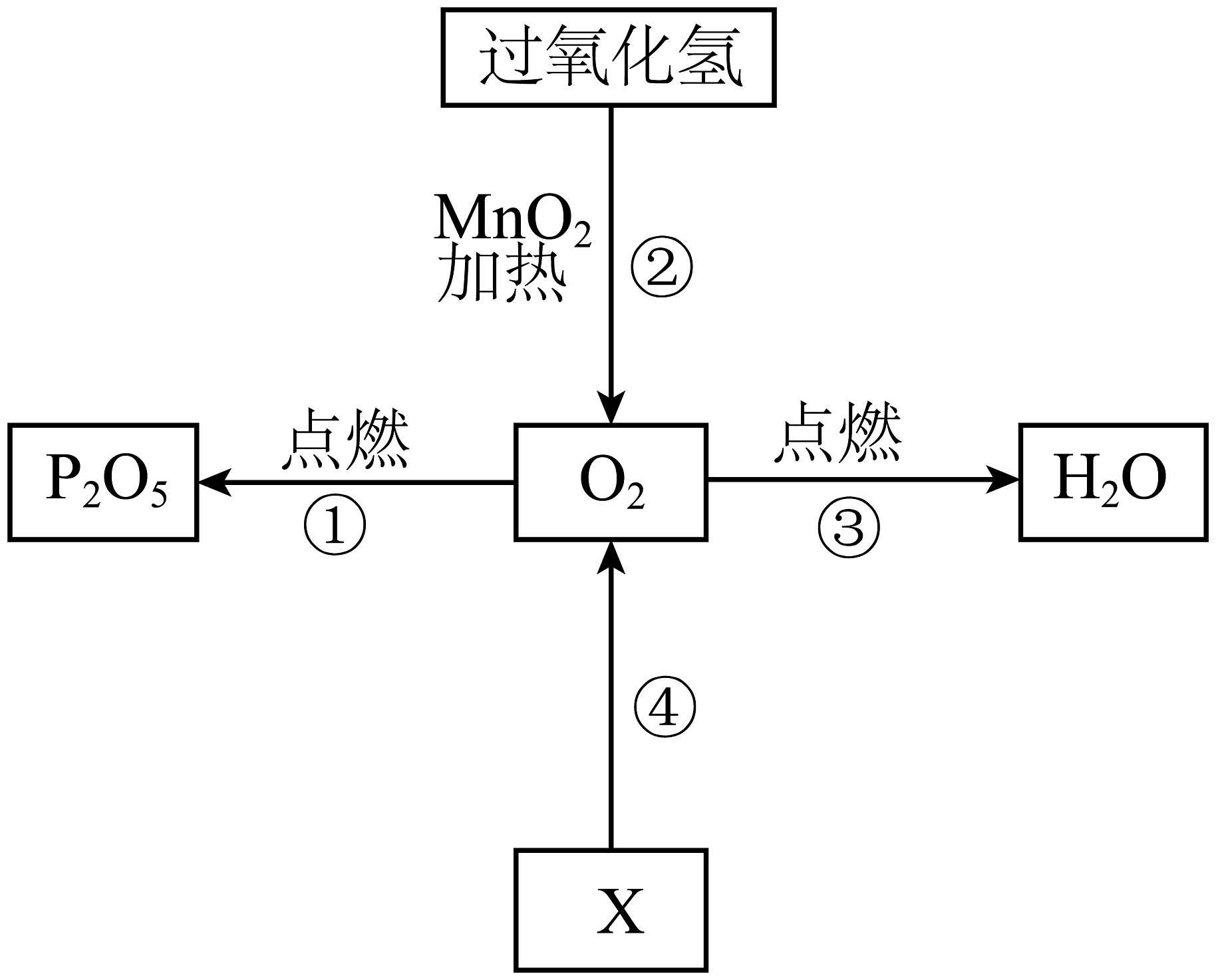 A、转化①:反应前后氧元素的化合价未发生改变 B、转化②:加入会使产生的质量增加 C、转化③:该反应的过程中氧元素的化合价升高 D、转化④:若该反应是分解反应,X中一定含有氧元素
A、转化①:反应前后氧元素的化合价未发生改变 B、转化②:加入会使产生的质量增加 C、转化③:该反应的过程中氧元素的化合价升高 D、转化④:若该反应是分解反应,X中一定含有氧元素 -
6、向密闭容器中加入一定质量的乙、丙、丁三种物质,在一定条件下发生化学反应,测得容器中甲、乙、丙、丁的质量随时间的变化如图所示。下列说法错误的是
 A、该反应中乙和丁是反应物,甲是生成物 B、a的值为12 C、丙可能是催化剂 D、该反应中,甲与乙的质量变化之比为4:1
A、该反应中乙和丁是反应物,甲是生成物 B、a的值为12 C、丙可能是催化剂 D、该反应中,甲与乙的质量变化之比为4:1 -
7、科技人员成功研制出一种新型催化剂,可将转化成液体燃料,反应的微观示意图如图所示。下列有关该反应的说法正确的是
 A、该反应遵守质量守恒定律 B、反应前后分子个数不变 C、参加反应的两物质的质量比为1:1 D、生成物的化学式为
A、该反应遵守质量守恒定律 B、反应前后分子个数不变 C、参加反应的两物质的质量比为1:1 D、生成物的化学式为 -
8、下列实验操作能达到实验目的的是
选项
实验目的
实验操作
A
检验自来水是否为硬水
取样,加入活性炭
B
验证质量守恒定律
称量镁燃烧前后的固体质量
C
探究蜡烛中是否含有氢元素
点燃蜡烛,在火焰上方罩一个蘸有澄清石灰水的烧杯
D
除去一瓶水中的难溶性杂质
过滤
A、A B、B C、C D、D -
9、下列说法正确的是A、反应前各物质的质量总和,一定等于反应后生成的各物质的质量总和 B、铁丝在氧气中燃烧后,生成物的质量比参加反应的铁丝的质量增加了 C、水的质量和受热变成水蒸气的质量相等,该变化符合质量守恒定律 D、酒精完全燃烧后,生成的水和二氧化碳的质量之和等于酒精减少的质量
-
10、氢气属于最清洁的燃料。氢气燃烧的化学方程式为 , 从中获得的信息错误的是A、氢气和氧气在点燃的条件下生成水 B、在点燃条件下,2份质量的氢气和1份质量的氧气反应生成2份质量的水 C、反应前后原子的数目不变 D、在点燃条件下,每2个氢分子和1个氧分子反应生成2个水分子
-
11、下列现象不能用质量守恒定律解释的是A、高锰酸钾受热分解后,固体质量减小 B、纸张燃烧后,灰烬的质量比纸张质量小 C、铜粉在空气中加热后,质量增大 D、水结冰后质量保持不变
-
12、现将12gA和12gB混合加热,A完全反应,反应后生成10gC和6gD,则参加反应的A与B的质量比是A、1:1 B、4:3 C、3:1 D、5:2
-
13、质量守恒定律是自然界基本定律之一,最早传播和用文字记载并使人们普遍接受质量守恒定律的科学家是A、拉瓦锡 B、门捷列夫 C、张青莲 D、屠呦呦
-
14、用来判断镁在氧气中燃烧是化学变化的依据的是A、放出大量的热 B、发出耀眼的白光 C、镁条变短 D、生成白色固体
-
15、实验是科学探究的重要途径,下面是测定空气中氧气含量的探究实验。
如图A、B两个实验均可用于空气中氧气含量的测定。用压力传感器测出B实验集气瓶中的气压变化,如图C所示。
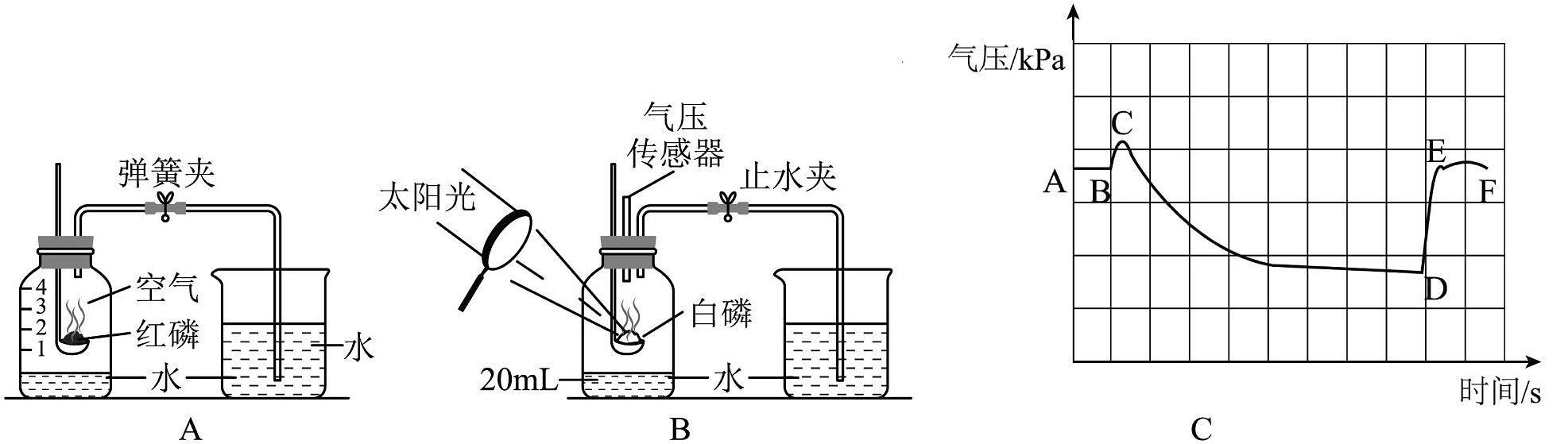 (1)、正确选择试剂是实验成功的关键,对图A实验中对试剂的选择合理的是______(填字母)。A、可以用铁代替红磷进行实验 B、红磷需要足量 C、只与氧气反应(2)、图A实验中,红磷燃烧的现象 , 此反应的文字表达式为。(3)、图B所示实验中,已知广口瓶的容积为220mL,冷却后打开止水夹,水从烧杯流入广口瓶中的体积为39mL,则空气中氧气的体积分数约为。(4)、实验中装置里气压变化如图C所示,CD段气压减小的主要原因是。
(1)、正确选择试剂是实验成功的关键,对图A实验中对试剂的选择合理的是______(填字母)。A、可以用铁代替红磷进行实验 B、红磷需要足量 C、只与氧气反应(2)、图A实验中,红磷燃烧的现象 , 此反应的文字表达式为。(3)、图B所示实验中,已知广口瓶的容积为220mL,冷却后打开止水夹,水从烧杯流入广口瓶中的体积为39mL,则空气中氧气的体积分数约为。(4)、实验中装置里气压变化如图C所示,CD段气压减小的主要原因是。 -
16、为探究氧气的化学性质进行如图实验:
 (1)、实验一瓶内放少量水是吸收二氧化硫,防止污染空气,由此推测二氧化硫的性质是。硫在氧气中燃烧的现象是发出 , 放热,生成有刺激性气味的气体,硫燃烧反应的属于(填基本反应类型)。(2)、实验二瓶内盛有少量水能否用少量细沙代替?答:。铁丝在氧气中剧烈燃烧反应的文字表达式为。(3)、实验三:把红热的木炭插入盛有氧气的集气瓶时,为什么要由瓶口向下缓慢插入?答:。
(1)、实验一瓶内放少量水是吸收二氧化硫,防止污染空气,由此推测二氧化硫的性质是。硫在氧气中燃烧的现象是发出 , 放热,生成有刺激性气味的气体,硫燃烧反应的属于(填基本反应类型)。(2)、实验二瓶内盛有少量水能否用少量细沙代替?答:。铁丝在氧气中剧烈燃烧反应的文字表达式为。(3)、实验三:把红热的木炭插入盛有氧气的集气瓶时,为什么要由瓶口向下缓慢插入?答:。 -
17、实验室现有下列仪器,回答相关问题:
 (1)、填仪器名称:a , c。(2)、实验室用高锰酸钾为原料制取氧气
(1)、填仪器名称:a , c。(2)、实验室用高锰酸钾为原料制取氧气①反应的文字表达为。
②组装发生装置时,除了上图所示的仪器外,还需要补充的仪器是。组装好发生装置后应该先再装入药品,然后在试管口内放一团棉花,以防止。
③选用c、d、e、g等四种仪器组成的装置收集氧气是因为氧气。用此装置收集气体时,如果产生气泡就立即收集,则收集到的气体(填“纯”或“不纯”)。
-
18、元素周期表是学习和研究化学的重要工具,根据如表回答有关问题。
族
周期
IA
0
1H
1.008
IIA
IIIA
IVA
VA
VIA
VIIA
2He
4.003
2
3Li
6.941
4Be
9.012
5B
10.81
6C
12.01
7N
14.01
8O
16.00
9F
19.00
10Ne
20.18
3
11Na
22.99
12Mg
24.31
13Al
26.98
14Si
28.09
15P
30.97
16S
32.06
17Cl
35.45
18Ar
39.95
(1)、第2周期第IA族元素符号是。在第2周期中属于稀有气体元素的是 , 该元素化学性质稳定的原因是。碳、氧元素最本质的区别是。(2)、硅原子的质子数为 , 它的相对原子质量是。(3)、如图是某原子结构示意图,它的最外层电子数是 , 在化学反应中该原子容易(填“得”或“失”)电子。 (4)、在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是______(填标号)。A、He和Ne B、C和Si C、Al和Mg D、O和Cl(5)、食盐的主要成分是氯化钠,其所含的阳离子是(写符号,下同),某带2个单位负电荷的阴离子与Ar的核外电子排布相同,该阴离子为。
(4)、在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是______(填标号)。A、He和Ne B、C和Si C、Al和Mg D、O和Cl(5)、食盐的主要成分是氯化钠,其所含的阳离子是(写符号,下同),某带2个单位负电荷的阴离子与Ar的核外电子排布相同,该阴离子为。 -
19、请阅读“科学史话——水的组成揭秘”,回答下列问题。
科学史话
水的组成揭秘
18世纪末,英国化学家普里斯特利(J。Priestley,1733—1804)把“易燃空气”和空气混合后盛在干燥、洁净的玻璃瓶中,当用电火花点火时,发出震耳的爆鸣声,且玻璃瓶内壁出现了液滴。
(1)、人们对水的组成的认识经历了相当长的时间。①普利斯特的研究中,“易燃空气”实际上是。
②请写出“易燃空气”与空气混合后点火所发生的反应的文字表达式:。
(2)、在电解水实验中,与正、负两极相连的玻璃管上方产生的气体体积比为。(3)、电解水的文字表达式为 , 在此反应中发生变化的微粒是(填“氧原子”、“氢原子”或“水分子”)。(4)、在水的净化实验中,过滤可以去除水中的(“可溶性”或“不溶性”)杂质,实验室过滤时要用到的玻璃仪器:漏斗、玻璃棒和 , 其中玻璃棒的作用是。(5)、生活中节约用水的方法有(写一条即可)。 -
20、如图所示的是课本中的一些实验,回答问题。
 (1)、图1实验,从微观角度,水的沸腾过程从液态水变成气态水,水分子之间的距离将(填“变大”或“变小”)。(2)、图2说明石蜡在约60℃的热水中熔化,所表现出来的性质属于(填“物理”或“化学”)性质。(3)、图3实验:硫酸铜溶液呈色,滴入氢氧化钠溶液后可观察到的现象是 , 加热上述反应后生成的物质,又可观察到的现象是。(4)、图4实验:观察到澄清石灰水变浑浊,说明大理石与稀盐酸反应生成的物质有。
(1)、图1实验,从微观角度,水的沸腾过程从液态水变成气态水,水分子之间的距离将(填“变大”或“变小”)。(2)、图2说明石蜡在约60℃的热水中熔化,所表现出来的性质属于(填“物理”或“化学”)性质。(3)、图3实验:硫酸铜溶液呈色,滴入氢氧化钠溶液后可观察到的现象是 , 加热上述反应后生成的物质,又可观察到的现象是。(4)、图4实验:观察到澄清石灰水变浑浊,说明大理石与稀盐酸反应生成的物质有。