相关试卷
-
1、为比较相同浓度的 FeCl3 溶液和CuSO4溶液对 H2O2分解的催化效果,某研究小组进行了如下探究:
 (1)、请写出 H2O2分解的化学方程式.(2)、【定性研究】
(1)、请写出 H2O2分解的化学方程式.(2)、【定性研究】如图甲,可通过观察来定性比较两者的催化效果.
(3)、【定量研究】如图乙,实验前检查该装置气密性的方法是.要定量比较两者的催化效果,可测量生成等体积气体所需的.
(4)、【深入研究】在FeCl3溶液中,究竟是哪种粒子起催化作用呢?
猜想1:铁离子(Fe3+)起催化作用;
猜想2:起催化作用;
猜想3:起催化作用;
……
请设计实验,验证猜想1.
实验操作
实验现象及结论
-
2、(1)某化学活动小组在一次实验中进行了如图所示实验:此时观察到的实验现象是____;实验后,小组同学充分振荡 U形玻璃管,将U 形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动.
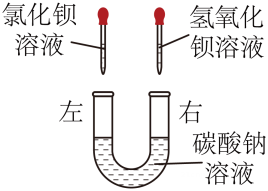 (1)、【提出问题】滤液中除 Na+外,还含有什么离子?
(1)、【提出问题】滤液中除 Na+外,还含有什么离子?【猜想与假设】A同学:含有OH-、Cl-、CO2-;B同学:含有OH-、Cl-、Ba2+ ;C同学:含有(填离子符号).
(2)、【实验探究】B同学为了验证自己的猜想,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象.由此B同学得出结论:自己的猜想不成立,A同学的猜想成立.【评论与交流】请你评价 B同学的结论:;同学们经过讨论后一致认为:B同学在验证自己的猜想时,若将所加试剂换成足量的另一种试剂(填化学式),则既能验证自己的猜想,也能确定滤液中的离子成分.
C同学用该试剂进行实验,最终确定了滤液中的离子成分.
(3)、【归纳与总结】通过上述实验我们能够总结出,在确定化学反应后所得溶液中的离子成分时,一般应加入 , 验证就可以确定溶液中的离子成分.
-
3、小明同学对研究物质的酸碱性产生了浓厚的兴趣,他使用pH试纸测得家中某些物质近似的pH,如下表:
物质
洁厕灵
苹果汁
护发素
玉米粥
洗发水
肥皂液
厨房清洁剂
pH
1
3
6
7~8
8
10
12
小明将自制的紫菜薹(tái)汁滴入上述7 种物质中,发现紫菜薹汁与紫色石蕊试液的变化相似,将紫菜薹汁滴入肥皂液中,液体变成绿色.
(1)、若将紫菜薹汁滴入护发素中,你认为液体的颜色(填“不变”“变红色”或“变绿色”).(2)、通过研究,小明同学懂得了洗发时先用洗发水再用护发素的科学道理.查阅资料:人体胃液pH在0.5~1.5之间,小明同学懂得了患胃酸过多的病人不能空腹食用上述食物中的.(3)、要洗去学校餐厅地面上的油垢,小明同学准备选择从家中带a“洁厕灵”、b“厨房清洁剂”两种物质中的(填“a”或“b”). -
4、类比法是化学中研究物质的重要方法之一.草酸的化学性质与碳酸相似.已知碳酸易分解,草酸在受热条件下也分解,仅生成三种氧化物.某校研究性学习小组对此展开探究:(1)、小明首先根据草酸中含有元素,可推测生成物中含有水.(2)、小明对分解生成的其他产物进行猜测、验证:
【假设一】生成物中有二氧化碳
实验一:将生成的气体通入澄清的石灰水,实验现象是 , 小明据此判断生成物中含有二氧化碳.
【假设二】生成物中有一氧化碳
实验二:小明用如图所示装置进行实验,从而证明生成物中含有一氧化碳.

请回答:A装置中黑色固体粉末是(填化学式),A装置中的实验现象是。
(3)、讨论交流:小芳认为,小明的“实验二”不需要 B装置也能够推断出生成物中含有一氧化碳,你是否支持小芳的观点:(填“支持”或“不支持”),请说出你的理由:
小芳认为,从环保的角度看,“实验二”装置有一个缺陷,请你指出该缺陷: , 处理的方法是.
-
5、做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
(1)、【作出猜想】甲同学认为溶液中的溶质只有 Na2SO4一种物质.乙同学认为溶液中的溶质是 Na2SO4 和两种物质.
(2)、丙同学认为溶液中的溶质是 Na2SO4 和 NaOH 两种物质.【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH 溶液反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
实验操作
实验现象
实验结论
乙同学实验
取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管溶液中
铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色
猜想(2)成立
丙同学实验
取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞
溶液变色
猜想(3)成立
(3)、【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.(4)、【知识拓展】生活中能否用铝制品来盛放强碱性溶液?(填“能”或“不能”).乙同学的实验中铝片与溶液发生了反应,请写出铝与该溶液发生反应的化学方程式:.
-
6、小杨往 NaOH 溶液中滴加稀硫酸,溶液无明显变化,他和小组同学以“酸与碱能否发生反应”为课题进行了科学探究,请回答下列问题.
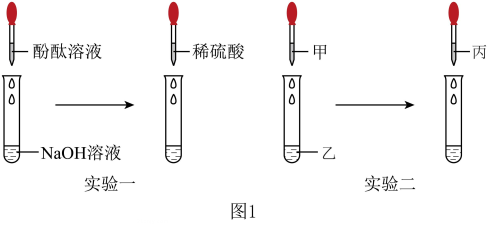
【实验一】
(1)、向NaOH溶液中先滴入几滴酚酞溶液,振荡,再滴入稀硫酸,观察到溶液由色变为无色,该反应的化学方程式为.(2)、继续往上述试管逐滴滴入 NaOH溶液,不断振荡,如果观察到现象,则证明滴加的稀硫酸过量.(3)、【实验二】按照“证明反应后 NaOH 消失了”这个角度,同学们又设计了实验二,利用NaOH 溶液、CuSO4溶液、稀盐酸同样证明了酸和碱能发生反应,其中试剂丙是.
(4)、【拓展延伸】CO2通入 NaOH 溶液中也无明显现象,CO2与NaOH溶液能否发生化学反应呢?小组同学对此继续探究.【查阅资料】常温下 NaOH、Na2CO3在水、乙醇中的溶解性如下表所示:
溶质
溶解性
溶剂
氢氧化钠
碳酸钠
水
极易溶
易溶
乙醇
易溶
微溶
【实验三】
小组同学设计了多角度验证CO2与NaOH溶液反应的实验,如图2所示(装置已连接好,气密性良好,止水夹a和b已关闭,部分仪器已略去).
【温馨提示】CO2与乙醇不反应,本实验条件下CO2在乙醇中的溶解忽略不计.
把注射器Ⅰ中氢氧化钠的乙醇溶液注入充满CO2的三口烧瓶中,轻轻振荡,观察到的现象是 , 写出该反应的化学方程式:
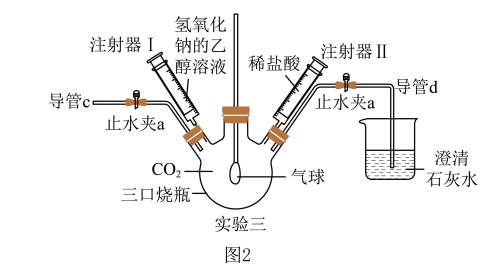 (5)、把导管d移出石灰水,打开止水夹 a、b,再从导管c端往三口烧瓶中鼓入N2 , 目的是 , 过了一段时间后,先把导管d放入澄清石灰水中,接着关闭止水夹a,再把注射器Ⅱ中的稀盐酸注入三口烧瓶内,观察到三口烧瓶中产生气泡,烧杯中的澄清石灰水变浑浊.此实验从角度证明了 CO2与NaOH溶液发生了反应.
(5)、把导管d移出石灰水,打开止水夹 a、b,再从导管c端往三口烧瓶中鼓入N2 , 目的是 , 过了一段时间后,先把导管d放入澄清石灰水中,接着关闭止水夹a,再把注射器Ⅱ中的稀盐酸注入三口烧瓶内,观察到三口烧瓶中产生气泡,烧杯中的澄清石灰水变浑浊.此实验从角度证明了 CO2与NaOH溶液发生了反应. -
7、某化学兴趣小组对酸、碱、盐的部分性质进行探究.
【探究一】氢氧化钠与二氧化碳反应
甲同学设计实验方案如图1所示:
 (1)、实验现象为 , 甲同学由此判断氢氧化钠和二氧化碳发生了反应.(2)、小组内其他同学认为甲同学方案不完善,理由是.(3)、【探究二】氢氧化钠和盐酸发生中和反应时放出热量
(1)、实验现象为 , 甲同学由此判断氢氧化钠和二氧化碳发生了反应.(2)、小组内其他同学认为甲同学方案不完善,理由是.(3)、【探究二】氢氧化钠和盐酸发生中和反应时放出热量乙同学向一定量10%的氢氧化钠溶液中滴加10%的盐酸,滴加过程中温度变化如表所示:
加入盐酸体积V/mL
2
4
6
8
10
12
14
16
18
20
混合溶液温度 T/℃
15.2|
19.6|
22.0
26.0
28.2|
26.7
25.7|
24.7
23.7
22.9
反应的化学方程式为.
(4)、根据表中数据分析混合溶液温度变化的原因是.(5)、小组内其他同学提出“将10%的盐酸直接滴入氢氧化钠固体中也能得出相同结论”,你认为是否合理?说明理由: .(6)、丙同学将甲同学和乙同学实验后的溶液混合,未发现明显现象.现将混合液中的氯化钠进行提纯,具体的操作为.(7)、【探究三】碳酸钠溶液与稀盐酸的分步反应
【查阅资料】向碳酸钠溶液中逐滴加入稀盐酸的反应是分步反应,第一步反应生成碳酸氢钠和氯化钠,当碳酸钠反应完后才发生第二步反应.
丁同学向106g质量分数为10%的碳酸钠溶液中逐滴加入质量分数为3.65%的稀盐酸,生成二氧化碳的质量变化如图2所示(不考虑CO2的溶解).
A→C 段发生反应的化学方程式为.
(8)、若B 点横坐标为150,则其纵坐标为. -
8、探究中和反应是否发生的方法有多种.小华同学进行了以下四个实验,并用图像分别描述了实验过程中的现象.其中,依据图所示现象不能判断中和反应一定发生的是( ).
 A、在稀盐酸中加入氯化铜,然后向其中逐滴加入 NaOH 溶液 B、在 NaOH溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸 C、在 NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸 D、在 NaOH溶液中加入 Ba(NO3)2 , 然后向其中逐滴加入稀硫酸
A、在稀盐酸中加入氯化铜,然后向其中逐滴加入 NaOH 溶液 B、在 NaOH溶液中加入CaCO3 , 然后向其中逐滴加入稀盐酸 C、在 NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸 D、在 NaOH溶液中加入 Ba(NO3)2 , 然后向其中逐滴加入稀硫酸 -
9、某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”.
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL 10%的盐酸(密度为1.05g/mL).
实验步骤:
(1)、计算:需要37%的浓盐酸的体积为mL(精确到0.01mL,下同);需要蒸馏水的体积为mL(水的密度为1.0g/mL).(2)、量取浓盐酸和蒸馏水.混合配制.
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
加入盐酸的体积(V)/mL
0
2
4
6
8
10
12
14
16
18
20
溶液温度变化(△t)/℃
△t1
5.2
9.6
12.0
16.0
18.2
16.7
15.7
14.7
13.7
12.9

表中△t1的值为.
(3)、试绘出溶液温度变化与加入盐酸体积之间的关系图.(4)、根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是.(5)、其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素).①横坐标及猜想理由:;
②纵坐标及猜想理由:.
-
10、某校同学开展了如下“溶液酸碱性的检验”的实验活动:
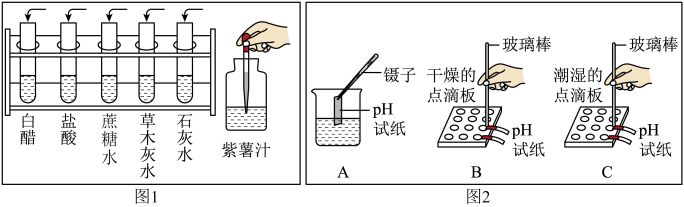 (1)、把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
(1)、把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:溶液
白醋
盐酸
蔗糖水
草木灰水
石灰水
加入紫薯汁后的颜色
红色
红色
紫色
绿色
绿色
①图1中存放紫薯汁的仪器名称是;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是.
(2)、用pH试纸测定图1中部分溶液的酸碱度:草木灰水 pH>7,属于(填“酸性”“中性”或“碱性”)溶液,白醋pH(填“>”“<”或“=”)7.(3)、图2是三位同学分别测定土壤酸碱度的实验操作示意图,其中正确的是(填“A”“B”或“C”,下同),可能导致被测溶液pH数值发生改变的错误操作是. -
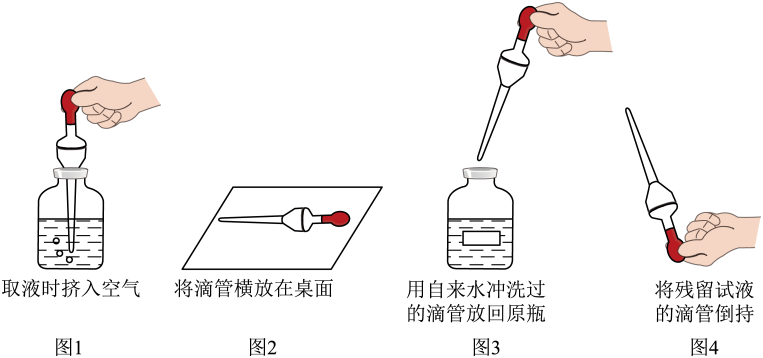
11、苏州市初中化学实验操作考查内容为“溶液酸碱性的检验”.请根据实验回答下列问题.(1)、测得碳酸饮料的pH7(填“<”“=”或“>”).(2)、下列使用pH试纸的方法中,正确的是____(填序号).A、将pH 试纸剪成几段使用 B、将pH试纸直接插入待测液中 C、将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在 pH试纸上 D、将pH试纸润湿后放在表面皿上,用干净的玻璃棒蘸取待测液滴在 pH 试纸上 E、读数时,在30秒内将 pH试纸呈现的颜色与标准比色卡对照(3)、本次实验中滴管使用出现了如图1~图4所示的四种常见错误操作.请你从这四幅图中任意选择一幅(请写明所选图的序号),具体说明改正错误的方法.
 (4)、使用白色点滴板完成实验有显色明显、便于对比、(填一项)等优点.
(4)、使用白色点滴板完成实验有显色明显、便于对比、(填一项)等优点. -
12、构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
 (1)、如用湿润的 pH 试纸测定盐酸的 pH,则结果会(填“偏大”“偏小”或“无影响”).(2)、图中①的现象是:.(3)、写出一个符合图中③的化学方程式.(4)、图中性质④属于反应(填基本反应类型).(5)、图中⑤的性质在工业上可用于(填用途).
(1)、如用湿润的 pH 试纸测定盐酸的 pH,则结果会(填“偏大”“偏小”或“无影响”).(2)、图中①的现象是:.(3)、写出一个符合图中③的化学方程式.(4)、图中性质④属于反应(填基本反应类型).(5)、图中⑤的性质在工业上可用于(填用途). -
13、请完成以下实验报告的填写.
实验名称:酸碱的中和反应
实验目的:验证盐酸和氢氧化钠能否发生反应.
供选择的仪器和药品:试管、胶头滴管、烧杯、酚酞溶液、稀盐酸、氢氧化钠稀溶液.
实验步骤
实验现象
实验结论、解释
(1)在中加入约1mL 氢氧化钠稀溶液,用胶头滴管滴入几滴酚酞溶液
溶液显色
碱能使酚酞溶液变色
(2)然后, , 直至溶液恰好变无色为止
溶液颜色最后褪去
两者能发生反应,反应的化学方程式是
-
14、下图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸中和反应的实验.

(说明:图中 A1、A2、A3、B1、B2、B3均为溶液编号)
根据上图实验,请你与甲、乙同学一起完成下列探究:
探究环节
甲同学的探究
乙同学的探究
提出问题
A3 溶液为什么不变红?
B3 溶液中溶质成分是什么?(酚酞不计)
作出猜想
实验过程中,酚酞变质了
猜想一:NaCl;猜想二:NaCl、HCl
(1)、实验验证取少量 A3 溶液于另一试管中,向其中滴加 NaOH溶液,溶液变红,说明甲同学的猜想(填“成立”或“不成立”)
(2)、你认为,在常温下 A2 溶液测出的 pH应(填“>”“=”或“<”)7(3)、取少量 B3 溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体 逐 渐 减 少,溶液 由 无 色 变为.据此,你认为乙同学的猜想(填“一”或“二”)成立(4)、交流反思甲、乙同学的实验中,反应均涉及的化学方程式是
(5)、A3 溶液未变红,你认为原因是 A2 溶液中较多,加入的 NaOH 溶液未将其完全中和甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制 -
15、下图为三种不同浓度的氢氧化钠溶液与对应浓度的盐酸反应的曲线.

下列说法正确的是( ).
A、在a、b、c三种曲线所示的实验中,所用盐酸浓度越大,V点对应溶液的pH越大 B、在a曲线所示的实验中,若用酚酞做指示剂,酚酞溶液由红色变为无色 C、在a、b、c三种曲线所示的实验中,反应速率相同 D、在a、b、c三种曲线所示的实验中,溶液酸性由强到弱的顺序是a>b>c -
16、同样是清洁剂,炉具清洁剂有强碱性,而厕所清洁剂有强酸性,用这两种清洁剂进行实验得到的结果一定有误的是( ).A、测得炉具清洁剂pH=13 B、测得厕所清洁剂 pH=8 C、炉具清洁剂使无色酚酞溶液变红 D、厕所清洁剂使紫色石蕊溶液变红
-
17、图中图像与所对应操作相符的是( ).
 A、图甲是对氢氧化钠溶液加水稀释 B、图乙是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合 C、图丙是向 HCl与 Na2SO4混合溶液中加入 Ba(OH)2溶液 D、图丁是用等质量、等浓度的双氧水分别制取氧气
A、图甲是对氢氧化钠溶液加水稀释 B、图乙是将镁片和铁片(均足量)分别和等质量、等溶质质量分数的稀硫酸混合 C、图丙是向 HCl与 Na2SO4混合溶液中加入 Ba(OH)2溶液 D、图丁是用等质量、等浓度的双氧水分别制取氧气 -
18、实验室发现一瓶标签脱落的固体试剂,小王分别取少量的该固体进行了下列实验.根据实验现象,该固体最可能是( ).
实验步骤
实验现象
检测水中加入固体前后液体的pH
固体不溶解,液体的pH几乎没变化
检测盐酸中加入固体前后溶液的pH
固体溶解,无气体放出,溶液 pH 增大
固体灼热状态下,通入纯净CO
固体质量减轻,尾气中只检测到 CO与 CO2
A、金属单质 B、碱 C、盐 D、金属氧化物 -
19、向滴有酚酞的盐酸溶液中逐滴加入氢氧化钠溶液,所得溶液的pH与加入溶液的体积关系如右图所示.下列说法正确的是( ).
 A、反应过程中溶液温度降低 B、A 点对应溶液的溶质为 HCl、NaCl C、恰好完全反应时溶液显中性 D、反应过程中溶液的颜色由红色变为无色
A、反应过程中溶液温度降低 B、A 点对应溶液的溶质为 HCl、NaCl C、恰好完全反应时溶液显中性 D、反应过程中溶液的颜色由红色变为无色 -
20、下列说法中正确的是( ).A、有盐和水生成的反应一定是中和反应 B、碱一定能使酚酞溶液变红色 C、溶液稀释前后溶质的质量一定相等 D、在原子中原子核内的质子数一定等于中子数