相关试卷
-
1、2025年5月12日是第17个全国防灾减灾日,主题是“人人讲安全,个个会应急—排查身边灾害隐患”。下列做法正确的是( )A、电动自行车在居民楼内充电 B、夜间煤气泄漏开灯检查 C、在加油站内拨打电话 D、楼房起火时,用湿毛巾捂住口鼻,贴近地面逃离
-
2、人类生活离不开氧气。
I探究人体呼吸作用
下表为某同学测量的呼吸前后部分气体组成的实验数据(通常状况)。
物质
吸入空气(体积分数/%)
呼出气体(体积分数/%)
N2
78
75
O2
21
16
CO2
0.039
4
(1)、人体呼吸时消耗O2产生CO2 , 该过程能量(填“吸收”或“释放”)。(2)、氮气在呼吸前后体积几乎不变。实验中呼出气体的总体积吸入空气的总体积(填“>”“=”或“く”)。(3)、ⅡI探究呼吸自救器的工作原理一种面罩式呼吸自救器中的制氧药剂主要含NaClO3、MnO2(催化剂)和铝粉。
NaClO3制氧原理:2NaClO32NaCl+3O2↑。213gNaClO。按上式完全分解,计算理论能生成O2的质量。
(4)、制氧药剂中铝粉的作用是燃烧提供NaClO3分解所需的热量。控制制氧药剂中物质的质量比m(NaClO3):m(MnO2)为22:1,进行实验,得到O2的质量如下。实验编号
m(制氧药剂)/g
m(NaClO3+MnO2)/g
m(铝粉)/g
m(O2)/g
1
100
99
1
20.6
2
100
98
2
28.4
3
100
97
3
38.6
4
100
96
4
37.3
①上述实验的目的是探究对得到氧气质量的影响。
②实验1(或实验2)中得到0质量明显小于实验3的主要原因是
③实验4中得到O2质量小于实验3的原因是。
 (5)、某种呼吸自救器的结构如题26图,可在有毒危险空间提供约2小时左右呼吸用氧气。区城A填充的是NaOH和 CaO。
(5)、某种呼吸自救器的结构如题26图,可在有毒危险空间提供约2小时左右呼吸用氧气。区城A填充的是NaOH和 CaO。①写出NaOH发生反应的化学方程式:。
②若将呼出气体通过单向阀(控制气体单向流动)直接排出呼吸面罩,可省去区域A,简化呼吸自救器的设计。实际不采用此种设计三的理由主要是。
-
3、古籍是文明的载体。古籍纸张酸化会造成纸张发黄断裂,需进行处理。
注:pH为6.5~8.5是纸张保存的最佳条件。
(1)、纸张成分及酸化原因。①纸张的主要成分为纤维素[(C6H12O5)n]。纤维素属于(填字母)。
A.无机化合物
B.有机高分子化合物
②纸张酸化原因之一是空气中微量SO2与纸张中的水分反应,完成化学方程式:
2SO2++2H2O——2H2SO4。经过漫长岁月,酸逐渐增多导致纸张酸化。
(2)、古法造纸时常用熟石灰和草木灰(主要成分K2CO3)混合使用处理原料,两者混用碱性会增强,其原因是(用化学方程式表示)。(3)、古籍纸张若出现明显酸化(以硫酸为例),需进行脱酸保护。一步脱酸法:酸化纸张用饱和石灰水浸泡,石灰水渗人纸张内部快速脱酸。
两步脱酸法:酸化纸张先用饱和石灰水浸泡,取出再用Ca(HCO3)2溶液浸泡,发生反
应:Ca(OH)2+Ca(HCO3)2=2CaCO3↓+2H2O
注:室温时,饱和石灰水pH约为12.6。
①石灰水脱硫酸的原理为(用化学方程式表示)。
②一步脱酸法处理后的湿纸张pH约为12,晾干后pH降至8左右。过程中pH下降的主要原因是。
③无论是一步脱酸法还是两步脱酸法,处理后的纸张均具有一定的抗酸性(消耗酸的能力),除微量碱残留外,具有抗酸性的原因为。
-
4、阅读下列材料,回答相关问题。
氢气是一种清洁、高效能源。氢能产业链分制氢、储氢、用氢等环节。由风能、太阳能等可再生能源发电,再电解水制得的氢气为“绿氢”。由化石燃料制得的氢气为“灰氢”,其成本相对低廉.但会排放大量CO2。化石燃料制氢气时若将排放的CO2进行捕集、封存等,减少碳排放,此时制得的氢气为“蓝氢”。甲烷一水蒸气重整制氢流程如下:

化学储氢是利用物质与H2反应生成储氢材料如氨(NH3)、水合肼(N2H4▪H2O)等,再通过改变条件使储氢材料转化为H2。氨和水合肼转化为H2的过程分别如下
常以质量儲氫密度来衡量化学储氢技术的优劣。如氨气的理论质量储氢密度为17.6%,是一种较好的储氢材料。
(1)、实验室模拟电解水制氢,装置如图。
①过程中的能量转化形式:太阳能→→化学能。该方法制得氢气的种类为(填字母)。A.绿氢
B.灰氢
C. 藍氫
②经检验b管产生H2 , 由此得出关于水的组成的推论是
(2)、甲烷一水蒸气重整制氢。①转化Ⅰ理论生成CO和H2的分子个数比为。
②写出转化Ⅱ发生反应的化学方程式 :。
(3)、氨释放H2的微观示意图如下。请在B对应框中将除氢分子外的微观粒子补充完整。 (4)、①储氢材料N2H4·H2O的质量储氢密度的理论值为。
(4)、①储氢材料N2H4·H2O的质量储氢密度的理论值为。②50℃时,N2H4·H2O的实际质量储氢密度小于理论值。原因是N2H4实际发生分解反应产生的气体中含有NH3 , 写出该反应的化学方程式:。
-
5、以闪锌矿[主要成分ZnS,少量FeS、CdS(硫化镉)]为原料制备硫酸锌的流程如下:
 (1)、“焙烧”时,金属硫化物(ZnS、FeS和CdS)与氧气反应均转化为金属氧化物和SO2写出ZnS与O2高温反应的化学方程式:。(2)、①“酸浸”时发生反应的基本类型为。
(1)、“焙烧”时,金属硫化物(ZnS、FeS和CdS)与氧气反应均转化为金属氧化物和SO2写出ZnS与O2高温反应的化学方程式:。(2)、①“酸浸”时发生反应的基本类型为。②“酸浸”所得滤液中阳离子有Cd2+、Fe2+、Fe3+和(填离子符号)。
(3)、“除铁”时发生反应;反应I:4FeSO4+O2+4H2O2Fe2O3↓+4H2SO4反应II:Fe(SO4)3+3H2OFe2O3↓+3H2SO4
①除铁所得“滤渣2”的用途有(写一种)。
②铁元素化合价在反应I和反应II前后的变化情况分别为(填字母)。
A.升高降低
B.升高不变
C.不变降低
D.降低升高
(4)、“除镉过滤”前需先测定溶液中CdSO4浓度,计算所需锌粉质量的理论值[m理论(Zn)]。图所示的是实际参加反应锌的质量与理论值之比分别为1.2和1.0时,除镉率随时间的变化。

①金属活动性:ZnCd(填“>”或“<”)。
②除镉率接近 100%时,>1 的原因是。
-
6、某同学在实验室制取CO2并进行研究。
 (1)、该同学拟用块状石灰石制CO2。
(1)、该同学拟用块状石灰石制CO2。①应选用的另一种试剂是(填名称)。
②用图1所示仪器组装一套可以随时添加液体试剂的发生装置,需要用到的仪器有(填字母)。
(2)、如图2所示,进行验证CO2能与水反应生成酸性物质的实验。①试管中的物质X为。
②通人CO2后可观察到的现象为
(3)、下列反应均能生成CO2。A. 木炭燃烧
B.碳酸钠与稀硫酸反应
C.石灰石高温分解
D.CO与氧化铁高温下反应
①其中最适合用于实验室制取CO2的是(填字母)。
②你选择的反应适合用于实验室制取CO2的主要理由是(写两条)。
(4)、收集CO2时,常用燃着的木条放在集气瓶口验满。木条熄灭,CO2真的集满了吗?如图3,向三颈烧瓶中持续通CO2 , 测定瓶内氧气体积分数的变化情况,并用燃着的木条置于瓶口观察其是否熄灭,结果如图4所示。
①图3中,通CO2导管的末端应处于(填“A”或“B”)位置。
②图4所示C点处燃着的木条熄灭,此时三颈烧瓶内CO2的体积分数约为
-
7、《国务院关于实施健康中国行动的意见》中提出要提高全民健康水平。(1)、中国居民平衡膳食餐盘(如图1)描述一个人一餐中膳食的组成和大致比例。
①“膳食餐盘”所示的食物中富含蛋白质的是(填字母)。
②若需补充维生素C,建议多吃“膳食餐盘”中的(双选,填字母)。
 (2)、洗鼻液有助于修复鼻粘膜。配制方法:向如图2所示洗鼻器中加入4.5gNaCl,加少量水振荡,继续加水至洗鼻器的500mL刻度处·摇匀。
(2)、洗鼻液有助于修复鼻粘膜。配制方法:向如图2所示洗鼻器中加入4.5gNaCl,加少量水振荡,继续加水至洗鼻器的500mL刻度处·摇匀。①该洗鼻液的溶质为。
②所得溶液密度约为1g·mL-,该溶液的溶质质量分数为。
(3)、某市售家用净水器(如图3所示)可将自来水净化为直饮水。①自来水通过不锈钢滤网层相当于实验室中的操作(填操作名称)。
②图中主要用于吸附杂质、除去臭味的物质是。
(4)、H2具有一定的抗细胞氧化作用。用氢棒(有效成分Mg)制备富氢水(溶有H2的水)的反应为Mg+2H2O—Mg(OH)2+H2↑。室温时Mg(OH)≥溶解度:1.24X10-2g。①富氢水(氢棒已取出)散口放置,水中H浓度下降的原因是(从微观角度解释)。
②氢棒使用一段时间后产生H2的能力下降,将氢棒用白醋(含醋酸)浸泡即可恢复其在水中产生H2的能力,原因是。
-
8、为验证活性炭或食盐能加快铁粉生锈速率,进行实验。下表是2g铁粉、5g水与不同质量活性炭、食盐均匀混合后,在10分钟内温度上升的实验记录。
实验编号
活性炭质量/g
食盐质量/g
温度上升值/℃
1
0
0
0.1
2
0.2
0
22.0
3
x
0.1
3.1
4
0.2
0.1
56.3
下列说法正确的是( )
A、铁的锈蚀不需要氧气参与 B、表中x的值为0.2 C、欲得出结论“活性炭能加快铁粉生锈速率”可以对比实验1和2 D、对比实验1和4得出的结论是“食盐能加快铁粉生锈速率” -
9、下列实验方案不能达到相应实验目的的是( )
选项
实验目的
实验方案
A
干燥 H2
将气体通过盛有浓硫酸的洗气瓶
B
鉴别稀硫酸和氯化钠溶液
取样,分别滴加酚酞溶液,观察颜色
C
比较纯铜片与黄铜片的硬度
将两者相互刻画,观察划痕
D
探究NH4NO3固体溶解过程的能量变化
将NH4NO3固体加入水中,搅拌,测量过程中温度的变化
A、A B、B C、C D、D -
10、工业制备的重铬酸钾(K2Cr2O7)中常混有少量KCl,两种物质的溶解度曲线如图所示。下列说法正确的是( )
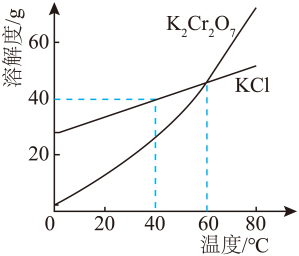 A、K2Cr2O7的溶解度一定比KCl的大 B、40℃时,将50gKCl加入100g水中,所得溶液质量为150 g C、60℃时,两种物质的饱和溶液的溶质质量分数相等 D、采用蒸发结晶的方法可除去K2Cr2O7中混有的少量KCl
A、K2Cr2O7的溶解度一定比KCl的大 B、40℃时,将50gKCl加入100g水中,所得溶液质量为150 g C、60℃时,两种物质的饱和溶液的溶质质量分数相等 D、采用蒸发结晶的方法可除去K2Cr2O7中混有的少量KCl -
11、白炽灯泡的结构如图,通电后钨丝在高温下发光。生产时灯泡内可能会混人少量氧气。
下列说法正确的是( )
 A、钨丝的熔点低 B、两侧的金属丝不导电 C、灯泡内填充氮气是因为其化学性质活泼 D、白炽灯工作时,红磷能消耗残留氧气
A、钨丝的熔点低 B、两侧的金属丝不导电 C、灯泡内填充氮气是因为其化学性质活泼 D、白炽灯工作时,红磷能消耗残留氧气 -
12、下列实践项目与相应物质性质没有直接关联的是( )
选项
实践项目
物质性质
A
用75℅医用酒精消毒
酒精易挥发
B
使用炉具清洁剂(含NaOH)时戴乳胶手套
NaOH具有腐蚀性
C
用铁板和硫酸铜溶液制作金属蚀刻画
铁能与硫酸铜发生反应
D
用柠檬酸与小苏打自制汽水
柠檬酸能与小苏打反应生成 CO2
A、A B、B C、C D、D -
13、用如图所示装置模拟粉尘爆炸实验,吹人空气后发生爆炸,硬纸板被掀起。下列说法不正确的是( )
 A、面粉属于可燃物 B、吹人空气前,面粉没有燃烧是因为塑料瓶内没有氧气 C、吹人空气,面粉剧烈燃烧大量放热,气体体积迅速膨胀 D、面粉加工厂应严禁烟火
A、面粉属于可燃物 B、吹人空气前,面粉没有燃烧是因为塑料瓶内没有氧气 C、吹人空气,面粉剧烈燃烧大量放热,气体体积迅速膨胀 D、面粉加工厂应严禁烟火 -
14、下列有关铁丝在氧气中燃烧反应的叙述不正确的是( )A、放出热量 B、生成 Fe3O4 C、反应前后固体质量相等 D、参加反应的铁与生成物中铁元素质量相等
-
15、阅读下列材料,回答问题:过氧化氢(H2O2)在二氧化锰催化下分解产生氧气,该原理可用于实验室制氧气。氧气化学性质活泼,能与许多物质反应,如铁丝在氧气中燃烧.火星四射,生成黑色固体。(1)、下列关于过氧化氢的说法正确的是( )A、过氧化氢分子中含有氧分子 B、过氧化氢分子中氢、氧原子个数比为1:1 C、过氧化氢中氢、氧元素的质量比为1:8 D、34g过氧化氢完全分解可生成32 g氧气(2)、实验室用30mL8%的过氧化氢溶液和二氧化锰制氧气,并进行铁丝燃烧实验。下列实验操作不规范的是( )A、检查气密性
 B、取用液体
B、取用液体 C、收集氧气
C、收集氧气 D、铁丝燃烧
D、铁丝燃烧
-
16、自然界能减少大气中CO2。含量的途径是( )A、火山喷发 B、森林着火 C、光合作用 D、碳酸分解
-
17、钇是稀土元素的一种,其在元素周期表中的部分信息如图。下列说法不正确的是( )
 A、钇的元素符号为Y B、钇原子的核外电子数为39 C、钇原子的质子数为39 D、忆元素的相对原子质量为88.91 g
A、钇的元素符号为Y B、钇原子的核外电子数为39 C、钇原子的质子数为39 D、忆元素的相对原子质量为88.91 g -
18、人体中含量(以质量分数计)在0.01%以下的元素称为微量元素。部分元素及其在人体中的含量如下表,其中属于微量元素的是( )
元素
O
Ca
K
Fe
含量
65%
1.5%
0.4%
约0.004%
A、O B、Ca C、K D、Fe -
19、粗盐的初步提纯包含溶解、过滤、蒸发等操作,一定不需用到的仪器是( )A、烧杯 B、漏斗 C、燃烧匙 D、蒸发皿
-
20、下列化学用语表示正确的是( )A、铝离子:Al+3 B、2个硫原子:S C、银元素:AG D、氣化镁:MgCl2