相关试卷
-
1、下图是某反应的微观示意图。
 (1)、请将反应后方框内缺少的微观粒子示意图补画完整。(2)、该反应前后碳元素的化合价如何变化?(3)、请从微观角度解释该反应遵循质量守恒定律的原因。
(1)、请将反应后方框内缺少的微观粒子示意图补画完整。(2)、该反应前后碳元素的化合价如何变化?(3)、请从微观角度解释该反应遵循质量守恒定律的原因。 -
2、请按要求写出反应的符号表达式。(1)、有水生成的化合反应。(2)、有水生成的分解反应。(3)、碱式碳酸铜【】在加热的条件下分解生成三种氧化物。(反应前后元素化合价均未改变)
-
3、为了验证质量守恒定律,某化学小组分别称量了下列三组试剂在敞口烧杯内混合前后的总质量:
①碳酸钠粉末和稀盐酸;②氢氧化钠溶液和硫酸铜溶液;③蔗糖和水。
上述三组试剂中不能验证质量守恒定律的组合及其不符合要求的原因是什么?
-
4、“见著知微、见微知著”是化学学科的特点之一。请从微观角度解释下列现象。(1)、品红在热水中扩散比在冷水中快。(2)、体温计受热,汞柱上升。
-
5、甲、乙、丙三种物质有如图所示的转化关系。
 (1)、若三种物质中都含有地壳中含量最多的元素,甲、乙的组成元素相同,丙是单质。则甲、乙化学性质不同的原因是;乙生成丙的符号表达式为。(2)、若甲和丙都是单质,紫红色金属丙能在加热的条件下与甲反应生成黑色固体乙,该反应的符号表达式为。
(1)、若三种物质中都含有地壳中含量最多的元素,甲、乙的组成元素相同,丙是单质。则甲、乙化学性质不同的原因是;乙生成丙的符号表达式为。(2)、若甲和丙都是单质,紫红色金属丙能在加热的条件下与甲反应生成黑色固体乙,该反应的符号表达式为。 -
6、某钙镁咀嚼片的部分说明书如下图所示。
××牌钙镁咀嚼片
主要成分:碳酸钙、碳酸镁
每片含量:钙;镁
……
(1)、其中“钙、镁”是指(填“元素”、“原子”或“单质”)。(2)、若每片咀嚼片中碳酸钙的质量分数为 , 则该咀嚼片中钙的质量分数为。 -
7、下图是五种粒子的结构示意图。
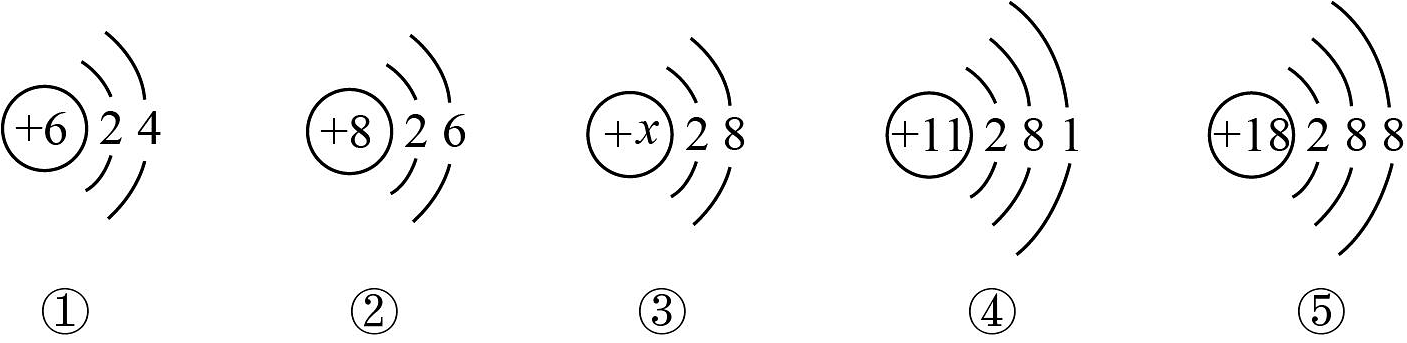 (1)、已知③带2个单位的正电荷,则;它所属元素位于元素周期表中的第周期。(2)、图中具有相对稳定结构的原子是(填化学用语)。
(1)、已知③带2个单位的正电荷,则;它所属元素位于元素周期表中的第周期。(2)、图中具有相对稳定结构的原子是(填化学用语)。 -
8、水与人类的生产生活密切相关。(1)、自来水生产过程为常用(填物质名称)除去水中的颜色、异味。(2)、电解水实验如下图所示。此实验可以得出水是由组成;试管内气体的化学性质是(写出一条即可)。
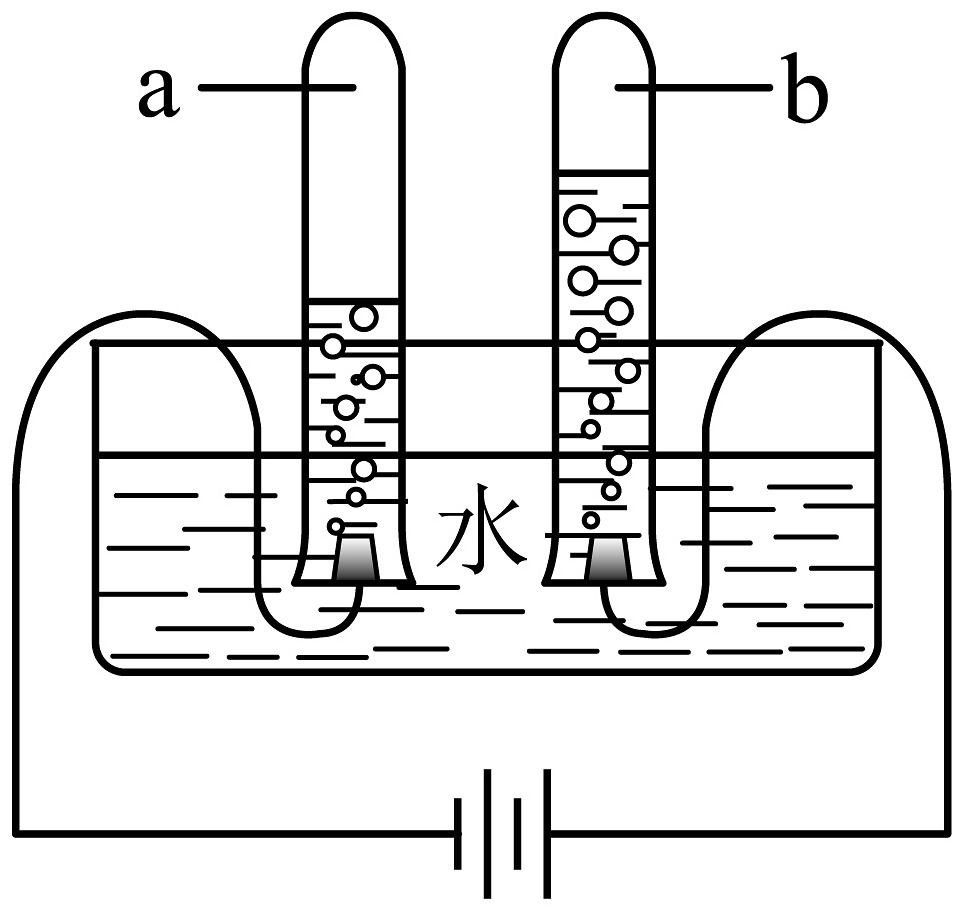
-
9、用正确的化学用语填空。(1)、亚铁离子可表示为;(2)、标出氧化铝中金属元素的化合价;(3)、河南博物院常用空气中含量最多的气体保护文物,该气体的2个分子表示为。
-
10、下图表示一定量的红磷在密闭容器中燃烧的过程。则y不可能表示
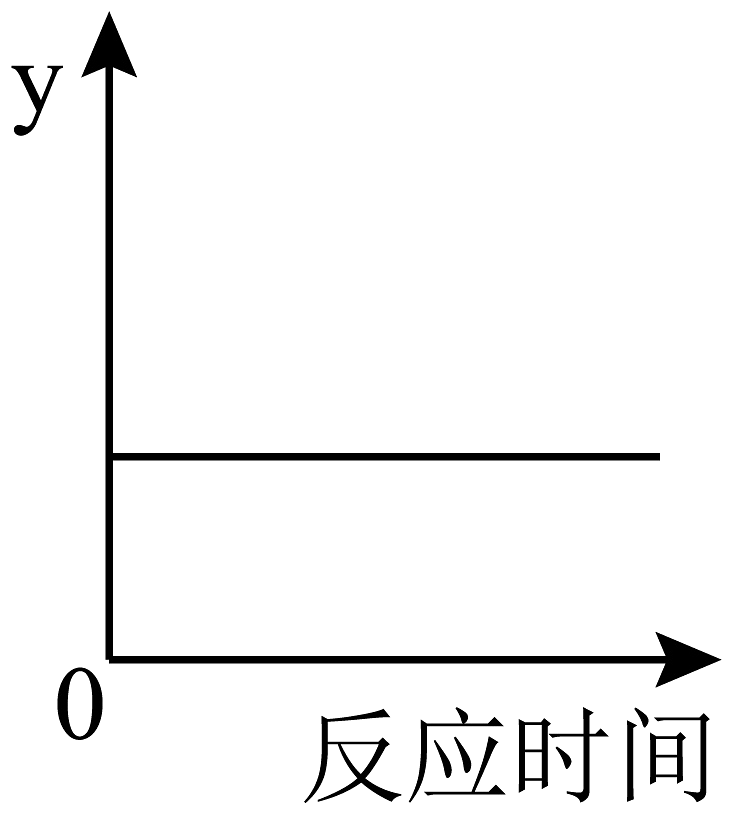 A、分子的总个数 B、元素的总质量 C、原子的总个数 D、物质的总质量
A、分子的总个数 B、元素的总质量 C、原子的总个数 D、物质的总质量 -
11、密闭容器内有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示。下列说法错误的是
 A、物质丙一定是化合物 B、该化学反应中乙、丙质量比为 C、该反应的基本反应类型为分解反应 D、物质丁可能是该反应的催化剂
A、物质丙一定是化合物 B、该化学反应中乙、丙质量比为 C、该反应的基本反应类型为分解反应 D、物质丁可能是该反应的催化剂 -
12、物质的鉴别是重要的实验技能。下列方案不能达到目的的是A、通过闻气味区分氨气和氧气 B、利用燃着的木条区分二氧化碳和氮气 C、通过蒸干看残留物区分自来水和纯净水 D、利用颜色区分硫酸铜溶液和硫酸亚铁溶液
-
13、逻辑推理是一种重要的科学思维。下列推理正确的是A、单质由同种元素组成,所以由同种元素组成的物质一定是单质 B、阳离子是带正电荷的粒子,所以带正电荷的粒子一定是阳离子 C、氧气是由氧元素组成的,所以制取氧气的反应物中一定含有氧元素 D、同种元素的质子数相同,所以质子数相同的粒子一定属于同种元素
-
14、“桂子月中落,天香云外飘”。桂花中含有橙花醇(化学式为),下列有关说法正确的是A、该物质由碳、氢、氧原子构成 B、其相对分子质量为 C、其中碳元素的质量分数最高 D、碳、氢、氧元素质量比为
-
15、化学实验的现象精彩纷呈。以下实验现象的描述中正确的是A、铁在空气中燃烧剧烈,火星四射 B、木炭伸入氧气中,生成能使澄清石灰水变浑浊的气体 C、用浓氨水和酚酞溶液探究分子运动的实验,一段时间后发现浓氨水变红 D、镁条在空气中燃烧,发出耀眼的白光,有白烟产生
-
16、化学是一门实验的学科。下列实验设计能实现其目的是
 A、测定空气中氧气的含量 B、检验氢气的纯度 C、将硬水转化为软水 D、检查装置的气密性
A、测定空气中氧气的含量 B、检验氢气的纯度 C、将硬水转化为软水 D、检查装置的气密性 -
17、从物质分类的角度,冰水混合物不属于A、单质 B、纯净物 C、化合物 D、氧化物
-
18、物质由微观粒子构成。下列物质中既有分子又有离子的是A、空气 B、氨气 C、金刚石 D、食盐水
-
19、同学们在安全教育日活动中制作了一批标识。学校存放酒精消毒喷雾的房间应张贴的标识为A、
 B、
B、 C、
C、 D、
D、
-
20、洁净的空气对人类非常重要。下列物质不会污染空气的是A、二氧化氮 B、细颗粒物 C、二氧化硫 D、二氧化碳