-
1、下列实验方案可以达到实验目的的是
选项
实验目的
实验方案
A
鉴别过氧化氢溶液和水
分别将带火星的木条接近盛有等量两种液体的试管口
B
除去泥水中的不溶性物质
沉降、过滤
C
将硬水转化为软水
蒸馏
D
鉴别二氧化碳和氮气两瓶气体
将燃着的木条分别伸入集气瓶中
A、A B、B C、C D、D -
2、推理是化学学习的一种方法,以下推理正确的是A、单质中只含有一种元素,因此只含有一种元素的物质一定是单质 B、氧气是由氧元素组成的,所以制取氧气的反应物中一定含氧元素 C、在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,非金属元素一定显负价 D、稀有气体元素的原子最外层电子数为8(氦除外),因此微粒
 一定是稀有气体元素的原子
一定是稀有气体元素的原子
-
3、下列符号中,既表示一种元素符号,又能表示该元素的一个原子,还能表示该元素组成的物质的是A、 B、 C、 D、
-
4、下列对有关事实的解释中错误的是A、热水使变瘪的乒乓球复原——受热后分子体积变大 B、冰水共存物属于纯净物——冰和水都由水分子构成 C、酒精燃烧,水不燃烧——分子不同,化学性质不同 D、酒精挥发——酒精分子总是在不断的运动
-
5、下图是两种气体发生反应的微观示意图,其中相同的球代表同种原子。下列说法正确的是
 A、反应物分子在化学变化中不可分 B、反应后生成物属于混合物 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应
A、反应物分子在化学变化中不可分 B、反应后生成物属于混合物 C、化学反应前后原子的种类不变 D、该反应既不是化合反应也不是分解反应 -
6、下列结构示意图,表示阳离子的是A、
 B、
B、 C、
C、 D、
D、
-
7、下列对实验现象的描述正确的是A、硫在氧气中燃烧发出淡蓝色火焰 B、氢气在空气中燃烧发出蓝色火焰 C、木炭在空气中充分燃烧生成黑色固体 D、铁丝在氧气中燃烧时,火星四射,生成黑色固体
-
8、下列物质中属于氧化物的是A、河水 B、高锰酸钾 C、液态氧 D、五氧化二磷
-
9、如图是实验室制取氧气实验装置图,请回答问题:
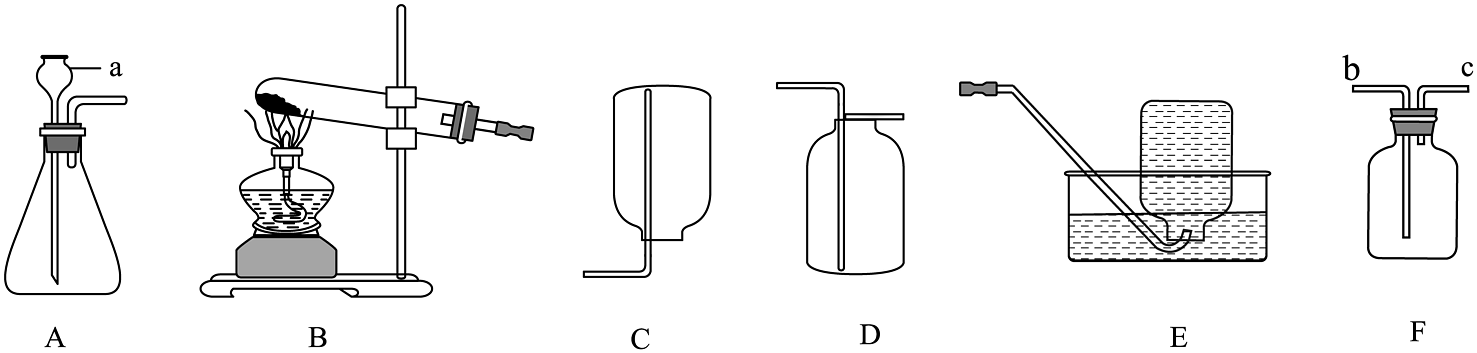 (1)、装置A中仪器a的末端必须浸在液面下,原因是;用该装置制取氧气的化学方程式为。(2)、若用高锰酸钾制氧气发现水槽中的水变成了紫红色,你认为产生该现象的原因可能是;该反应的化学方程式为。(3)、若用装置D收集氧气,写出检验该气体收集满的方法;用E装置收集氧气,如果制得的氧气不纯,可能的原因是(答出一种即可);若用图F所示正放的收集装置,则氧气应从(填“b”或“c”)端通入。(4)、工业上利用煅烧石灰石(CaCO3)的方法生产生石灰(CaO),同时得到产物二氧化碳。若煅烧1500t含杂质10%的石灰石,能生产生石灰多少吨?
(1)、装置A中仪器a的末端必须浸在液面下,原因是;用该装置制取氧气的化学方程式为。(2)、若用高锰酸钾制氧气发现水槽中的水变成了紫红色,你认为产生该现象的原因可能是;该反应的化学方程式为。(3)、若用装置D收集氧气,写出检验该气体收集满的方法;用E装置收集氧气,如果制得的氧气不纯,可能的原因是(答出一种即可);若用图F所示正放的收集装置,则氧气应从(填“b”或“c”)端通入。(4)、工业上利用煅烧石灰石(CaCO3)的方法生产生石灰(CaO),同时得到产物二氧化碳。若煅烧1500t含杂质10%的石灰石,能生产生石灰多少吨? -
10、某化肥厂以煤、空气、水为原料合成氨,生产流程如图所示。
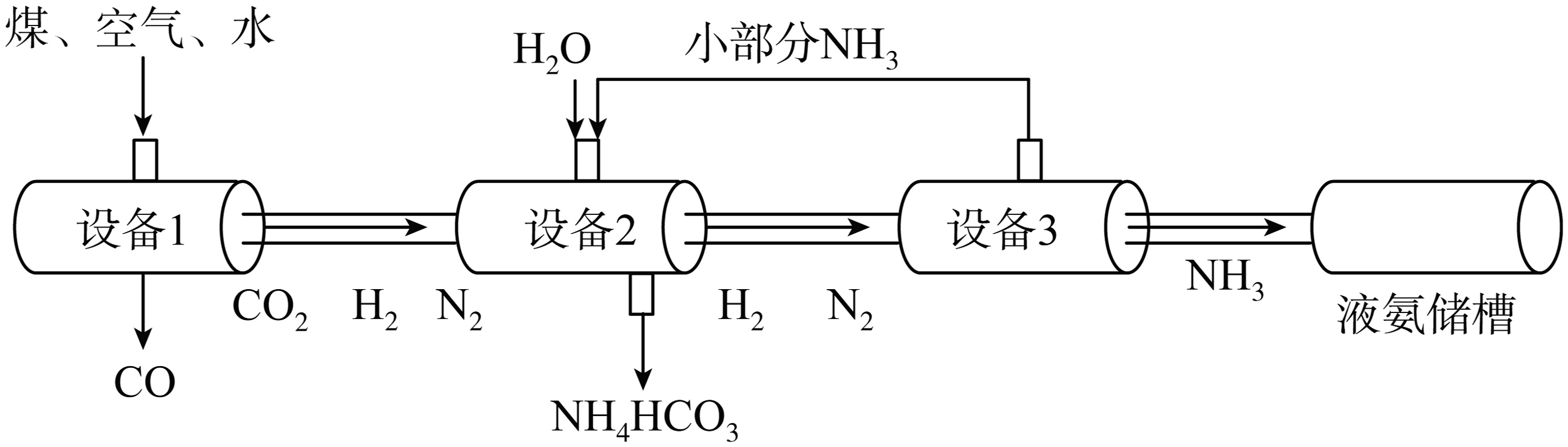 (1)、设备2中参加反应的物质有。(2)、设备3中参加反应的N2和H2的质量比为。
(1)、设备2中参加反应的物质有。(2)、设备3中参加反应的N2和H2的质量比为。 -
11、在化学实验操作中,为了实验的安全和结论的准确,往往要按照一定的顺序进行操作或探究,请回答有关问题:
(1)倾倒液体时,为什么标签要向着手心?
(2)点燃甲烷气体前要检验气体的纯度,请说出原因?
(3)排水法收集氧气后,要先从水槽中移出导管,再熄灭酒精灯,目的是什么?
-
12、公路上,一辆满载的货车由于紧急刹车,轮胎忽然燃烧起来。司机撤离驾驶室时迅速熄火并切断汽车的油路开关,赶来的救援人员一边使用灭火器和水枪灭火,一边设法将车上的易燃物品转移,短时间内就扑灭了火灾,避免了更危险的情况发生。请回答以下问题。(1)、结合燃烧的条件分析为什么轮胎会着火。(2)、司机和救援人员采取了哪些措施灭火,依据的原理是什么?
-
13、现有6.4g未知物和氧气充分反应,经测定生成4.4g二氧化碳,2.8g一氧化碳和7.2g水。则参加反应氧气的质量是 , 参加反应氧气和生成二氧化碳的化学计量数之比为。
-
14、A—D是初中化学常见的物质,A和C的组成元素相同、在常温下均为液体,B为单质,且能供给呼吸,它们的相互转化关系如图所示(箭号所指方向为生成物,部分反应条件已略去)。
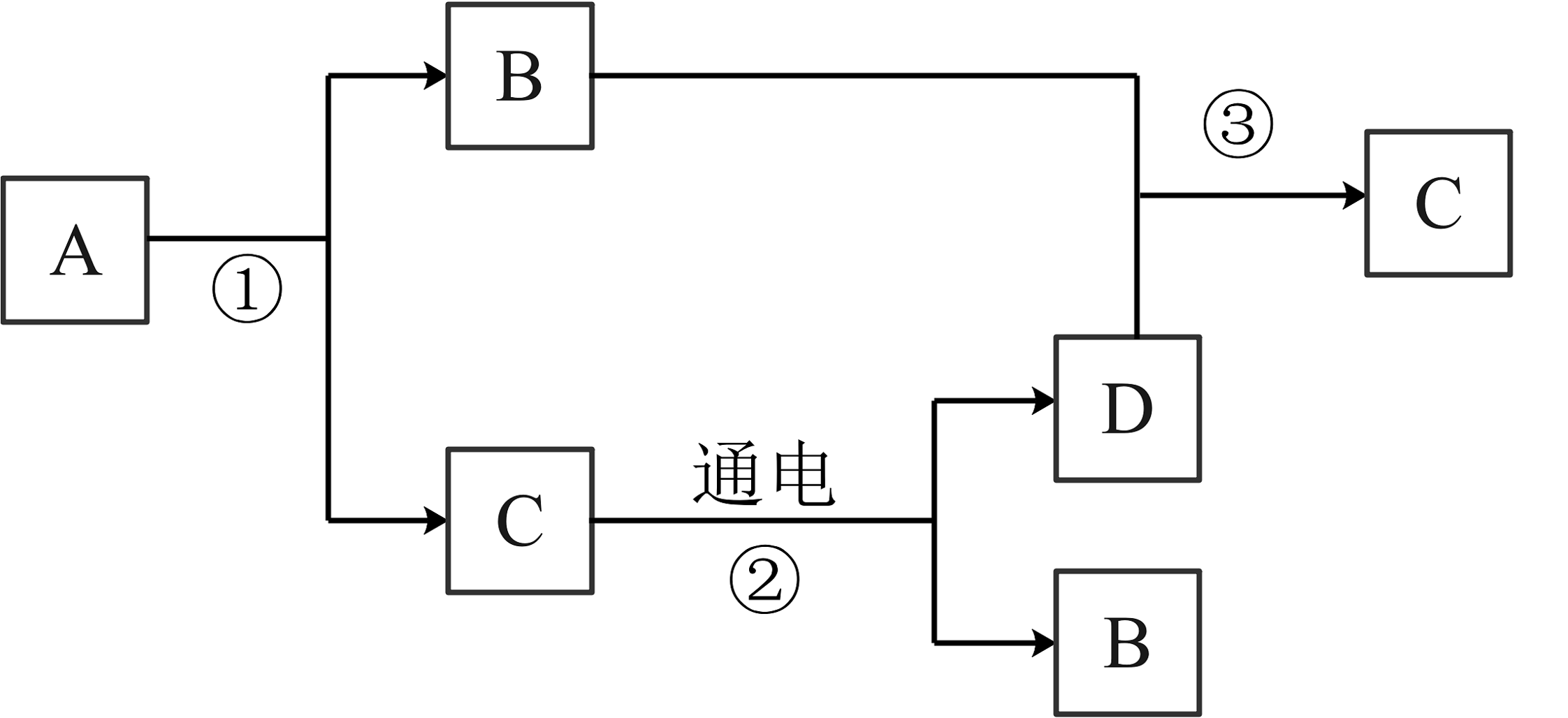 (1)、A物质的名称为;(2)、反应③的符号表达式为;(3)、反应②的基本反应类型为。
(1)、A物质的名称为;(2)、反应③的符号表达式为;(3)、反应②的基本反应类型为。 -
15、“84”消毒液、H2O2溶液都是常用消毒剂。取少量“84”消毒液于试管中,滴加H2O2溶液,发现有大量气泡产生;然后(填写实验操作),观察到(填写现象),证明产生的气体是氧气;NaClO与H2O2溶液反应除生成氧气外,还生成氯化钠和水。该反应的化学方程式为。
-
16、多数金属化学性质活泼,应用广泛。金属钠能与水发生剧烈的反应,生成氢氧化钠和氢气,写出该反应的化学方程式。已知钠、镁、铝的相对原子质量分别为23、24、27,则相同质量的三种金属中,所含原子个数最多的是。
-
17、水与人类的生产生活密切相关。请回答问题:(1)、欲除去黄河水中的不溶性杂质,可通过过滤操作,其中用到的玻璃仪器有烧杯、玻璃棒、。(2)、实验室用电解水的方法来探究水的组成,该反应的化学方程式为;该反应遵守质量守恒定律的微观原因是:化学反应前后,氢、氧原子的均不变。
-
18、用数字和化学符号表示:(1)、地壳中含量最高的金属元素。(2)、保持水的化学性质的最小粒子。(3)、氧化镁中镁元素化合价为+2价。
-
19、在硫酸亚铁和硫酸铁的混合物中,硫元素的质量分数为23%,则混合物中铁元素的质量分数为( )A、46% B、31% C、66% D、无法确定
-
20、下列有关说法正确的是A、原子是最小的粒子故不可再分 B、分子能保持物质的化学性质而原子不能 C、由同种元素组成的物质一定是单质 D、不同种元素的本质区别是原子核内质子数不同