相关试卷
-
1、下列物质的水溶液在空气中小心加热蒸干至质量不再减少为止,能得到较纯净的原溶质的是
①CuSO4 ②FeSO4 ③K2CO3 ④Ca(HCO3)2⑤NH4HCO3 ⑥KMnO4 ⑦FeCl3
A、全部都可以 B、仅①②③ C、仅①③⑥ D、仅①③ -
2、具有如下电子层结构的原子,其相应元素一定属于同一主族的是A、轨道上有2个未成对电子的原子和轨道上有2个未成对电子的原子 B、轨道上只有1个空轨道的原子和轨道上只有1个空轨道的原子 C、最外层电子排布为的原子和最外层电子排布为的原子 D、最外层电子排布为的原子和最外层电子排布为的原子
-
3、下列有关光谱的说法中不正确的是A、原子中的电子在跃迁时会发生能量的变化,能量的表现形式之一是光(辐射),这也是原子光谱产生的原因 B、霓虹灯光、激光、焰火、物理成像都与电子跃迁释放能量有关 C、通过原子光谱可以发现新的元素,也可以鉴定某些元素 D、同一原子的发射光谱和吸收光谱的特征谱线位置相同
-
4、常温下,下列关于的氨水说法正确的是A、 B、稀释10倍,变为9 C、和的盐酸等体积混合后,溶液呈酸性 D、加入固体,溶液减小
-
5、有氯化钠、碳酸钠、碳酸氢钠的固体混合物共4克,加热到质量不再减少为止。此时剩余固体质量为3.38克,在残留的固体中加入足量盐酸,将产生的气体通过干燥管后,通入澄清石灰水中,生成2g固体。(1)、原混合物中碳酸氢钠的物质的量是。(2)、原混合物中碳酸钠的质量是多少?(写出具体计算过程)
-
6、回答下列问题。(1)、某校环保兴趣小组在处理污水样品时,需用质量分数为36.5%、密度为的浓盐酸配制成250mL 0.1mol/L的稀盐酸。下图装置是某同学转移溶液的示意图,图中的错误有、。
 (2)、盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的___________。(填序号)。A、
(2)、盛放浓盐酸的试剂瓶标签上应印有图中警示标识中的___________。(填序号)。A、 B、
B、 C、
C、 D、
D、 (3)、在如图所示仪器中,配制上述溶液一定不需要的是(填图中相应仪器的序号)。
(3)、在如图所示仪器中,配制上述溶液一定不需要的是(填图中相应仪器的序号)。 (4)、根据计算,本实验需要量取浓盐酸的体积为mL(保留小数点后一位),本实验应使用的量筒(填选项)。
(4)、根据计算,本实验需要量取浓盐酸的体积为mL(保留小数点后一位),本实验应使用的量筒(填选项)。A.10mL B.100mL C.250mL D.500mL
(5)、在容量瓶的使用方法中,下列操作正确的是(填选项)。A.使用容量瓶前检查是否漏水
B.容量瓶用水洗净后,再用配好的稀HCl溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
D.配制溶液时,若试样是液体,用量筒取试样后直接倒入容量瓶中,缓慢加水至接近刻度线1~2cm处,用胶头滴管加蒸馏水至刻度线
E.盖好瓶塞,用食指顶住瓶塞,另一只手托住容量瓶底部,反复倒转多次,摇匀
(6)、假设配制时其他操作均正确,只出现以下某一情况,试判断对所配制的溶液浓度的影响(相比于要求的值,即0.1mol/L,填“偏高”、“偏低”或“无影响”)。A.容量瓶中有少量蒸馏水:;
B.配制的溶液装入洁净的但有少量蒸馏水的试剂瓶中:;
C.定容时俯视:。
-
7、某校化学兴趣小组为研究的性质,设计如图装置进行实验(夹持装置已略去)。其中a为干燥的红色纸片,b为湿润的红色纸片,回答以下问题:
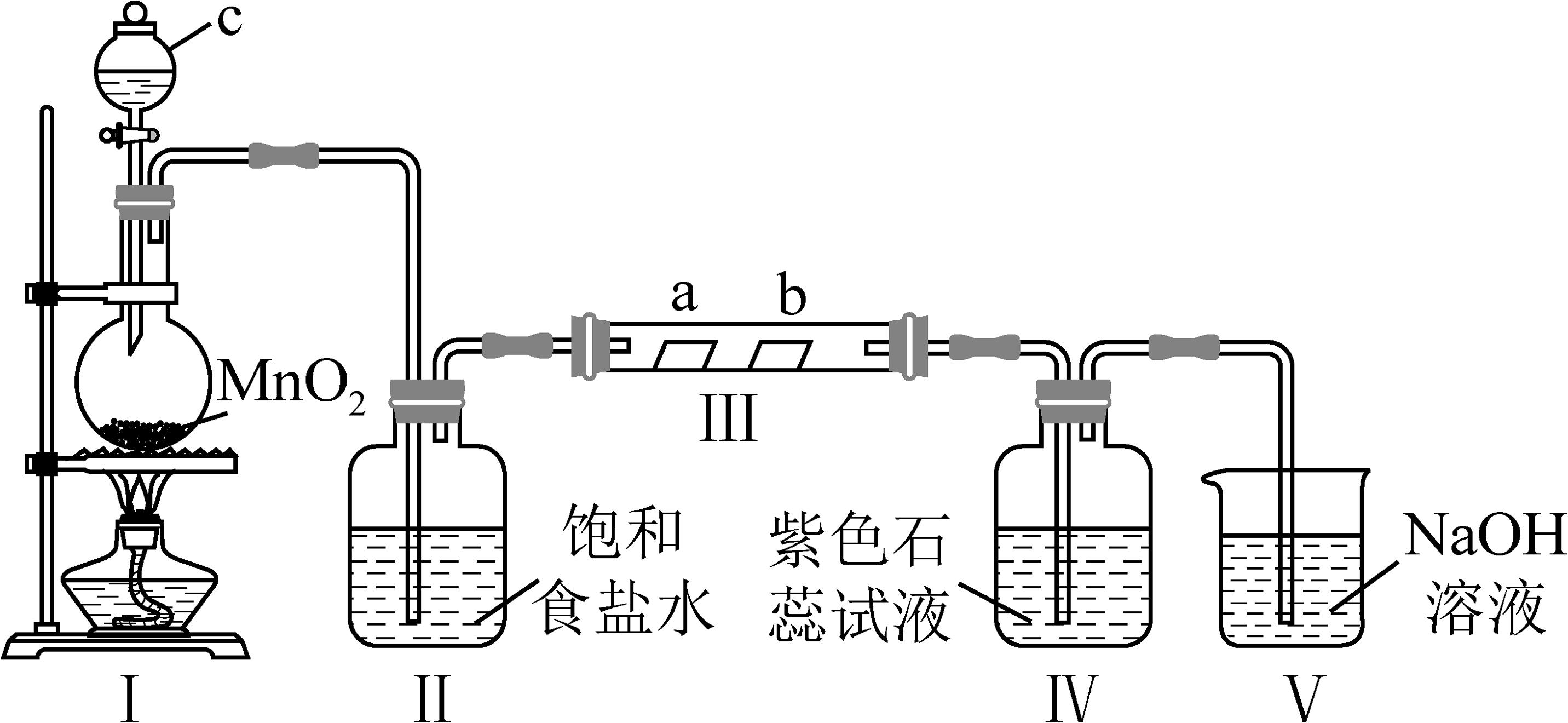 (1)、装置Ⅰ中仪器c的名称是。装置Ⅱ的作用是。(2)、Ⅰ中发生反应的离子方程式为。(3)、若产生足量,实验过程中装置Ⅳ中的实验现象为。(4)、写出装置Ⅴ中发生反应的化学方程式。(5)、实验结束后在装置Ⅲ中观察到b红色褪去,但并未观察到“a无明显变化”这一预期现象。欲观察到a无明显变化,b红色褪去,需在图中装置Ⅱ与Ⅲ之间添加图中的装置(填序号)。
(1)、装置Ⅰ中仪器c的名称是。装置Ⅱ的作用是。(2)、Ⅰ中发生反应的离子方程式为。(3)、若产生足量,实验过程中装置Ⅳ中的实验现象为。(4)、写出装置Ⅴ中发生反应的化学方程式。(5)、实验结束后在装置Ⅲ中观察到b红色褪去,但并未观察到“a无明显变化”这一预期现象。欲观察到a无明显变化,b红色褪去,需在图中装置Ⅱ与Ⅲ之间添加图中的装置(填序号)。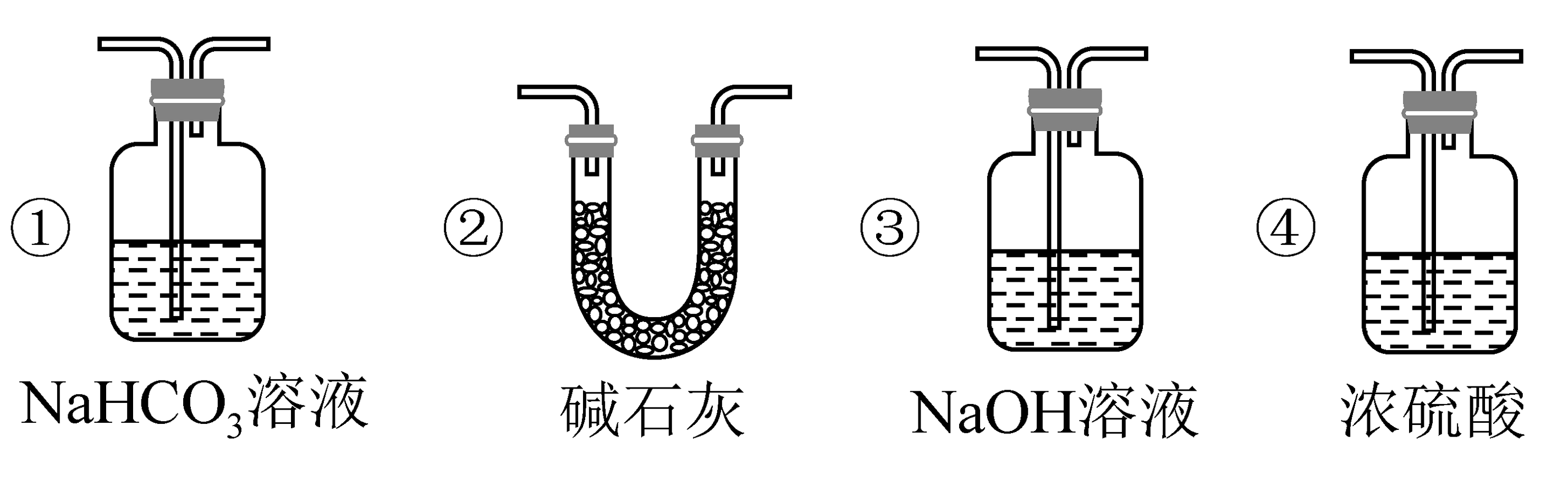 (6)、已知高锰酸钾固体在室温下也能将浓盐酸氧化,发生反应:。
(6)、已知高锰酸钾固体在室温下也能将浓盐酸氧化,发生反应:。①标明上述化学方程式电子转移方向和数目
②若产生 , 则被氧化的物质的量为。
-
8、下图所示转化关系中,A、G均为常见气态非金属单质,B为强碱,C溶液具有漂白作用,D为无氧酸盐,常温下E为无色无味的液体,F为淡黄色固体,反应①、②均可在常温下进行。
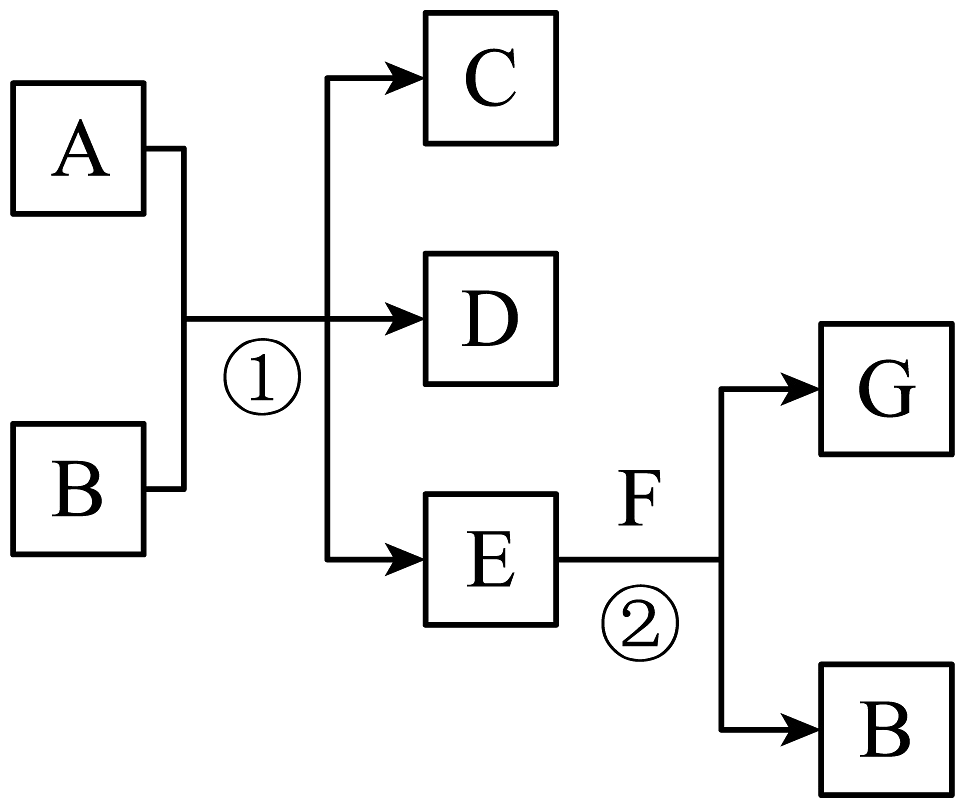
回答下列问题:
(1)、G的化学式:;气体A的颜色为。(2)、写出反应②的化学方程式:。(3)、C溶液可用于家庭清洁卫生,但是不能与洁厕灵(主要成分是盐酸)同时使用,两者混用会产生有毒的氯气,请写出反应的离子方程式:。 -
9、按要求填空。(1)、以下为中学化学中常见的几种物质: A.Cu B.熔融NaCl C. D. E. F.酒精 G.溶液 H.。请按下列分类标准回答问题。
①属于电解质的是(填标号,下同);
②属于酸的是;
③写出E与G反应的离子方程式。
(2)、①写出纯碱的化学式;②写出次氯酸钠在水中的电离方程式。
-
10、下列实验操作和现象及所得出的结论都正确的是
选项
实验操作和现象
结论
A
将干燥的通入到装有潮湿有色布条广口瓶中,观察到有色布条的颜色逐渐褪去
有漂白性
B
Na投入水中会熔成光亮的小球
Na与水反应放热且Na的熔点低
C
同温下,向等物质的量浓度的溶液中分别滴几滴酚酞,观察到红色较深的是
碱性大于
D
向25mL沸水中滴加5-6滴饱和溶液,继续煮沸至混合液呈红褐色,停止加热
该实验得到了沉淀
A、A B、B C、C D、D -
11、1943年我国化学工程专家侯德榜发明了侯氏制碱法,又称联合制碱法,为我国化工事业的发展做出了卓越贡献。其部分工艺流程如图,下列说法不正确的是
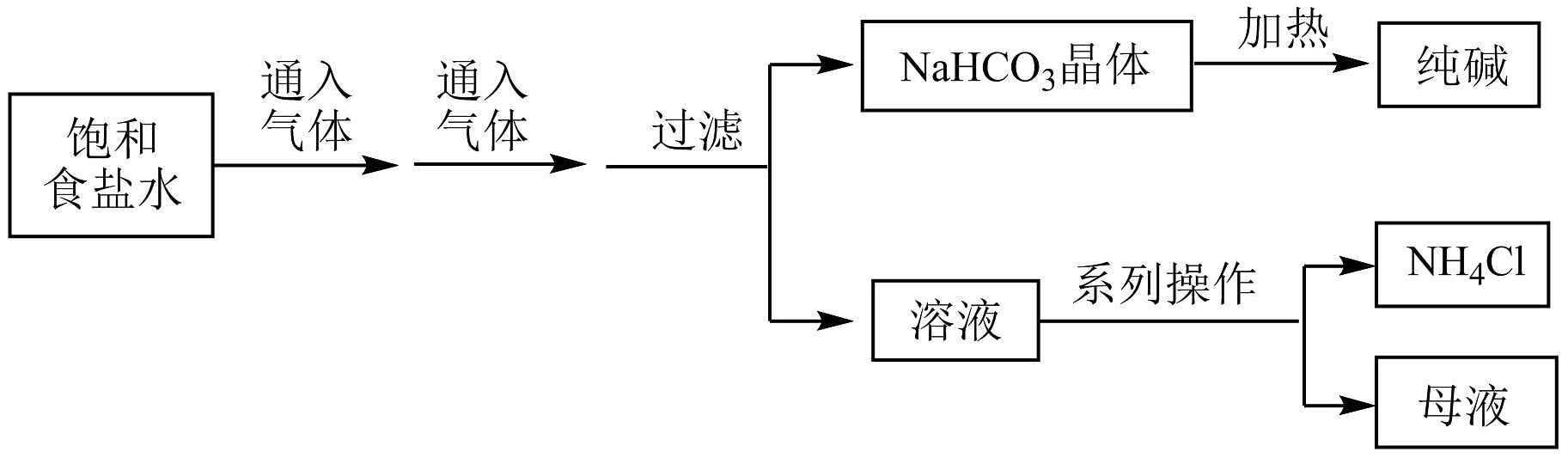 A、该工艺利用了不同物质溶解度的差异 B、流程图中可循环使用的物质有NH3和CO2 C、饱和食盐水中先通入的气体为NH3 , 再通入的气体为CO2 D、副产物NH4Cl可用于化肥工业
A、该工艺利用了不同物质溶解度的差异 B、流程图中可循环使用的物质有NH3和CO2 C、饱和食盐水中先通入的气体为NH3 , 再通入的气体为CO2 D、副产物NH4Cl可用于化肥工业 -
12、某兴趣小组利用数字化实验测定光照过程中氯水的pH、氯水中氯离子的浓度、广口瓶中氧气的体积分数三者的变化,实验结果如图所示。下列说法正确的是


 A、氯水中存在自由移动的离子,能导电,故属于电解质 B、氯水中没有HCl,光照过程中才有HCl生成 C、光照过程中体积分数逐渐增加,说明发生了氧化还原反应,其中为还原产物 D、由图可知,50s时浓度约为450mg/L,计算可知氯水中
A、氯水中存在自由移动的离子,能导电,故属于电解质 B、氯水中没有HCl,光照过程中才有HCl生成 C、光照过程中体积分数逐渐增加,说明发生了氧化还原反应,其中为还原产物 D、由图可知,50s时浓度约为450mg/L,计算可知氯水中 -
13、二氧化氯(ClO2)是一种黄绿色易溶于水的气体,常用于饮用水消毒。下列有关ClO2制备与杀菌的说法不合理的是A、可用饱和食盐水除去ClO2中的NH3 B、ClO2在强碱性环境中使用失效,可能的原因是:2ClO2+2OH- =ClO+ ClO+H2O C、NaClO2在酸性条件下歧化生成ClO2和NaCl,则n(氧化剂):n(还原剂)=1:4 D、等物质的量的ClO2杀菌效果比Cl2强
-
14、已知某固体样品中含有、中的一种或两种,下列说法正确的是
 A、取适量样品配成溶液,滴加1滴酚酞溶液,若溶液变红,则样品中只含有 B、取样在试管中加热,将可能产生的气体全部通入澄清石灰水,若最终仍为澄清溶液,则样品中不含 C、取一定量的样品,利用如图所示装置测定样品中的含量,若球形干燥管增重4.4g,则所取样品中含有0.1mol D、已知固体样品同时含有和。现取一定质量的样品配成溶液,滴加溶液至沉淀完全,根据白色沉淀的质量可求出的含量
A、取适量样品配成溶液,滴加1滴酚酞溶液,若溶液变红,则样品中只含有 B、取样在试管中加热,将可能产生的气体全部通入澄清石灰水,若最终仍为澄清溶液,则样品中不含 C、取一定量的样品,利用如图所示装置测定样品中的含量,若球形干燥管增重4.4g,则所取样品中含有0.1mol D、已知固体样品同时含有和。现取一定质量的样品配成溶液,滴加溶液至沉淀完全,根据白色沉淀的质量可求出的含量 -
15、三效催化剂能有效实现汽车尾气中CO、CxHy、NOx三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。下列说法正确的是
 A、在转化过程中,氮元素均被还原 B、X的化学式为Ba(NO3)2 C、还原过程中每生成1molN2分子,转移5mol电子 D、依据图示判断催化剂不参与储存和还原过程
A、在转化过程中,氮元素均被还原 B、X的化学式为Ba(NO3)2 C、还原过程中每生成1molN2分子,转移5mol电子 D、依据图示判断催化剂不参与储存和还原过程 -
16、设表示阿伏加德罗常数的值,下列判断正确的是A、5.6g铁与足量盐酸反应转移的电子数为 B、溶液中含有的数目为 C、标准状况下,22.4L CO和的混合气体中所含的碳原子数为 D、0.1mol过氧化钠含有的离子总数为
-
17、下列实验装置正确且能达到相应实验目的的是
 A、用装置甲制备胶体 B、用装置乙检验中是否混有 C、用装置丙配制溶液 D、用装置丁吸收多余的
A、用装置甲制备胶体 B、用装置乙检验中是否混有 C、用装置丙配制溶液 D、用装置丁吸收多余的 -
18、化学与生活等密切相关,下列说法错误的是A、连花清瘟胶囊的成分中石膏属于纯净物 B、“铁质菜刀生锈”与氧化还原反应有关 C、维生素C可将转变为 , 所以维生素C具有还原性,常用作抗氧化剂 D、为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
-
19、配制一定物质的量浓度的溶液是一个重要的定量实验,下列有关说法正确的是A、容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液 B、配制一定物质的量浓度的稀盐酸时,用量筒量取9.82mL浓盐酸 C、可在容量瓶中直接稀释浓盐酸 D、定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
-
20、下列反应的离子方程式书写正确的是A、次氯酸与KOH溶液反应:H++OH-=H2O B、Cl2与水反应:Cl2+H2O=2H++ClO-+Cl- C、过氧化钠与水反应:2O+2H2O=4OH-+O2↑ D、将硫酸铜溶液与氢氧化钠溶液混合:Cu2++2OH-=Cu(OH)2↓