相关试卷
-
1、X、Y、Z、W四种元素为短周期元素,它们在元素周期表中的相对位置如下表所示,已知W的最高正价与最低负价代数和为6,下列说法正确的是( )
X
Y
Z
W
A、Z的气态氢化物稳定性高于Y的气态氢化物 B、标准状况下,X的单质状态与W的相同 C、X、Z、W对应氧化物的水化物均为强酸 D、Z的简单离子还原性弱于W的简单离子还原性 -
2、已知反应: , 下列结论正确的是( )A、HCl作还原剂,氢元素被氧化 B、氧化性: C、该反应转移的电子数为 D、氧化剂和还原剂个数之比为1:5
-
3、核污水中存在锶的一种放射性核素存在引发白血病的风险,这种核素的中子数和质子数之差为( )A、38 B、52 C、12 D、14
-
4、为了检验某长期放置的FeCl2溶液是否完全变质,可选用的试剂是( )A、氨水 B、酸性高锰酸钾溶液 C、KSCN D、淀粉
-
5、有关化学键的说法错误的是( )A、存在离子键的物质一定是离子化合物 B、化学键是相邻原子或离子之间的强烈的相互作用,该作用只表现为吸引力 C、存在共价键的物质可能为单质,可能是共价化合物,也可能是离子化合物 D、化学键的强度远大于分子间作用力,一般而言化学键强度也强于氢键
-
6、下列说法中不正确的是( )A、铁在一定条件下与氧气或水蒸气反应的产物均有 B、铁在高温下与水蒸气的反应是置换反应 C、铁与盐酸反应生成氯化铁和氢气 D、铁与的反应属于氧化还原反应
-
7、用 NA表示阿伏加德罗常数,下列说法正确的是( )A、标准状况下,11.2L N2 和O2的混合气体中所含分子数为 NA B、常温常压下 14 g 氮气中含有 NA个原子 C、常温常压下,48gO3 的体积约为 22.4 L D、标准状况下,18g 水的体积约为 22.4 L
-
8、下图是氯及其化合物的“价-类”二维图,a、b、c、d、e均为含氯元素的物质。下列叙述不正确的是( )
 A、a和d的溶液均呈酸性 B、e可由b与碱溶液反应得到 C、工业上用b与充分混合后在光照下制盐酸 D、化合物c的化学式为 , 可作自来水消毒剂
A、a和d的溶液均呈酸性 B、e可由b与碱溶液反应得到 C、工业上用b与充分混合后在光照下制盐酸 D、化合物c的化学式为 , 可作自来水消毒剂 -
9、下列关于氧化钠和过氧化钠的叙述正确的是( )A、在Na2O2与CO2的反应中,氧化剂是Na2O2 , 还原剂是CO2 B、Na2O与Na2O2都能与水反应生成碱,它们都是碱性氧化物 C、Na2O2和Na2O都是白色固体,都能与冷水作用得到O2和NaOH D、相同个数的氧化钠和过氧化钠中,阴、阳离子个数之比均为1:2
-
10、下列离子方程式正确的是( )A、MgSO4溶液与Ba(OH)2溶液反应:+Ba2+=BaSO4↓ B、Al2O3溶于盐酸中:O2-+2H+=H2O C、Cu片插入AgNO3溶液中:Cu+Ag+=Cu2++Ag D、澄清石灰水中加入盐酸:OH-+H+=H2O
-
11、下列有关化学用语正确的是( )A、次氯酸的结构式:H-Cl-O B、中子数为10的氧原子:10O C、NH4Cl的电子式:
 D、铝离子的结构示意图:
D、铝离子的结构示意图:
-
12、下列反应不属于氧化还原反应的是( )A、 B、 C、 D、
-
13、与溶液中浓度相同的是( )A、溶液 B、溶液 C、溶液 D、溶液
-
14、下列关于钠单质的说法不正确的是( )A、切取钠后剩余的钠块应放回原瓶 B、钠着火时需要用干燥的沙土灭火 C、切开钠的外皮后,钠的光亮表面变暗是因为生成了 D、钠单质与溶液反应,不能置换出铜单质
-
15、下列各组中的离子,能在溶液中大量共存的是( )A、K+、H+、SO、OH- B、Na+、Ca2+、、 C、Na+、H+、Cl-、 D、Na+、Cu2+、Cl-、SO
-
16、下列叙述中,正确的是( )A、KNO3固体不导电,所以KNO3不是电解质 B、铜丝、石墨均能导电,所以它们都是电解质 C、熔融的MgCl2能导电,所以MgCl2是电解质 D、NaCl溶于水,在通电条件下才能发生电离
-
17、按溶液、浊液、胶体的顺序排列正确的是( )A、矿泉水、豆浆、牛奶 B、糖水、食盐水、茶叶水 C、碘酒、泥水、血液 D、Cu(OH)2悬浊液、澄清石灰水、石灰浆
-
18、下列物质属于纯净物的是( )A、煤 B、氯水 C、稀硫酸 D、液氨
-
19、利多卡因(vi)是常用的局部麻醉剂,其合成路线如图所示:
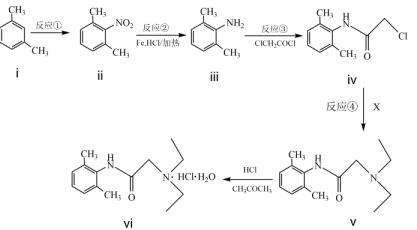 (1)、化合物i的名称为。(2)、反应②的反应类型为。(3)、化合物Y为iii的同分异构体,属于芳香族化合物且核磁共振氢谱中峰组数目与iii的相同,写出一种符合上述条件的的结构简式。(4)、的分子式为 , 有关化合物的说法正确的是____(填字母)。A、属于非极性分子 B、分子中含有手性碳原子 C、分子的核磁共振氢谱中有三组峰 D、反应④的过程中有的断裂(5)、根据化合物的结构特征,分析其可能具有的化学性质,完成下表。
(1)、化合物i的名称为。(2)、反应②的反应类型为。(3)、化合物Y为iii的同分异构体,属于芳香族化合物且核磁共振氢谱中峰组数目与iii的相同,写出一种符合上述条件的的结构简式。(4)、的分子式为 , 有关化合物的说法正确的是____(填字母)。A、属于非极性分子 B、分子中含有手性碳原子 C、分子的核磁共振氢谱中有三组峰 D、反应④的过程中有的断裂(5)、根据化合物的结构特征,分析其可能具有的化学性质,完成下表。序号
反应试剂、条件
反应形成的新结构
反应类型
a
加成反应
b
氧化反应(生成有机产物)
(6)、以苯胺(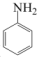 )为原料,利用反应③和④的原理,合成化合物
)为原料,利用反应③和④的原理,合成化合物 。
。已知
 。
。基于你设计的合成路线,回答下列问题:
(a)合成路线中,填(“有”或“没有”)涉及到碳原子杂化类型的改变。
(b)步骤中涉及反应④原理的化学方程式为。
-
20、甲醛(是主要的室内环境污染物,同时又是重要的化工原料。(1)、Ⅰ.利用分光光度法测定室内含量
测定原理:将痕量加入过量酸性溶液中,被还原为 , 再加入过量KI-淀粉溶液,溶液显蓝色。已知:溶液吸光度大小与溶液颜色深浅成正比。
①基态原子的核外电子排布式:。
②完成离子方程式:
(2)、测定方法:实验①:向一定量待测溶液中滴加过量酸性溶液,振荡后加入过量的淀粉-KI溶液。
实验②:用等体积去离子水代替实验①中的溶液,重复上述操作。
两组实验充分反应后,测得不同波长下吸光度 , 绘制吸收光谱曲线如下图所示。

①请你判断表现实验①中溶液吸光度的曲线为。
②根据上图曲线,选定在波长下,测定不同浓度溶液的吸光度 , 得到之间的关系为:。 , 某待测溶液的吸光度为0.182,则该溶液中含量为。
(3)、Ⅱ.甲醛的制备:甲醇脱氢法已知反应a:
反应b:
反应c:
反应d:
。
(4)、在一个恒容密闭容器中充入 , 在催化剂作用下发生反应a、d。在不同温度下连续反应后,测得甲醇的转化率、甲醛的选择性与温度的关系如下图所示。
①600℃时,体系中的物质的量为 , 平均反应速率。
②当温度高于650℃,甲醛的选择性下降的原因不可能是。
A.升高温度使催化剂活性降低 B.升高温度使反应逆向移动
C.温度升高反应速率加快 D.升高温度使反应正向移动