相关试卷
-
1、硝基苯甲酸乙酯在存在下发生水解反应: , 两种反应物的初始浓度均为时测得 , 的转化率随时间变化的数据如表所示,下列说法不正确的是( )
0
120
180
240
330
530
600
700
800
0
33.0
41.8
48.8
58.0
69.0
70.4
71.0
71.0
A、反应在区间的平均反应速率为 B、平均反应速率:区间区间 C、时该反应的平衡常数约为6.0 D、为提高的平衡转化率,除可适当控制反应温度外,还可以增大浓度,及时分离出生成物 -
2、工业上以和为原料在一定温度和压强下合成尿素.反应分两步进行:
i.和生成; iⅱ.分解生成尿素.
结合反应历程中的能量变化示意图,下列说法不正确的是( )
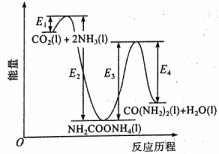 A、i为放热反应,ⅱ为吸热反应 B、正反应的活化能:反应反应ⅱ C、反应达平衡后,升高温度(保持其它条件不变),中间产物减小 D、
A、i为放热反应,ⅱ为吸热反应 B、正反应的活化能:反应反应ⅱ C、反应达平衡后,升高温度(保持其它条件不变),中间产物减小 D、 -
3、下列说法正确的是( )A、的基态原子核外电子共占有8种不同的能级 B、邻羟基苯甲醛分子内氢键示意图:
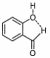 C、第四周期元素的基态原子中,未成对电子数最多的是
D、分子中的键形状:
C、第四周期元素的基态原子中,未成对电子数最多的是
D、分子中的键形状:
-
4、水溶液呈碱性的是( )A、 B、 C、 D、
-
5、实验室有甲、乙两瓶丢失标签的无色溶液,其中一瓶是盐酸,另一瓶是碳酸钠溶液。为确定甲、乙两瓶溶液的成分及其物质的量浓度,现操作如下:
①量取50.00mL甲溶液,向其中缓慢滴加乙溶液20.00mL,共收集到二氧化碳气体560mL。
②另取20.00mL乙溶液,向其中缓慢滴加甲溶液50.00mL,共收集到二氧化碳气体224mL。上述气体体积均已换算为标准状况,则根据上述操述及实验数据填空:乙是 , 甲溶液的物质的量浓度为 , 乙溶液的物质的量浓度为;(二氧化碳在溶液中的少量溶解忽略不计)
-
6、某同学做“被氧化”的实验,发现溶液变深棕色。猜想可能是生成的或NO与或反应,使溶液变为深棕色,设计下列装置探究。回答下列问题
 (1)、检查气密性,加入药品后关闭c打开a、b,通一段时间的目的是。(2)、反应开始时装置甲中发生反应的离子方程式是。(3)、关闭(选填“a”“b”“c”),打开(选填“a”“b”“c”)及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO与反应;(4)、完成(3)中实验后,关闭分液漏斗活塞,打开a通一段时间 , 更新丙、丁中试剂,关闭a和b,打开c及分液漏斗活塞。反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明也可与反应。对此你认为这个结论(填“合理”“不合理”),理由是(若你认为合理此空不用填)(5)、这个装置的一个缺陷是。(6)、实验结束后,同学们发现装置甲中溶液呈绿色,而不显蓝色。A同学认为是该溶液中硝酸铜的质量分数较高所致,而B同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验方案来判断两种看法是否正确。这些方案中可行的是(填字母)。
(1)、检查气密性,加入药品后关闭c打开a、b,通一段时间的目的是。(2)、反应开始时装置甲中发生反应的离子方程式是。(3)、关闭(选填“a”“b”“c”),打开(选填“a”“b”“c”)及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明NO与反应;(4)、完成(3)中实验后,关闭分液漏斗活塞,打开a通一段时间 , 更新丙、丁中试剂,关闭a和b,打开c及分液漏斗活塞。反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明也可与反应。对此你认为这个结论(填“合理”“不合理”),理由是(若你认为合理此空不用填)(5)、这个装置的一个缺陷是。(6)、实验结束后,同学们发现装置甲中溶液呈绿色,而不显蓝色。A同学认为是该溶液中硝酸铜的质量分数较高所致,而B同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验方案来判断两种看法是否正确。这些方案中可行的是(填字母)。a.加热该绿色溶液,观察颜色变化
b.加水稀释该绿色溶液,观察颜色变化
c.向该绿色溶液中通入氮气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
-
7、人胃酸(主要成分是盐酸)过多,会引起很多胃病,需服用抗酸药治疗。抗酸药胃舒平的主要成分是氢氧化铝,某同学为测定该药中氢氧化铝的质量分数进行如下几步操作(设该药片中的其他成分不与盐酸或氢氧化钠反应):
步聚1:取1粒药片(每片药片的质量为0.50g)研碎
步聚2:将上研碎的药片粉末加入到40.00mL0.40mol/L稀盐酸中溶解
步聚3:用0.40mol/LNaOH溶液中和过量稀盐酸,记录消耗NaOH溶液的体积;
请回答下列问题。
(1)、实验室用密度为质量分数为36.5%的浓盐酸配制该0.40mol/L盐酸溶液240mL,应用量筒量取mL浓盐酸。(2)、实验用到的玻璃仪器有烧杯、玻璃棒、量筒和。(3)、下列操作会使配制的溶液浓度偏低的有____。A、转移溶液时,未洗涤玻璃棒和烧杯内壁 B、配制溶液前容量瓶底部有少量蒸馏水残留 C、摇匀后发现液面下降,再加水至刻度线 D、定容时俯视刻度线 E、溶液未冷却即转移到容量瓶中(4)、某同学4次测定所消耗的NaOH溶液的体积如下:测定次数
第1次
第2次
第3次
第4次
V[NaOH(aq)]/mL
16.04
15.96
16.20
16.00
根据这个同学的实验数据,计算这种药片中氢氧化铝的质量分数为%(结果保留小数点后两位)。
-
8、某化合物A(由三种元素构成),为了探究其组成,进行如下实验
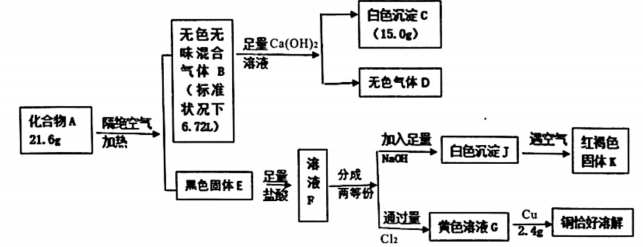
已知:气体D在标准状况下的密度为1.25g/L。试回答
(1)、黑色固体E的化学式。(2)、写出溶液F中通入过量的离子方程式。(3)、写出化合物A隔绝空气加热的化学方程式。(4)、写出检验黄色溶液G中金属阳离子的方法:。(5)、红褐色固体K受热完全分解生成红棕色固体,某同学取该红棕色固体与一定量的反应后的固体,溶于足量稀盐酸中,再往其中滴加硫氰化钾溶液,溶液未变红。该同学得出结论:红棕色固体已反应完。你认为该同学的结论是否正确?(填“是”或“否”),请结合离子方程式说明原因。 -
9、已知短周期主族元素A、B、C、D、E分布在三个周期,B、C最外层电子数相同,E原子序数大于C,其中E的简单离子半径在同周期中最小,C单质极易与常见无色无味液态物质发生置换反应且做氧化剂,短周期中D的最高价氧化物的水化物的碱性最强。回答下列问题:(1)、D在周期表中的位置是 , D与A形成化合物的电子式为。(2)、B、C、D简单离子的半径由大到小的顺序为(填离子符号),写出B离子的结构示意图。(3)、E的单质与D的最高价氧化物的水化物反应的离子方程式。
-
10、回答下列问题:(1)、①金刚砂的主要成分的化学式是。(2)、分子的空间结构为 , 共价键为键(填“极性”或“非极性”)(3)、比较还原性强弱:(填“>”“<”或“=”);用一个离子方程式说明与与的还原性相对强弱。(4)、科学家已获得了气态分子,其结构为正四面体。已知断裂1molN-N吸收193kJ能量,断裂1molN≡N吸收946kJ能量,则完全转化为时(填“吸收”或“放出”)能量

-
11、下列实验目的、操作、现象及结论合理的是( )
实验目的
实验操作
现象及结论
A
比较与氧化性强弱
取少量溶液于试管中,滴入硫酸酸化的溶液
溶液由浅绿色变为黄色氧化性:
B
比较Mg与Al金属性强弱
向同浓度等体积的、溶液中分别滴加同浓度的过量的NaOH溶液
溶液中有白色沉淀生成且不溶解,溶液中有白色沉淀生成后溶解,则金属性:Mg>Al
C
检验溶液中是否含有
向溶液中滴加酸性溶液
若紫红色退去,则溶液中含有
D
检验溶液中是否含有
取少量溶液于试管中,滴加稀盐酸
若产生的气体能使澄清石灰水变浑浊,则溶液中含有
A、A B、B C、C D、D -
12、溶液X中含有下表中离子若干种,且离子浓度均为相等(不考虑水的电离与离子水解)。向X中加入足量稀盐酸,有气体生成,经分析反应前后阴离子种类没有变化,下列说法正确的是( )
阳离子
、、、、、
阴离子
、、、、、
A、溶液X中一定有 B、原溶液一定没有、 , 但、不确定 C、溶液X中可能有或中的一种或两种都有 D、溶液X中至少1种阳离子,2种阴离子,最多2种阳离子,3种阴离子 -
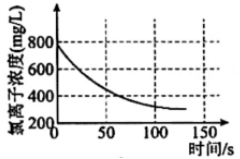
13、下列选项描述与对应图像相符的是( )
①
 ②
②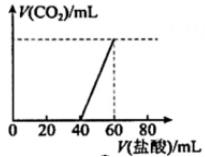 ③
③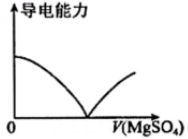 ④
④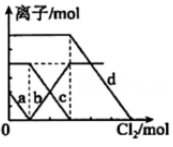 A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为、NaOH混合液中滴加盐酸产生的图像,且 C、图③为溶液中滴加溶液的导电性变化图像,导电能力约为0的原因是两者恰好完全反应且生成物都不是电解质 D、图④为、混合液,各离子物质的量随氯气通入的变化图像,c代表的是
A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为、NaOH混合液中滴加盐酸产生的图像,且 C、图③为溶液中滴加溶液的导电性变化图像,导电能力约为0的原因是两者恰好完全反应且生成物都不是电解质 D、图④为、混合液,各离子物质的量随氯气通入的变化图像,c代表的是 -
14、将20.6gAl、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体6.72L(标况)。另取等质量的合金溶于过量的稀硝酸中生成8.96L(标况)NO,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量是( )A、25.4g B、41.0g C、30.8g D、28.3g
-
15、合成氨及其衍生物工业是化工生产的重要门类,请结合图示判断下列说法正确的是( )
 A、湿润的淀粉-KI试纸可以鉴别气体2和溴蒸气 B、饱和NaCl溶液中先通入过量再通入过量可以得到固体1 C、1L气体1、2的混合气与在一定条件下转化为对坏境无害的物质,混合气中二者的体积比为1:1 D、气体2能与水反应生成故气体2是酸性氧化物
A、湿润的淀粉-KI试纸可以鉴别气体2和溴蒸气 B、饱和NaCl溶液中先通入过量再通入过量可以得到固体1 C、1L气体1、2的混合气与在一定条件下转化为对坏境无害的物质,混合气中二者的体积比为1:1 D、气体2能与水反应生成故气体2是酸性氧化物 -
16、由一种阳离子与两种酸根阴离子组成的盐称为混盐,是一种常见的混盐。下列说法不正确的是( )A、有较强的氧化性 B、有类似于漂白粉的性质,也是混合物 C、由氯气为原料,每生成 , 转移的电子为1mol D、的溶液中加入足量浓硫酸,可有黄绿色的气体产生
-
17、关于反应: , 下列说法正确的是( )A、若有参加反应,则生成 B、中氮元素为-1价 C、氧化产物与还原产物的物质的量之比为15:1 D、若参加反应,转移电子的物质的量为10mol
-
18、下列离子方程式书写正确的是( )A、大理石与稀硝酸反应: B、碳酸氢钠溶液和过量的澄清石灰水混合: C、少量通入溶液中: D、过量铁粉投入稀硝酸中:
-
19、向用盐酸酸化的溶液中加入溶液,产生的沉淀质量m与加入的体积V之间的关系,不可能是下图中的( )A、
 B、
B、 C、
C、 D、
D、
-
20、下列“类比”合理的是( )A、和反应是氧化还原反应,则BrCl和反应生成HBrO和HCl也是氧化还原反应 B、Mg、Al与浓盐酸构成的原电池中较活泼的Mg作负极,故Mg、Al与氢氧化钠构成的原电池中也是Mg作负极 C、与能反应生成S,故与能在一定条件下反应生成 D、中Cl的化合价为+1价,则中F的化合价为+1价