相关试卷
-
1、我校化学社团的同学们通过查阅资料设计了一种制备氢氧化亚铁沉淀的实验装置,其实验原理是先在封闭体系中利用铁粉和盐酸得到氯化亚铁;亚铁盐溶液再与氢氧化钠溶液作用即可制得氢氧化亚铁。实验装置如图所示。回答下列问题:
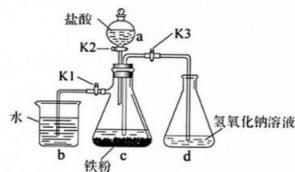 (1)、实验中所用蒸馏水均需经煮沸后迅速冷却,目的是。仪器的名称是。(2)、将过量铁粉置于中,按图连接好装置。打开(填“”“”或“”,下同),关闭。装置的作用是。(3)、经过一段时间,观察到中溶液逐渐变为浅绿色,同时中有气体产生,该气体的作用是。(4)、打开和关闭相应的旋塞,使中浅绿色溶液流入 , 其原因是;中观察到的现象是 , 相关的化学方程式为 , 。
(1)、实验中所用蒸馏水均需经煮沸后迅速冷却,目的是。仪器的名称是。(2)、将过量铁粉置于中,按图连接好装置。打开(填“”“”或“”,下同),关闭。装置的作用是。(3)、经过一段时间,观察到中溶液逐渐变为浅绿色,同时中有气体产生,该气体的作用是。(4)、打开和关闭相应的旋塞,使中浅绿色溶液流入 , 其原因是;中观察到的现象是 , 相关的化学方程式为 , 。 -
2、下图是元素周期表的一部分。
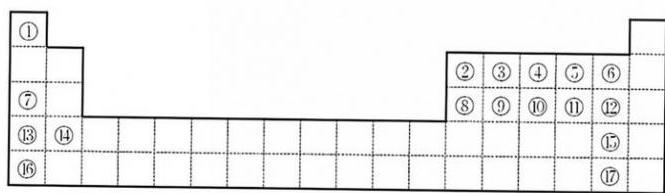
根据要求回答下列问题:
(1)、元素④⑤⑥⑦的简单离子的半径从大到小的顺序是(用离子符号表示)。(2)、元素①②⑦能够形成一种含有极性共价键的离子化合物,该化合物中的阴离子与元素③的简单氢化物分子具有相同的原子数和电子数,写出该阴离子的电子式;一定压强和温度条件下,实验测得元素⑧和组成的化合物的蒸气密度是相同条件下密度的133.5倍,且该化合物中各原子均满足价层8个电子的稳定结构,请写出该物质的结构式。(3)、元素②存在质量数分别为10和11的两种天然稳定同位素,元素②的相对原子质量为10.8,则质量数为10的同位素在自然界中的丰度为;元素也存在两种天然稳定同位素,质量数为35的同位素丰度为 , 质量数为37的同位素丰度为 , 则由这两种同位素构成的、相对分子质量分别为70、72、74的三种分子的个数比为。(4)、元素⑥的简单阴离子的还原性顺序由强到弱为(用离子符号表示),原因是(从结构角度回答) -
3、写出满足下列要求的三个置换反应的化学方程式。
i.所涉及的元素的原子序数不超过20
ii.所涉及的六种单质分属六个不同的主族
①
②
③
-
4、1819年德国矿物学教授E.Mitscherlich发现了化合物中的同晶形规律,这个规律是:相同晶型的化合物具有相同数目的原子且原子以相同的方式结合。例如,和就是互为同晶型的两种化合物。化学家们后来利用这一规律来推测当时某些元素的相对原子质量。现在已知两种非金属元素和的含氧酸钠盐互为同晶型化合物,在的含氧酸钠盐中,钠元素的质量分数为元素的质量分数为 , 其余为氧;在的含氧酸钠盐中,钠元素的质量分数为元素的质量分数为 , 其余为氧。若元素的相对原子质量为 , 则元素的相对原子质量是( )A、 B、 C、 D、
-
5、向镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体。向反应后的溶液中加入的氢氧化钠溶液 , 使金属离子刚好沉淀完全,得到的沉淀质量为。再将所得沉淀灼烧至质量不再改变为止,得到固体。则下列关系正确的是( )
① ② ③
④ ⑤ ⑥
A、①③⑤ B、②④⑥ C、②③④ D、①⑤⑥ -
6、下列选项描述与对应图像相符的是( )
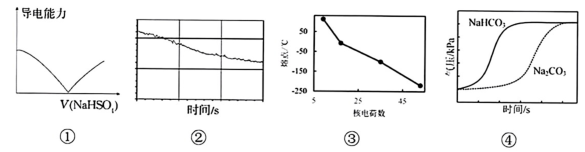 A、图①为向溶液中滴加等浓度的溶液时,溶液导电能力的变化 B、图②为新制饱和氯水在受到阳光直射时,溶液中的变化 C、图③为卤族元素单质的熔点随核电荷数递增的变化 D、图④为向盛有和溶液的密闭容器中滴入等浓度盐酸时气压的变化
A、图①为向溶液中滴加等浓度的溶液时,溶液导电能力的变化 B、图②为新制饱和氯水在受到阳光直射时,溶液中的变化 C、图③为卤族元素单质的熔点随核电荷数递增的变化 D、图④为向盛有和溶液的密闭容器中滴入等浓度盐酸时气压的变化 -
7、下列探究活动得出的结论正确的是( )A、向某无色溶液中滴加溶液,产生白色沉淀:该无色溶液中含有离子 B、向酸性高锰酸钾溶液中滴入溶液,溶液的紫红色褪去:离子具有还原性 C、向某盐的溶液中滴入足量盐酸,无现象,再滴入溶液产生白色沉淀:该盐中含有离子 D、加热铁粉和硫粉的混合物,当反应开始后立即撤去热源,观察到反应能够持续进行:该反应是放热反应
-
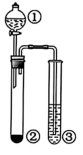
8、利用如图所示装置进行下列实验,能得出相应实验结论的是( )
选项 ①
②
③
实验结论
A.
稀硫酸
粉末
澄清石灰水
非金属性:
B.
浓盐酸
固体
KI-淀粉溶液
氧化性:
C.
水
固体
水
与水反应生成气体
D.
浓盐酸
晶体
溶液
浓盐酸有挥发性
A、A B、B C、C D、D -
9、下列化合物的微观结构中,同种原子间不形成共价键的是( )A、 B、 C、 D、
-
10、下列反应的离子方程式书写不正确的是( )A、未密封的绿矾溶液中出现絮状沉淀: B、将少量明矾溶液滴入过量的氨水中: C、溴水使淀粉试纸变蓝: D、与含有等物质的量的溶液反应:
-
11、实验中若皮肤不慎与白磷接触,可用稀溶液冲洗接触部位,其解毒原理包括两个反应:
①(未配平)
②
下列说法正确的是( )
A、反应①和②中都只是还原剂 B、反应②中被氧化的与还原剂的物质的量之比为 C、用溶液冲洗后,应再用饱和溶液和水冲洗接触部位 D、若有的转化为则理论上反应①和②消耗的分子数之比为 -
12、历史上相当长的一段时间内,人们试图合成高溴酸盐都一直未获得成功,直到1968年美国化学家E.H.Appelman利用含有的硒酸盐发生衰变第一次得到了高溴酸盐,该过程可表示为:。下列说法正确的是( )A、上述过程没有生成新物质,因此是一个物理变化 B、已知位于第四周期VIIA族则可推测在同一周期VIA族 C、根据上述过程可知一个的原子核比一个的原子核多一个中子 D、发生衰变产生的电子若全部用来还原 , 可得到
-
13、为五种不同的核素,化合物和所含元素相同,相对分子质量相差7.含质子,和三种元素位于同周期且的质子数为质子数之和的一半,原子最外层电子数是其核外电子层数的两倍。下列说法不正确的是( )A、原子半径: B、的简单氢化物标准状况下均为气态 C、和互为同位素 D、和的单质均为空气中的成分
-
14、下列关于物质结构或元素周期律(表)的说法中正确的是( )A、短周期主族元素的比较原子半径时,核外电子层数多的均大于核外电子层数少的 B、短周期中具有相同电子层结构的简单离子比较半径时,核电荷数大的离子半径小 C、在化合物分子中,由同种原子形成共价键都是非极性共价键,简称非极性键 D、除之外的短周期主族非金属元素均满足:最高正价最低负价
-
15、为了纪念人类历史上那些做出过伟大科学成就的科学家,许多国家都发行过纪念他们的邮票。下列邮票中的科学家与其对应描述不相符的是( )A、拉瓦锡提出了第一个元素分类表
 B、门捷列夫编制了第一张元素周期表
B、门捷列夫编制了第一张元素周期表 C、卢瑟福提出了原子的有核模型
C、卢瑟福提出了原子的有核模型 D、维尔纳发现并证明原子序数等于核电荷数
D、维尔纳发现并证明原子序数等于核电荷数
-
16、下列化学用语或模型表示不正确的是( )A、保持干冰化学性质的最小微粒的结构模型:
 B、VIA族元素中非金属性最强元素的原子结构示意图:
B、VIA族元素中非金属性最强元素的原子结构示意图: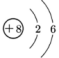 C、侯氏制碱法得到的可用作化肥的副产品的电子式:
C、侯氏制碱法得到的可用作化肥的副产品的电子式: D、天然气主要成分的分子结构式:
D、天然气主要成分的分子结构式:
-
17、2023年诺贝尔化学奖颁发给了研究量子点的三位科学家,其研究成果表明,物质在纳米级时因微粒大小不同而具有不同的颜色、性质,它们的研究在医疗、科技等多个领域有重大意义。下列叙述正确的是( )A、科学家研究过程中制得了直径为的CdS,这种CdS是一种胶体 B、利用丁达尔效应鉴别胶体和淀粉溶液 C、胶体区别于其他分散系的本质特征是分散质粒子直径为 D、可以通过渗析方法分离胶体和泥沙水的混合物
-
18、2023年入冬以来,呼吸道感染性疾病的发病率逐渐升高,为确保同学们的身体健康,学校要求各班每日做好通风、消杀工作。每日消杀所用“84消毒液”的有效成分为( )A、二氧化氯 B、次氯酸钠 C、次氯酸钙 D、过氧乙酸
-
19、钛酸钡是一种压电材料,主要用于电子陶瓷、PTC热敏电阻、电容器等多种电子元器件的制备。某工厂以重晶石为原料,生产的工业流程如下图:

已知常温下: , 。
回答下列问题:
(1)、为提高的酸浸速率,可采取的措施为(写出一条)。(2)、转化过程中溶液中钛元素在不同pH时主要以、、这三种形式存在(变化曲线如右图所示)。实际制备工艺中,先用氨水调节混合溶液的pH为 , 再进行转化,理由是。(3)、工业上用饱和溶液处理重晶石(假设杂质不与溶液作用),待达到平衡后,移走上层清液,重复多次操作,将转化为 , 此反应的平衡常数K=(填写计算结果)。若不考虑的水解,要使恰好完全转化为 , 则至少需要浓度为溶液mL。(4)、在隔绝空气条件下,煅烧草酸氧钛钡晶体时有两种气体(水蒸气除外)生成,该反应的化学方程式为。流程中用而不用其它酸的理由是。 -
20、三草酸合铁酸钾晶体(M=491g/mol)是一种感光剂和高效的污水处理剂,是制备负载型活性铁催化剂的主要原料,还可以作为一些有机反应的催化剂。
I.制备的途径如下,请回答下列问题:

研究小组通过查阅资料得知:
a.对光敏感,易溶于水,难溶于乙醇;
b.很多草酸盐(例如、)难溶于水,但能溶解于稀硝酸。
请回答:
(1)、步骤③中,控制水浴温度在40℃左右的原因为。(2)、关于制备流程,下列说法正确的是____A、步骤①为复分解反应,步骤③为氧化还原反应 B、步骤②判断是否洗涤干净,可以取少量最后一次洗涤液,加入氯化钡溶液,观察是否有白色沉淀产生 C、步骤④,加入乙醇目的在于降低的溶解度,使其结晶析出 D、步骤④⑤可以在日光下进行(3)、Ⅱ.测定三草酸合铁酸钾样品(含少量)的纯度,进行如下实验:步骤1:称取5.000g三草酸合铁酸钾晶体,配制成250mL溶液。
步骤2:取25.00mL溶液,用酸性溶液滴定至终点,消耗12.30mL。
步骤3:另取25.00mL溶液,加入过量Zn粉,将还原成 , 过滤,洗涤,将滤液和洗涤液合并。
步骤4:用酸性溶液滴定合并后溶液至终点,测得实验数据:
实验次数
滴定前读数/mL
滴定后读数/mL
1
0.10
14.90
2
0.52
14.82
3
0.00
16.66
4
0.30
14.10
步骤1中所需玻璃仪器除烧杯、玻璃棒、量筒外还有(填仪器名称)。
(4)、研究小组制得的纯度为。