相关试卷
-
1、用下列仪器或装置(夹持装置略)进行实验,不能达到实验目的的是( )
A
B
C
D




实验室制取氨气
分离碳酸钠溶液和乙酸乙酯
制备无水氯化镁
证明醋酸为弱酸
A、A B、B C、C D、D -
2、下列实验事实所对应的离子方程式不正确的是( )A、CO2溶于水产生HCO3-: CO2 + H2O H2CO3 HCO3- + H+ B、FeCl3溶液呈酸性: Fe3+ + 3H2O = Fe(OH)3↓ + 3H+ C、NO2溶于H2O红棕色消失: 3NO2 + H2O =2H+ + 2NO3- + NO D、向海带灰浸出液(含I-)中滴加几滴酸化的过氧化氢溶液:2I- + H2O2 + 2H+ =I2 + 2H2O
-
3、常温下,NH4Cl溶于水得到无色溶液,为使溶液中的c(NH4+) : c(Cl-) = 1:1,下列采取的措施正确的是( )A、加入适量的NaCl固体 B、加入适量的盐酸,抑制NH4+水解 C、加入适量的氨水,使溶液的pH等于7 D、加入适量的NaOH固体,使溶液的pH等于7
-
4、短周期元素G、M、W、X、Y、Z、Q的原子半径及其最高正化合价随原子序数递增的变化如图所示:

下列说法正确的是( )
A、熔点:M < Y B、第一电离能:X > W > G C、热稳定性: HQ > H2Z > HW D、酸性:HQO4 > H2ZO4 > H2YO3 -
5、用NA表示阿伏加德罗常数的值。下列说法正确的是( )A、常温下,0.1 mol NH3的体积为2.24 L B、1 mol HCCH分子中含有σ键的数目为 2 NA C、1 L 0.1 mol·L-1 Na2CO3溶液中CO32- 数目小于0.1 NA D、25℃时, pH=5的NH4Cl溶液中由水电离出的H+的浓度为10-9 mol·L-1
-
6、下列有关化学用语或图示表达正确的是( )A、二氧化硫的VSEPR模型:
 B、CO2的电子式:
B、CO2的电子式: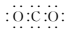 C、中子数为8的碳原子:814C
D、基态氧原子的轨道表示式:
C、中子数为8的碳原子:814C
D、基态氧原子的轨道表示式:
-
7、下列溶液中,酸碱性与其他三种不一致的是( )A、H2S溶液 B、NaHCO3溶液 C、K2S溶液 D、氨水
-
8、2022年2月,北京冬奥会秉承了创新、协调、绿色、开放、共享发展的理念。下列冬奥会使用的物品中,主要材料不属于有机高分子材料的是( )
A
B
C
D




冰墩墩中的聚酯纤维
速滑馆中的铝制幕墙
雪花花瓣中的聚碳酸酯
头盔表面的聚氨酯涂料
A、A B、B C、C D、D -
9、氮及其化合物在工农业生产中有着重要应用,减少氮的氧化物在大气中的排放是环境保护的重要内容之一。(1)、Ⅰ.和完全反应,每生成0.1 mol NO时,吸收8.9 kJ的热量,写出该反应的热化学方程式。
又知,一定条件下,用催化还原可消除NO污染。
kJ⋅mol
kJ⋅mol
则 kJ⋅mol。
(2)、一定温度下,向一体积不变的密闭容器中加入适量的和NO,发生上述反应,下列条件能判断该反应到达平衡状态的有____(填序号)。A、混合气体的平均相对分子质量不变 B、 C、单位时间里有4n mol断开同时有4n mol 断开 D、混合气体的压强不变 E、混合气体的密度不变(3)、80℃时,将0.40 mol ;气体充入2 L已经抽空的固定容积的密闭容器中发生反应 , 隔一段时间对该容器内的物质进行分析,得到如下数据:时间
0
20
40
60
80
100
/mol
0.40
a
0.20
c
d
e
/mol
0.00
0.24
b
0.52
0.60
0.60
①计算:mol。
②平衡后,向该容器中再充入0.2 mol 气体,平衡向移动。(填“正反应方向”或“逆反应方向”)。
(4)、Ⅱ.利用如图所示原理去除NO。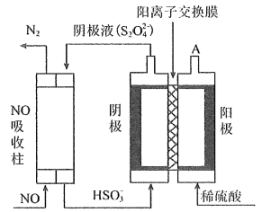
基态N原子中,电子占据的最高能级为能级,该能级轨道的形状为。电解池中阴极反应式为。
-
10、氨基甲酸铵()是一种白色固体,易溶于水和乙醇,难溶于。易分解、极易水解,可用作肥料、灭火剂、洗涤剂等。实验室用下图所
示装置制备氨基甲酸铵,已知有关反应原理:
 (1)、仪器E的名称为。(2)、装置F用于制备合成所需的原料气,写出实验室利用F制取该气体的化学反应方程式:。(3)、装置C、E中所盛的药品分别是、。(4)、装置D采用的是冰水浴,其原因是。(5)、如果将D中连接气球的导管改连装置G,则G装置能控制原料气按化学计量数充分反应。若反应初期观察到G装置内浓硫酸中产生气泡,应该(填“加快”、“减慢”或“不改变”)产生氨气的流速;此外,装置G还能(用字母选项填空)。
(1)、仪器E的名称为。(2)、装置F用于制备合成所需的原料气,写出实验室利用F制取该气体的化学反应方程式:。(3)、装置C、E中所盛的药品分别是、。(4)、装置D采用的是冰水浴,其原因是。(5)、如果将D中连接气球的导管改连装置G,则G装置能控制原料气按化学计量数充分反应。若反应初期观察到G装置内浓硫酸中产生气泡,应该(填“加快”、“减慢”或“不改变”)产生氨气的流速;此外,装置G还能(用字母选项填空)。A.吸收尾气中的氨气,防止污染
B.防倒吸
C.防止空气中的水蒸气进入反应器
(6)、已知氨基甲酸铵遇水可完全水解为碳酸氢铵,现取长期存放的样品4.69 g(内含杂质),用足量石灰水处理后,使样品中碳元素完全转化为碳酸钙,过滤、洗涤、干燥测得质量为6 g。求样品中氨基甲酸铵的质量分数为(计算结果保留2位有效数字)。
-
11、酮基布洛芬片是用于治疗各种关节肿痛以及牙痛、术后痛等的非处方药。其合成路线如图所示:
 (1)、A的化学名称为。(2)、B的分子式为。(3)、酮基布洛芬中官能团的名称为。(4)、写出C的结构简式:。(5)、写出D生成E的化学方程式:。(6)、H为酮基布洛芬的同分异构体,其分子结构中含有
(1)、A的化学名称为。(2)、B的分子式为。(3)、酮基布洛芬中官能团的名称为。(4)、写出C的结构简式:。(5)、写出D生成E的化学方程式:。(6)、H为酮基布洛芬的同分异构体,其分子结构中含有 的酯类化合物,写出任意一种H的结构简式。 (7)、参照上述合成路线,以
的酯类化合物,写出任意一种H的结构简式。 (7)、参照上述合成路线,以 和苯为原料(试剂任选),设计制备
和苯为原料(试剂任选),设计制备 的一种合成路线。
的一种合成路线。 -
12、太阳能电池的发展已经进入了第三代,即铜钢镓硒CIGs(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池。(1)、Si的原子结构示意图为 , 基态Cu原子的价电子排布式为。(2)、硒(Se)为第四周期元素,相邻的元素有砷(As)和溴(Br),则3种元素的第一电离能从大到小顺序为(用元素符号表示)。(3)、硫和碲与硒位于同主族,其简单氢化物和中,分解温度较高的是;键角较大的是 , 其原因是。(4)、β-MnSc的晶胞结构如图所示:

①β-MnSe中Mn的配位数为。
②若该晶体的晶胞参数为apm,阿伏加德罗常数的值为 , β-MnSe的密度g·cm(列出表达式即可)。
-
13、负载有Pt和Ag的活性炭,可选择性去除实现废酸的纯化,其工作原理如图。下列说法正确的是( )
 A、Ag作原电池正极 B、电子由Ag经活性炭流向Pt C、Pt表面发生的电极反应: D、每消耗标准状况下11.2 L的 , 最多去除1 mol Cl-
A、Ag作原电池正极 B、电子由Ag经活性炭流向Pt C、Pt表面发生的电极反应: D、每消耗标准状况下11.2 L的 , 最多去除1 mol Cl- -
14、0.1 mol/L 溶液的pH随温度的变化如图所示,下列说法正确的是( )
 A、温度高于60℃时,pH变化主要受水的电离平衡移动的影响 B、常温下: C、常温下: D、升高温度,平衡逆向移动
A、温度高于60℃时,pH变化主要受水的电离平衡移动的影响 B、常温下: C、常温下: D、升高温度,平衡逆向移动 -
15、自然界中时刻存在着氮的转化,下图为分子在催化剂作用下发生一系列转化示意图。

下列叙述正确的是( )
A、 , 均属于氮的固定 B、使用催化剂a、b均可以提高单位时间内生成物的产量 C、催化剂a、b表面均发生了极性共价键的断裂 D、在催化剂a作用下,氮原子发生了氧化反应 -
16、室温下,下列各组离子在指定溶液中一定不能大量共存的是( )A、与铝粉反应放出的透明溶液:、 , 、 B、常温下,由水电离的的溶液:、、 , C、使石蕊试液显红色的溶液:、、、 D、含有大量的溶液: , 、、、
-
17、下列说法正确的是( )A、石墨中的碳原子呈杂化,是混合型晶体 B、4.6 g乙醇分子中含有共价键数为(为阿伏加德罗常数) C、和结构相似,但硫化氢晶体中,一个周围有12个紧邻的分子,而冰中一个周围只有4个紧邻的分子 D、臭氧分子是非极性分子
-
18、用如图所示装置进行下列实验(尾气处理装置已省略),装置正确并能达到实验目的的是( )

选项
①中试剂
②中溶液
实验目的
A
浓硫酸、无水乙醇(沸石)
酸性高锰酸钾溶液
检验有乙烯气体生成
B
乙醇、乙酸、浓硫酸
氢氧化钠溶液
制取乙酸乙酯
C
Cu、浓硫酸
溴水
验证的还原性
D
澄清石灰水
验证的热稳定性
A、A B、B C、C D、D -
19、下列反应的离子方程式正确的是( )A、向氢氧化亚铁中加入足量的稀硝酸: B、泡沫灭火器原理: C、浓氨水中滴加少量硫酸铜溶液: D、澄清石灰水与过量反应:
-
20、下列有关有机物的说法中不正确的是( )A、属于取代反应 B、分子式为的有机物属于卤代烃 C、苯的二氯取代物有三种结构 D、分子组成上相差一个或若干个原子团的有机物之间一定互为同系物