相关试卷
-
1、Ⅰ肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气。已知:
①N2(g)+2O2(g)=N2O4(l) ΔH1=−19.5 kJ· mol−1
②N2H4(l)+O2(g)=N2(g)+2H2O(g) ΔH2=−534 kJ· mol−1
(1)、写出肼(l)和N2O4(l)完全反应生成N2和水蒸气时的热化学方程式:。(2)、已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O=O为500、N—N为154,O—H为462,则断裂1 mol N—H键所需的能量是 kJ。(3)、Ⅱ.一定条件下铁可以和CO2发生反应Fe(s)+CO2 (g)FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度变化与时间的关系如图所示。
t1 min时,反应速率的大小关系为v正 (CO2)v逆 (CO2 )(填“>”“<”或“=”)。
(4)、0~4min内,CO2的转化率为(保留三位有效数字) ,CO的平均反应速率为。(5)、下列选项能说明上述反应已达平衡状态的是____(填字母)。A、v(CO2)=v(CO) B、单位时间内生成n mol Fe的同时生成n mol FeO C、容器中气体压强不随时间的变化而变化 D、容器中CO2浓度不随时间的变化而变化(6)、燃料电池因具有发电效率高。环境污染少等优点而备受人们关注。用于笔记本电脑的甲醇(CH3OH)燃料电池示意图如下,a是极,此电极反应为。
-
2、氟化钾镁是一种具有优良光学性能的材料,主要应用于激光领域,其立方晶胞结构如图。表示阿伏加德罗常数的值。下列说法错误的是( )
 A、的配位数为12 B、若位于晶胞的体心,则位于晶胞的面心 C、每个位于距其最近且等距的构成的正四面体空隙中 D、若晶胞参数为a nm,则晶体的密度是
A、的配位数为12 B、若位于晶胞的体心,则位于晶胞的面心 C、每个位于距其最近且等距的构成的正四面体空隙中 D、若晶胞参数为a nm,则晶体的密度是 -
3、短周期主族元素W、X、Y、Z的原子序数依次增大,W的最高正价与最低负价代数和为0,W、X、Y形成的化合物甲的结构如图所示,Z原子M层上有2个未成对电子且此能级无空轨道。下列说法正确的是( )
 A、简单离子半径大小: B、简单氢化物的沸点: C、是由极性键构成的极性分子 D、甲中阴离子的空间构型为三角锥形
A、简单离子半径大小: B、简单氢化物的沸点: C、是由极性键构成的极性分子 D、甲中阴离子的空间构型为三角锥形 -
4、常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,其中心原子Cl为SP2杂化已被联合国卫生组织(WTO)列为Al级高效安全消毒剂,其中心原子Cl为SP2杂化。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠反应,其反应的化学方程式:CH3OH+6NaClO3+3H2SO4=CO2↑+6ClO2↑+3Na2SO4+5H2O,则下列说法错误的是( )A、CO2是非极性分子 B、键角:ClO3-<ClO2- C、CH3OH在反应中发生氧化反应 D、ClO2分子空间构型为V形
-
5、某科研人员提出HCHO与在羟基磷灰石(HAP)表面催化氧化生成 , 的历程,该历程示意图如图(图中只画出了HAP的部分结构)所示。下列说法正确的是( )
 A、HAP降低了该反应的焓变() B、反应过程中,发生了非极性键的断裂和生成 C、HCHO在反应过程中,无键发生断裂 D、和的中心原子上所含孤电子对数不同
A、HAP降低了该反应的焓变() B、反应过程中,发生了非极性键的断裂和生成 C、HCHO在反应过程中,无键发生断裂 D、和的中心原子上所含孤电子对数不同 -
6、观察下列模型并结合信息,判断有关说法错误的是( )
石英
FeSO4·7H2O
S8分子
HCN
结构模型示意图



 A、石英属于共价晶体,且两原子个数比为2:1 B、FeSO4·7H2O结构中键角1、2、3由大到小的顺序:3>1>2 C、固态硫S8中S原子为sp2杂化 D、HCN的结构式为
A、石英属于共价晶体,且两原子个数比为2:1 B、FeSO4·7H2O结构中键角1、2、3由大到小的顺序:3>1>2 C、固态硫S8中S原子为sp2杂化 D、HCN的结构式为 -
7、氨硼烷(NH3BH3)在一定条件下与水反应: , 的结构如图所示,已知H的电负性为2.1,B的电负性为2.0,下列说法正确的是( )
 A、NH3BH3分子中存在配位键,B原子提供孤电子对 B、1molNH3BH3发生反应时转移3mole- C、反应产物中只含有离子键、配位键和非极性共价键 D、反应过程中B原子的杂化方式由sp2变为sp3
A、NH3BH3分子中存在配位键,B原子提供孤电子对 B、1molNH3BH3发生反应时转移3mole- C、反应产物中只含有离子键、配位键和非极性共价键 D、反应过程中B原子的杂化方式由sp2变为sp3 -
8、下列有关化学用语表示正确的是( )A、
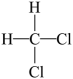 和
和 为同种物质
B、乙烷的结构式:
C、的电子式:
为同种物质
B、乙烷的结构式:
C、的电子式: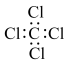 D、
D、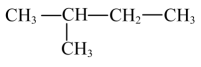 与
与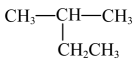 互为同分异构体
互为同分异构体
-
9、某有机物的结构如图所示,则下列说法中正确的是( )
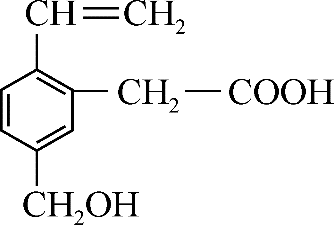 A、1mol该有机物能与2mol Na反应 B、该有机物能发生加成反应但不能发生取代反应 C、该有机物中有4种官能团 D、该有机物能使溴的四氯化碳溶液褪色,不能使酸性高锰酸钾溶液褪色
A、1mol该有机物能与2mol Na反应 B、该有机物能发生加成反应但不能发生取代反应 C、该有机物中有4种官能团 D、该有机物能使溴的四氯化碳溶液褪色,不能使酸性高锰酸钾溶液褪色 -
10、水生生物参与氮循环过程示意图如图所示。下列说法正确的是( )
 A、与分子中N原子的杂化类型、共价键类型均完全相同 B、反应②③⑥中N元素皆被氧化 C、与过程中转移电子的数目相同 D、水生生物的氮循环,既可以为其他生物提供营养物质,又可以减轻水体富营养化
A、与分子中N原子的杂化类型、共价键类型均完全相同 B、反应②③⑥中N元素皆被氧化 C、与过程中转移电子的数目相同 D、水生生物的氮循环,既可以为其他生物提供营养物质,又可以减轻水体富营养化 -
11、科学家已获得极具理论研究意义的N4分子,其结构为正四面体(如下图所示),与白磷分子相似。已知断裂1 mol N-N键吸收193 kJ热量 ,形成1 mol N≡N叁键放出941 kJ热量,则 ( )
 A、N4分子中的N是SP2杂化 B、N4是极性分子 C、N4和N2互为同分异构体 D、1 mol N4气体转化为N2时放出724 kJ 能量
A、N4分子中的N是SP2杂化 B、N4是极性分子 C、N4和N2互为同分异构体 D、1 mol N4气体转化为N2时放出724 kJ 能量 -
12、下列有关物质结构的表述正确的是( )A、次氯酸的电子式:
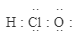 B、As(砷)的简化电子排布式:
C、铜原子价电子轨道表示式:
B、As(砷)的简化电子排布式:
C、铜原子价电子轨道表示式: D、的结构示意图:
D、的结构示意图:
-
13、下列说法错误的是( )A、基态Al原子核外电子的空间运动状态有7种 B、亚硫酸氢钠溶液显酸性的原因: C、中的键角小于中的键角 D、蒸干溶液并灼烧所得固体可最终得到
-
14、下列反应中,属于取代反应的是( )A、
 B、2CH3CH2OH+O22CH3CHO+2H2O
C、
B、2CH3CH2OH+O22CH3CHO+2H2O
C、 +H2CH3CH2OH
D、CH2=CH2+HClCH3CH2Cl
+H2CH3CH2OH
D、CH2=CH2+HClCH3CH2Cl
-
15、苏轼的《格物粗谈》有这样的记载:“红柿摘下未熟,每篮用木瓜三枚放入,得气即发,并无涩味。”按照现代科技观点,该文中的“气”是指( )A、甲烷 B、生长素 C、丁烷 D、乙烯
-
16、X、Y、Z、W、Q为短周期主族元素,原子序数依次增大且原子序数总和等于49.它们的化合物在常温下有如图所示的转化关系:
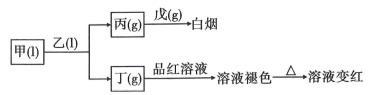
已知:乙、戊分子都含有10个电子,且两种分子中心原子的杂化方式均为杂化,乙中共价键的键角小于戊中共价键的键角。丙易溶于水,0.1mol/L丙的水溶液中,。甲为三种元素组成的化合物,其他化合物均为两种元素组成的化合物。试回答下列问题:
(1)、Q元素原子的简化电子排布式为。(2)、甲、乙、丙、丁、戊五种分子中,中心原子杂化方式为的是(填分子的化学式);乙中共价键的键角小于戊中共价键的键角的原因是。(3)、戊分子为分子(填“极性”或“非极性”),甲分子的VSEPR模型为。(4)、写出甲与乙反应的化学方程式:。(5)、下列说法正确的是____(填序号)。A、简单阴离子半径:W>Q B、常温下,0.1简单氢化物水溶液的pH:Q>W>Z>Y C、最高价氧化物对应水化物的酸性:Q>W D、化合物中含极性键、非极性键和离子键 E、甲与乙的化学反应中,甲作氧化剂 -
17、Cu及其化合物在医药、催化、材料等领域有广泛应用。回答下列问题:(1)、Cu元素与H元素可形成一种红色化合物,其晶体结构单元如图甲所示。则该化合物的化学式为。
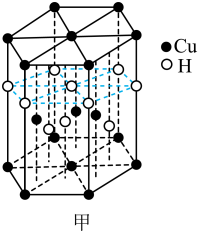 (2)、通过如图乙所示反应可以实现铜离子的富集,进行回收。
(2)、通过如图乙所示反应可以实现铜离子的富集,进行回收。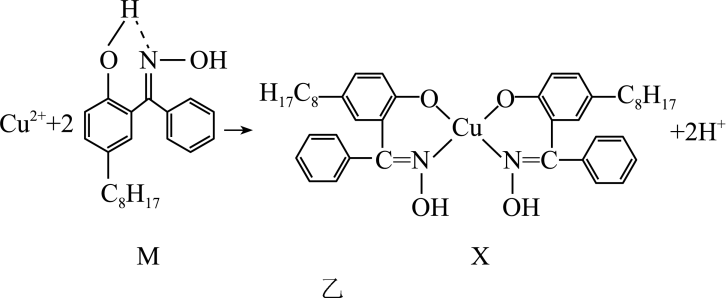
①基态铜原子的核外电子有种空间运动状态。与Cu元素同周期,基态原子有2个未成对电子的金属元素有种。
②下图a、b、c分别表示C、N、O和F的逐级电离能I变化趋势(纵坐标的标度不同)。第一电离能的变化图是(填序号),第三电离能的变化图是(填序号)。

③化合物X中的中心铜离子的配位数是 , 图乙反应中断裂和生成的化学键有(填序号)。
a.离子键 b.键 c.极性键 d.氢键 e.配位键
-
18、元素周期表前四周期W、X、Y、Z、E五种元素,W元素的原子最外层电子排布式为;X元素的原子价电子排布式为;Y元素位于第二周期且原子中p能级与s能级电子总数相等;Z元素原子的M能层的p能级中有3个未成对电子;中有5个未成对电子。(1)、写出元素名称:Z;E。(2)、Y基态原子的电子排布图为。(3)、当时,分子中,两共价键的键角为度;当时,X与Y形成的化合物与氢氧化钠溶液反应的离子方程式是。(4)、E元素原子的价电子排布式是 , 在元素周期表中的位置是 , 按照核外电子排布,可以把元素周期表分为5个区,E元素位于周期表的区。
-
19、根据所学知识回答下列问题(1)、下列所示的几种物质中,互为同素异形体的为 , 其中属于共价晶体的是 , 间的作用力是。
 (2)、气态通常以二聚体的形式存在,其空间结构如图甲所示,二聚体中Al的轨道杂化类型为。的熔点为1090℃,远高于的192℃,由此可以判断铝氟之间的化学键为键。结构属于立方晶系,晶胞如图乙所示,的配位数为。若晶胞参数为a pm,晶体密度(列出计算式,阿伏加德罗常数的值为)。
(2)、气态通常以二聚体的形式存在,其空间结构如图甲所示,二聚体中Al的轨道杂化类型为。的熔点为1090℃,远高于的192℃,由此可以判断铝氟之间的化学键为键。结构属于立方晶系,晶胞如图乙所示,的配位数为。若晶胞参数为a pm,晶体密度(列出计算式,阿伏加德罗常数的值为)。
-
20、为原子序数依次增大的前20号元素,它们最外层电子数之和为16,且W、同主族,X的基态原子有7种空间运动状态。下列叙述不正确的是( )A、第一电离能:W一定比同周期相邻的元素小 B、简单气态氢化物稳定性一定为: C、常见氧化物熔沸点:不一定高于 D、简单离子半径可能为: