相关试卷
-
1、镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型。NiMH中的M表示储氢金属或合金,该电池在充放电过程中的总反应方程式是: , 下列说法正确的是( )A、放电过程中负极MH得电子发生氧化反应 B、NiMH电池放电过程中,正极的电极反应式为 C、NiMH电池电子由负极→正极→电解质溶液→负极,形成闭合回路 D、NiMH电池可以用盐酸作为电解质溶液
-
2、下列关于浓硫酸的说法正确的是( )A、浓硫酸使蓝色胆矾变白体现了脱水性 B、浓硫酸不能干燥、HI、等强还原性化合物 C、蔗糖和浓硫酸的“黑面包”实验中,浓硫酸主要体现了脱水性和强氧化性 D、浓硫酸和碳单质在加热条件下反应,反应中浓硫酸既体现出酸性,又体现出氧化性
-
3、化学反应A+B→C(吸收能量)分两步进行:①A+B→X(放出能量),②X→C(吸收能量)。下列示意图中表示总反应过程中能量变化正确的图像是( )A、
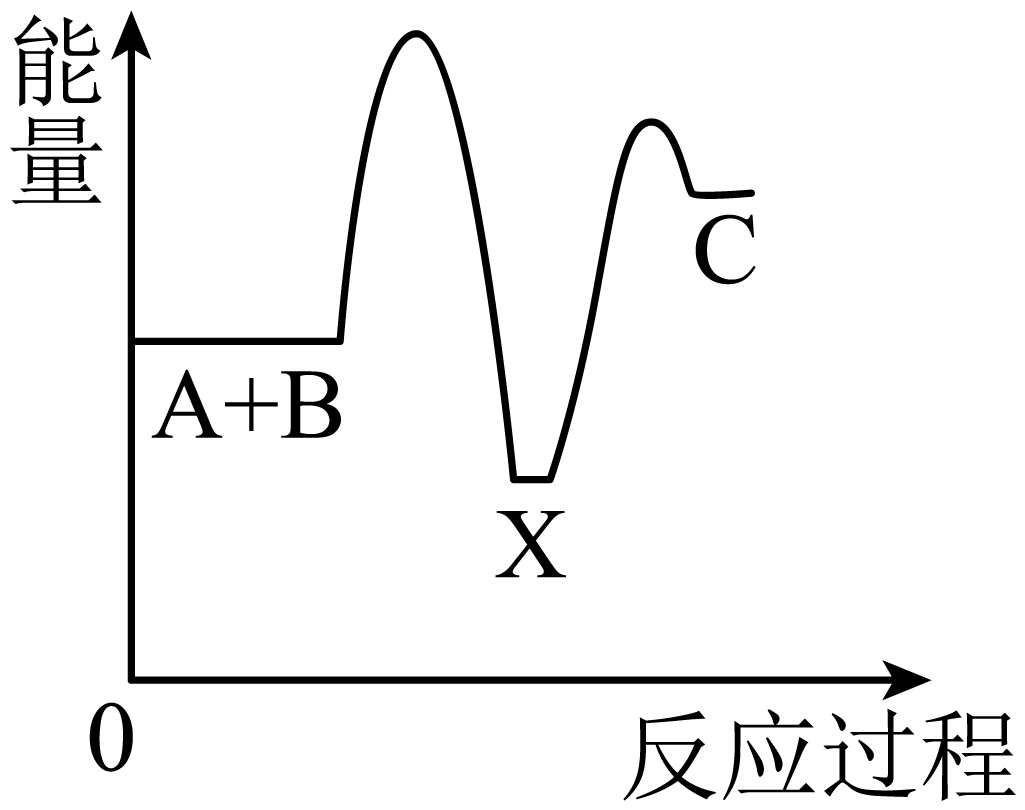 B、
B、 C、
C、 D、
D、
-
4、(NH4)2SO4在一定条件下发生如下反应: , 将反应后的气体通入一定量的BaCl2溶液中,发现溶液中有白色沉淀生成,还有部分气体从溶液中逸出,检验发现从溶液中逸出的气体无色、无味,溶液中氯化钡恰好完全反应。下列说法正确的是( )A、生成的沉淀中既有BaSO4、又有BaSO3 , 且约为 B、生成的沉淀中既有BaSO4、又有BaSO3 , 且约为 C、因为弱酸不能制强酸,所以该实验中反应后气体通入BaCl2溶液中只有BaSO4沉淀 D、从溶液中逸出的气体只有N2 , 最后留下溶液中溶质只有较多的NH4Cl
-
5、在无机非金属材料中,硅扮演着重要的角色。下列有关硅及其化合物的说法中正确的是( )A、制备粗硅的化学方程式为: B、硅胶可作瓶装药品的干燥剂及催化剂载体,是因为是酸性氧化物 C、既可以与NaOH溶液反应,又可以与HF溶液反应 D、青花瓷胎体的原料为高岭土[],若以氧化物形式可表示为
-
6、能与水反应生成次氯酸,可杀死新型冠状病毒等多种病毒。一种制备的原理为 , 装置如图所示。

已知:①的熔点为-116℃、沸点为3.8℃,具有强烈刺激性气味、易溶于水;②与有机物、还原剂接触或加热时会发生燃烧并爆炸。
下列说法中正确的是( )
A、装置②中盛装的试剂是浓硫酸,用来干燥 B、装置④与⑤之间可用橡胶管连接 C、易液化,装置⑤中的液氨只能冷凝 , 因此从装置⑤中逸出气体的主要成分是 D、通入干燥空气的目的是将生成的稀释,减小爆炸危险 -
7、下列各组离子或分子在给定条件的溶液中可能大量共存的是( )A、加入铝片有大量氢气产生的溶液中:、、、 B、在0.1mol/L的盐酸中:、、、 C、在强碱性溶液中:、、、 D、碱性无色溶液中:、、、
-
8、NA代表阿伏加德罗常数的值,以下说法正确的是( )A、将足量Zn与100mL18mol/L浓硫酸反应,生成224mL气体,转移电子为0.02NA B、在标准状况下,22.4LHF所含的原子总数为2NA C、1mol固体中含离子总数与1mol固体中含离子总数之比为 D、1mol(其中D代表重氢原子符号)中含有的中子数为10NA
-
9、下图是用于干燥、收集并吸收多余气体的装置,下列方案正确的是( )

选项
试剂X
收集气体
试剂Y
A.
碱石灰
氯化氢
水
B.
碱石灰
氨气
水
C.
五氧化二磷
二氧化硫
氢氧化钠溶液
D.
氯化钙
一氧化氮
氢氧化钠溶液
A、A B、B C、C D、D -
10、下列有关反应的离子方程式书写正确的是( )A、氯气溶于水: B、过量与“84”消毒液(有效成分NaClO)反应: C、向溶液中加入过量浓氨水: D、通入酸性高锰酸钾溶液:
-
11、少量锌粉与100mL的稀盐酸反应,为了加快此反应速率且不改变生成的总量,以下方法可行的是( )
①适当升高温度;②再加入100mL的稀盐酸;③加少量固体;④加入少量醋酸钠固体;⑤加几滴浓硫酸;⑥滴入几滴硫酸铜溶液。
A、①⑤ B、②③ C、①⑥ D、②④ -
12、下列各组反应(表中物质均为反应物)在反应刚开始时,放出H2的速率最大的是( )
选项
金属(粉末状)及其物质的量/mol
酸的浓度及体积
反应温度/℃
A.
Mg 0.1
8 mol∙L-1硝酸 10mL
30
B.
Mg 0.1
3 mol∙L-1盐酸 10mL
30
C.
Fe 0.1
6 mol∙L-1盐酸 10mL
30
D.
Mg 0.1
3 mol∙L-1硫酸 10mL
30
A、A B、B C、C D、D -
13、学习小组探究了铜的氧化过程及铜的氧化物的组成。回答下列问题:(1)、铜与浓硝酸反应的装置如下图,仪器A的名称为 , 装置B的作用为 , 若浓硝酸足量,C中反应的化学方程式为。
 (2)、铜与过量H2O2反应的探究如下:
(2)、铜与过量H2O2反应的探究如下: 实验②中Cu溶解的离子方程式为。实验②产生的气体为 , 产生该气体的原因为。(3)、用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,。X的化学式为。
实验②中Cu溶解的离子方程式为。实验②产生的气体为 , 产生该气体的原因为。(3)、用足量NaOH处理实验②新制的溶液得到沉淀X,元素分析表明X为铜的氧化物,提纯干燥后的X在惰性氛围下加热,mgX完全分解为ng黑色氧化物Y,。X的化学式为。 -
14、化学反应速率在生产、生活和科学研究中有重要意义。
Ⅰ.构成原电池能增大化学反应速率,甲、乙两个原电池装置如图所示:

回答下列问题:
(1)、若装置甲的溶液M为稀硫酸,两个电极采用镁棒和铝棒。①电极X的电极反应式为。
②该电池的正极是(填“镁棒”或“铝棒”),该电极产物W是(填化学式)。
(2)、若装置甲中两电极质量变化与时间的关系如图所示,其中一个电极为Ag电极,则该电池的电解质溶液为(填化学式)溶液,电极X为(填字母)
a.Fe电极 b.Mg电极 c.Cu电极 d.Al电极
(3)、Ⅱ.一定温度下,在4 L密闭容器内进行的某一反应(该反应仅涉及两种物质),气体M、气体N的物质的量随时间变化的曲线如图所示。
t2 min时,v(正)(填“>”“<”或“=”)v(逆)。
(4)、若t1=2,则0~2 min内,M的平均反应速率v(M)=。(5)、t3 min时,反应物的转化率为。 -
15、物质的类别和核心元素化合价是研究物质性质的两个重要维度。硫及其部分化合物的“价-类”二维图如图所示,回答下列问题:
 (1)、甲的化学式为;其水溶液在空气中放置容易变浑浊,该反应的化学方程式为。(2)、通入气体乙可使酸性高锰酸钾溶液褪色,说明乙具有性;实验中可用足量的NaOH溶液吸收气体乙,防止污染空气,该反应的离子方程式为。(3)、某同学在用锌与丙的稀溶液反应制H2时,为了加快反应速度,将丙的稀溶液换成浓溶液,该同学的方案(填“合理”或“不合理”),理由是。(4)、丁的钠盐在空气中容易变质,检验其是否变质的方法是。(5)、已知酸性条件下K2Cr2O7能被丁还原为Cr3+ , 24 mL 0.05 mol•L-1 的丁溶液与0.02 mol•L-1的K2Cr2O7溶液恰好反应,则消耗K2Cr2O7溶液的体积为mL。
(1)、甲的化学式为;其水溶液在空气中放置容易变浑浊,该反应的化学方程式为。(2)、通入气体乙可使酸性高锰酸钾溶液褪色,说明乙具有性;实验中可用足量的NaOH溶液吸收气体乙,防止污染空气,该反应的离子方程式为。(3)、某同学在用锌与丙的稀溶液反应制H2时,为了加快反应速度,将丙的稀溶液换成浓溶液,该同学的方案(填“合理”或“不合理”),理由是。(4)、丁的钠盐在空气中容易变质,检验其是否变质的方法是。(5)、已知酸性条件下K2Cr2O7能被丁还原为Cr3+ , 24 mL 0.05 mol•L-1 的丁溶液与0.02 mol•L-1的K2Cr2O7溶液恰好反应,则消耗K2Cr2O7溶液的体积为mL。 -
16、高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
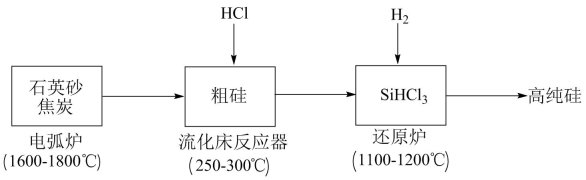 (1)、工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为。当有 1molC参与反应时,该反应转移的电子数是。(2)、有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和。
(1)、工业上用石英砂和过量焦炭在电弧炉中高温加热生成粗硅的化学方程式为。当有 1molC参与反应时,该反应转移的电子数是。(2)、有关物质的熔沸点数据如下表,提纯SiHCl3的主要工艺操作依次是沉降、冷凝和。物质
Si
SiCl4
SiHCl3
SiH2Cl2
SiH3Cl
HCl
SiH4
熔点/℃
1410
-70.4
-126.5
-122
-118
-114.2
-185
沸点/℃
2355
57.6
31.8
8.2
-30.4
-84.9
-111.9
(3)、还原炉中发生的化学反应方程式为:。(4)、上述工艺生产中循环使用的物质除Si、SiHCl3外,还有。(5)、工艺师常用氢氟酸来雕刻玻璃,该反应的化学方程式为。(6)、若还原炉中有氧气混入,会造成的不良后果有(答一点即可)。 -
17、某小组模拟工业制备NH4SCN,其原理是: , 其中不合理的是( )




A.制备氨气
B.观察氨气流速
C.制备
D.尾气处理
A、A B、B C、C D、D -
18、下列关于硅元素及其化合物的说法正确的是( )A、陶瓷是以黏土和石灰石作为原料,经高温烧结而成的 B、因SiO2能导电,故SiO2可用来生产光导纤维 C、碳化硅可用作耐高温结构材料、耐高温半导体材料 D、瓷坩埚及石英坩埚能与氢氟酸接触,也能对苛性碱和碳酸钠进行熔融操作
-
19、CF1107是一种离子液体,有良好的光学性能,是电子、半导体、显示行业的理想材料。其阴离子(结构如图所示)由X、Y、Z、W、M五种原子序数依次增大的短周期元素构成,其中X、Y、Z、W同周期,Z与M同主族,下列有关说法正确的是( )
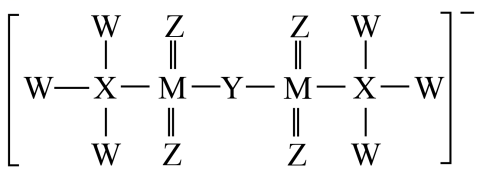 A、最高正价:W>M>Y>X B、简单氢化物稳定性:W>M C、含氧酸的酸性:M>Y>X D、Z与M组成的常见化合物均能使品红溶液褪色
A、最高正价:W>M>Y>X B、简单氢化物稳定性:W>M C、含氧酸的酸性:M>Y>X D、Z与M组成的常见化合物均能使品红溶液褪色 -
20、实验室探究SO2和Fe(NO3)3溶液反应的原理,装置如图,实验中Y装置产生白色沉淀。下列说法错误的是( )
 A、滴加浓硫酸之前应进行的操作是打开弹簧夹,通入N2一段时间 B、Y中产生的白色沉淀是BaSO4 C、在X装置中浓硫酸体现氧化性和酸性 D、若将Fe(NO3)3换成氨水,Y中能产生白色沉淀
A、滴加浓硫酸之前应进行的操作是打开弹簧夹,通入N2一段时间 B、Y中产生的白色沉淀是BaSO4 C、在X装置中浓硫酸体现氧化性和酸性 D、若将Fe(NO3)3换成氨水,Y中能产生白色沉淀