相关试卷
-
1、用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O22Cl2+2H2O
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.
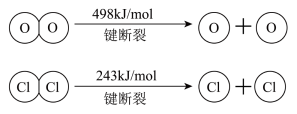 (1)、H2O的电子式是。(2)、反应A的热化学方程式是(注意:不写条件)。(3)、断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)。(4)、请回答:
(1)、H2O的电子式是。(2)、反应A的热化学方程式是(注意:不写条件)。(3)、断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)。(4)、请回答:参加反应的物质及状态
1mol分子中的化学键断裂时需要吸收的能量
436
a
369
H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1 , 蒸发1mol Br2(1)需要吸收的能量为30kJ,则上表中a的数值为:。
(5)、已知甲烷的燃烧热为890.3kJ·mol-1 , H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1 , N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1 , 则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=。(6)、二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:①2H2(g)+O2(g)=2H2O(g) = -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) =-1366.8kJ·mol-1
③H2O(l)=H2O(g) =+44.0kJ·mol-1
则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:。
-
2、有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6mol/L的H2SO4溶液中,乙同学将电极放入6mol/L的NaOH溶液中,如图所示。
 (1)、甲中SO移向(填“铝片”或“镁片”),写出甲中正极的电极反应式。(2)、乙中负极为(填“铝片”或“镁片”),写出正极的电极反应式式:。(3)、铅蓄电池中,正极材料为PbO2 , 负极材料为Pb,电解液为硫酸,放电时其正极反应式为。(4)、如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
(1)、甲中SO移向(填“铝片”或“镁片”),写出甲中正极的电极反应式。(2)、乙中负极为(填“铝片”或“镁片”),写出正极的电极反应式式:。(3)、铅蓄电池中,正极材料为PbO2 , 负极材料为Pb,电解液为硫酸,放电时其正极反应式为。(4)、如图为氢氧燃料电池的工作原理示意图,a、b均为惰性电极。
①使用时,空气从口通入(填“A”或“B”)。电流由流向(填“a”或“b”)。其总反应方程式为 , 在碱性条件下,负极反应式为。
(5)、直接乙醇燃料电池()具有很多优点。现有以下三种乙醇燃料电池。
①碱性乙醇燃料电池中,电极a上发生的电极反应式为。
②酸性乙醇燃料电池中,电极a上发生的电极反应式为。
③熔融碳酸盐乙醇燃料电池中,电极b上发生的电极反应式为。
(6)、某同学设计如图的原电池,负极实验现象为 , 则正极的电极反应式为: , 当导线中有3.01×1023个电子流过,溶液质量变化为g。
-
3、某研究小组用如图装置制取SO2并对其性质进行相关实验(部分夹持装置已略去)。
 (1)、装置A用于制取SO2 , 发生反应的化学方程式为。(2)、将B中FeCl3溶液换成KMnO4酸性溶液也能达到检验SO2性质的目的,根据氧化还原反应配平其方程式:(3)、C中观察到的现象是;B、C、D三支试管中的现象分别体现了SO2的性、性和漂白性。(4)、装置D中的实验目的是探究SO2与品红作用的可逆性,请写出实验操作及现象。(5)、尾气处理时将气体通入溶液。终止反应,冷却溶液后将装置A中Y型试管倾斜,使(填“左”或“右”,下同)侧的物质全部转移到侧,这时看到溶液的颜色为色。
(1)、装置A用于制取SO2 , 发生反应的化学方程式为。(2)、将B中FeCl3溶液换成KMnO4酸性溶液也能达到检验SO2性质的目的,根据氧化还原反应配平其方程式:(3)、C中观察到的现象是;B、C、D三支试管中的现象分别体现了SO2的性、性和漂白性。(4)、装置D中的实验目的是探究SO2与品红作用的可逆性,请写出实验操作及现象。(5)、尾气处理时将气体通入溶液。终止反应,冷却溶液后将装置A中Y型试管倾斜,使(填“左”或“右”,下同)侧的物质全部转移到侧,这时看到溶液的颜色为色。 -
4、已知某化学反应A2(g)+2B2(g)=2AB2(g),能量变化如图所示,下列叙述中正确的是( )
 A、该反应的进行一定需要加热或点燃 B、该反应若生成2molAB2(g)时,放出的热量为(E1-E2)kJ C、物质AB2比A2更稳定 D、该反应断开化学键吸收的总能量大于形成化学键释放的总能量
A、该反应的进行一定需要加热或点燃 B、该反应若生成2molAB2(g)时,放出的热量为(E1-E2)kJ C、物质AB2比A2更稳定 D、该反应断开化学键吸收的总能量大于形成化学键释放的总能量 -
5、各相关物质的燃烧热数据如下表。下列热化学方程式正确的是( )
物质
A、 B、 C、2H2O(l)=2H2(g)+O2(g) D、 -
6、科学家设计出质子膜H2S燃料电池,实现了利用H2S废气资源回收能量并得到单质硫。质子膜H2S燃料电池的结构示意图如图所示。下列说法不正确的是( )
 A、电极a为电池的负极 B、电极b上发生的电极反应为:O2+4H++4e−=2H2O C、电路中每流过2 mol电子,在正极消耗22.4LH2S D、每34 g H2S参与反应,有2molH+经质子膜进入正极区
A、电极a为电池的负极 B、电极b上发生的电极反应为:O2+4H++4e−=2H2O C、电路中每流过2 mol电子,在正极消耗22.4LH2S D、每34 g H2S参与反应,有2molH+经质子膜进入正极区 -
7、某兴趣小组设计的原电池如图所示,下列说法正确的是( )
 A、Cu电极为负极,发生氧化反应 B、电池工作时,电子从Zn电极经电解质溶液流向Cu电极 C、当Zn电极质量减少65g时,Cu电极生成22.4LH2 D、放电过程中,从左向右移动
A、Cu电极为负极,发生氧化反应 B、电池工作时,电子从Zn电极经电解质溶液流向Cu电极 C、当Zn电极质量减少65g时,Cu电极生成22.4LH2 D、放电过程中,从左向右移动 -
8、化学反应与能量变化对人类生产、生活有重要的意义,下列说法正确的是( )
 A、图1装置可以用于探究一个反应是吸热反应还是放热反应 B、能量变化如图2的反应必须加热才能发生反应 C、常温常压下,断开1molH2中的化学键吸收436kJ的能量,断开1molCl2中的化学键吸收243kJ的能量,形成2molHCl中的化学键释放862kJ的能量,故H2和Cl2反应释放能量 D、一定条件下,石墨转化为金刚石要吸收能量,故金刚石比石墨稳定
A、图1装置可以用于探究一个反应是吸热反应还是放热反应 B、能量变化如图2的反应必须加热才能发生反应 C、常温常压下,断开1molH2中的化学键吸收436kJ的能量,断开1molCl2中的化学键吸收243kJ的能量,形成2molHCl中的化学键释放862kJ的能量,故H2和Cl2反应释放能量 D、一定条件下,石墨转化为金刚石要吸收能量,故金刚石比石墨稳定 -
9、下列有关离子方程式正确的是( )A、NO2通入水中: B、向Na2SO4溶液中滴加BaCl2溶液: C、SiO2与NaOH制Na2SiO3: D、室温下用稀HNO3溶解Cu:
-
10、高纯硅是现代信息、半导体和光伏发电等产业都需要的基础材料。工业上提纯硅有多种路线,其中一种工艺流程如图:

下列说法正确的是( )
A、硅在自然界中主要以游离态形式存在 B、电弧炉中的反应为SiO2+CSi+CO2↑ C、还原炉中,理论上得到的氧化产物与还原产物的物质的量之比为1:3 D、(沸点31.5℃)中含有少量的(沸点57.6℃),通过蒸馏可提纯 -
11、细菌可以促使铁、氮两种元素进行氧化还原反应,并耦合两种元素的循环。耦合循环中的部分转化如图所示,下列说法错误的是( )
 A、上图所示氮循环中,N2转化为氨态氮属于氮的固定 B、氨气是生产氮肥的主要原料,工业上用氮气和氢气合成氨 C、反硝化过程中,含氮物质发生氧化反应 D、硝化过程中,含氮物质发生氧化反应
A、上图所示氮循环中,N2转化为氨态氮属于氮的固定 B、氨气是生产氮肥的主要原料,工业上用氮气和氢气合成氨 C、反硝化过程中,含氮物质发生氧化反应 D、硝化过程中,含氮物质发生氧化反应 -
12、表示阿伏加德罗常数的值,下列说法正确的是( )A、标准状况下,将2molNO和1molO2混合后,体系中的分子总数为2NA B、常温下,1molFe与足量的浓硫酸充分反应,转移电子数为2NA C、1molSiO2可溶于水生成1molH2SiO3 D、向50mL18mol/L的硫酸中加入足量的铜片并加热,被还原的硫酸物质的量小于0.45mol
-
13、下列说法中正确的是( )A、物质发生化学反应时都伴随着能量变化,伴随能量变化的物质变化也一定是化学变化 B、需要加热的化学反应一定是吸热反应,不需要加热就能进行的反应一定是放热反应 C、吸热反应就是反应物的总能量比生成物的总能量高;也可以理解为化学键断裂时吸收的能量比化学键形成时放出的能量多 D、因为3O2=2O3是吸热反应,所以臭氧比氧气的化学性质更活泼
-
14、下列说法不正确的是( )A、玻璃、水泥、陶瓷是三大传统的无机非金属材料 B、SO2既可用于漂白纸浆,又可用于杀菌、消毒 C、中国天眼传输信息用的光纤材料的主要成分是Si D、因为铁在浓硫酸中会钝化,所以可以用铁罐盛放热的浓硫酸
-
15、化学与生活息息相关,下列说法正确的是( )A、二氧化硫具有漂白作用,工业上常用来漂白纸浆、毛、丝、食品等 B、氨气易液化,液氨汽化时要吸收大量的热,因此液氨可用作制冷剂 C、混泥土的使用十分广泛,其中生产普通的硅酸盐水泥的主要原料是石英砂 D、华为公司自主研发麒麟990芯片采用7nm工艺,芯片的主要成分是二氧化硅
-
16、碳中和是指企业、团体或个人在一定时间内直接或间接产生的温室气体排放总量,通过植树造林、节能减排等形式,抵消自身产生的二氧化碳排放量,实现二氧化碳“零排放”。二氧化碳和氢气按一定的体积比混合,在一定条件下可以制得烯烃,该技术已经成为节能减碳实现“零排放”的有效途径之一。如图是合成橡胶和TNT的路线。

回答下列问题:
(1)、TNT的结构简式为。(2)、写出反应①的化学方程式;烯烃B与Cl2反应的化学反应方程式。
(3)、C8H9Cl含有的官能团的名称为;E的结构简式为;反应②反应类型。 -
17、Ⅰ.某有机化合物A经李比希法测得其中含碳元素为70.6%、含氢元素为5.9%,其余为氧元素。现用下列方法测定该有机化合物的相对分子质量和确定分子结构。
方法一:用质谱法分析得知的质谱图如图所示。方法二:核磁共振仪测出的核磁共振氢谱如图所示。
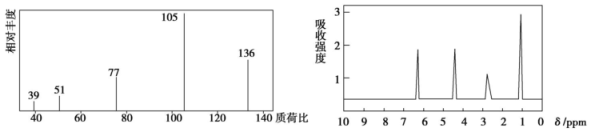
方法三:利用红外光谱仪测得分子的红外光谱,如图所示。

已知:A分子中苯环上只有一个取代基,试回答下列问题。
(1)、A的分子式为。其有种化学环境不同的氢原子。(2)、A的结构简式为 , 与A互为同分异构体,且含有相同官能团的芳香族化合物共有种。(3)、Ⅱ.已知:烯烃与酸性溶液反应时,不同的结构可以得到不同的氧化产物。烯烃被酸性高锰酸钾溶液氧化时的对应产物如下: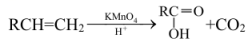
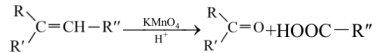
若某烯烃分子式为 , 与酸性溶液反应后只生成一种有机化合物,则该烯烃可能的结构简式为。
(4)、请写出 被酸性溶液氧化后的产物。 (5)、Ⅲ.共轭二烯烃及其衍生物可以与含碳碳不饱和键的化合物进行如下反应。例如:
被酸性溶液氧化后的产物。 (5)、Ⅲ.共轭二烯烃及其衍生物可以与含碳碳不饱和键的化合物进行如下反应。例如: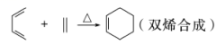
合成
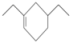 的原料为、(键线式表示)。(6)、请写出
的原料为、(键线式表示)。(6)、请写出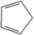 与
与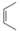 反应方程式为。
反应方程式为。 -
18、铁是地球上分布最广泛的金属之一,约占地壳质量的 , 仅次于氧、硅、铝,位居地壳含量第四位。蛋白琥珀酸铁口服液可以用来治疗缺铁性贫血的治疗。请回答以下相关问题:(1)、写出基态铁原子的价层电子排布式。(2)、给出蛋白琥珀酸铁含有的三种元素的第一电离能从小到大排序 , 并解释原因。(3)、将三种元素最简单氢化物按照键角从大到小排序(4)、已知在元素周期表中位于同主族,将这四种元素的最简单氢化物按照沸点从大到小排序。(5)、金属羰基化合物在催化反应中有着重要的作用,其本质是金属原子与一氧化碳中的碳原子形成配位键。金属原子在形成最稳定的羰基化合物时要遵守18电子规则,即每个金属原子的价层都满足18电子结构。若金属价层电子数为奇数,则可以通过两个金属原子之间形成共价单键实现价层电子数为偶数。根据以上信息,写出原子最稳定的羰基化合物的分子式。(6)、铁有多种同素异形体,在范围内,铁以面心立方最密堆积存在,如图为面心立方堆积的铁的晶胞。已知铁的摩尔质量为 , 铁原子的半径为 , 给出铁晶胞密度的表达式。

-
19、请按要求回答下列问题:(1)、某炔烃与氢气加成后的产物结构简式为
 , 则的系统命名为。有机物B中共有个手性碳原子。 (2)、写出反式聚-1,3-丁二烯的结构简式。(3)、已知物质的产量是衡量一个国家石油化工水平的标志。请写出利用得到乙醇的化学方程式: , 反应类型为:。(4)、请写出用乙炔作原料制备聚氯乙烯过程中发生加聚反应的化学方程式:。(5)、某烷烃的相对分子质量为114,与溴单质发生取代反应所得的一溴代物只有一种。写出该取代反应的化学方程式:。
, 则的系统命名为。有机物B中共有个手性碳原子。 (2)、写出反式聚-1,3-丁二烯的结构简式。(3)、已知物质的产量是衡量一个国家石油化工水平的标志。请写出利用得到乙醇的化学方程式: , 反应类型为:。(4)、请写出用乙炔作原料制备聚氯乙烯过程中发生加聚反应的化学方程式:。(5)、某烷烃的相对分子质量为114,与溴单质发生取代反应所得的一溴代物只有一种。写出该取代反应的化学方程式:。 -
20、对石油重油的加工利用是石化工业中非常重要的一种资源综合开发利用项目,不仅可以减少重油对环境的危害,同时可以获得很多重要的化工原料。以下是利用重油合成一些有机物的基本合成路线:

下列说法错误的是( )
A、A为乙烯,①为加成反应 B、已知C为 , ②为加成反应 C、可用酸性高锰酸钾溶液鉴别和苯 D、中含有的官能团为硝基和羧基