相关试卷
-
1、检验黑木耳中铁离子的步骤为:灼烧黑木耳→加酸溶解→过滤→取滤液检验,所选择的装置(夹持装置已略去)或操作不正确的是( )




A.灼烧黑木耳
B.加酸后搅拌溶解
C.过滤得滤液
D.检验铁离子
A、A B、B C、C D、D -
2、化学既神奇又美丽。下列说法正确的是( )A、冬天飞舞的雪花,水分子之间通过O-H键结合形成晶体 B、金刚石中碳原子之间通过C-C键形成空间网状结构 C、CuSO4溶液中加入过量浓氨水得到深蓝色溶液,Cu(OH)2溶液为深蓝色 D、碘升华得到紫色碘蒸气,升华过程破坏了碘分子之间的氢键
-
3、利用反应可制备化工试剂 . 下列说法正确的是( )A、的电子式为 B、基态原子的价电子排布图为
 C、为共价化合物
D、的VSEPR模型为平面三角形
C、为共价化合物
D、的VSEPR模型为平面三角形
-
4、中华文明源远流长,化学与文化传承密不可分。下列物质主要由合金材料制成的是( )




A.裴李岗文化骨笛
B.走马楼简牍
C.商朝后期陶埙
D.曾侯乙青铜编钟
A、A B、B C、C D、D -
5、比哌立登是一种抗震颤麻痹药,可用于轻型帕金森综合症的治疗。其合成路线如图:

回答下列问题:
(1)、C中官能团的名称为。(2)、A→C的化学反应方程式为。(3)、D与G合成H的反应类型为。(4)、根据物质结构知识判断沸点:
 (填“>”或“<”)。 (5)、J是C的同分异构体,J能与FeCl3发生显色反应,符合条件的J有种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:3:6的结构简式为(写一种即可)。(6)、参照上述合成路线,以1,3-丁二烯和
(填“>”或“<”)。 (5)、J是C的同分异构体,J能与FeCl3发生显色反应,符合条件的J有种,其中核磁共振氢谱显示4组峰,且峰面积之比为1:2:3:6的结构简式为(写一种即可)。(6)、参照上述合成路线,以1,3-丁二烯和 主要原料,设计
主要原料,设计 的合成路线(无机试剂和含有三个碳原子以下的有机试剂任选)。
的合成路线(无机试剂和含有三个碳原子以下的有机试剂任选)。 -
6、低碳烯烃是基础有机化工原料,工业上可利用合成气直接或间接制取。主要反应方程式如下。
间接制取低碳烯烃:CO(g)+2H2(g)CH3OH(l) △H1=-116kJ•mol-1
2CH3OH(l) C2H4(g)+2H2O(l) △H2=-35kJ•mol-1
直接制取低碳烯烃:2CO(g)+4H2(g) C2H4(g)+2H2O(g) △H3
回答下列问题:
(1)、已知H2O(g) H2O(l) △H=-44kJ•mol-1 , 则△H3=kJ/mol。(2)、将N2、CO和H2以体积比为1:1:2充入密闭容器中直接制取乙烯,CO的平衡转化率与温度的关系如图1所示,则P1P2(填“>”“<”或“=”),M点的正反应速率N点的逆反应速率(填“>”“<”或“=”)。在500K,压强为P1的条件下,该反应的Kp=(列出计算式)。 (3)、已知反应空速是指一定条件下,单位时间单位体积(或质量)催化剂处理的气体量。在常压、450℃,n(CO):n(H2)为1:2的条件下,利用合成气直接制取乙烯。反应空速对CO转化率和乙烯选择性[选择性=×100%]的影响如图2所示。随着反应空速的增加,乙烯的选择性先升高后降低的原因是。
(3)、已知反应空速是指一定条件下,单位时间单位体积(或质量)催化剂处理的气体量。在常压、450℃,n(CO):n(H2)为1:2的条件下,利用合成气直接制取乙烯。反应空速对CO转化率和乙烯选择性[选择性=×100%]的影响如图2所示。随着反应空速的增加,乙烯的选择性先升高后降低的原因是。 (4)、利用合成气制取低碳烯烃时,需使合成气吸附在催化剂表面的活性位点上。研究发现催化剂晶体的颗粒越小,催化效果越好,其理由是。(5)、Ga2O3是工业上利用合成气制低碳烯烃的催化剂,其晶体结构单元如图3所示(O2-之间紧密堆积,Ga3+位于O2-形成的空隙中且未画出),其中O2-半径为anm,晶体结构单元的高为bnm。已知阿伏加德罗常数的值为NA , 则Ga2O3晶体的摩尔体积Vm=m3/mol。
(4)、利用合成气制取低碳烯烃时,需使合成气吸附在催化剂表面的活性位点上。研究发现催化剂晶体的颗粒越小,催化效果越好,其理由是。(5)、Ga2O3是工业上利用合成气制低碳烯烃的催化剂,其晶体结构单元如图3所示(O2-之间紧密堆积,Ga3+位于O2-形成的空隙中且未画出),其中O2-半径为anm,晶体结构单元的高为bnm。已知阿伏加德罗常数的值为NA , 则Ga2O3晶体的摩尔体积Vm=m3/mol。
-
7、苯胺是一种无色油状液体,主要用于制造染料、药物和树脂等。利用水蒸气蒸馏法分离提纯粗苯胺(杂质为难以气化的物质)的装置如图所示。

实验操作:将粗苯胺加入仪器B中,向仪器A中加水,打开F,加热仪器A使水沸腾。同时对仪器B进行预热,关闭F,让水蒸气导入蒸馏装置,通入冷凝水,开始蒸馏。
回答下列问题:
(1)、仪器C的名称是;仪器E的作用是。(2)、如果加热A一段时间后发现漏加沸石,应该采用的补救操作是。(3)、水蒸气冷凝放热较多,为了提高冷凝效果可采取的措施是。(4)、蒸馏至时可停止蒸馏。(5)、将D中苯胺分离出来,需要用到的玻璃仪器有。(6)、已知混合物的蒸气总压等于外界大气压时,混合物开始沸腾。混合气体的总压等于各气体的分压之和,各气体的分压之比等于它们的物质的量之比。苯胺与水共沸时,苯胺的分压为5.6kPa,水蒸气的分压为95.7kPa,理论上每蒸出1g水同时蒸出苯胺的质量为g(计算结果保留2位有效数字);苯胺微溶于水,使水的蒸气压降低,则实际蒸出苯胺的质量(“偏大”“偏小”或“不变”)。 -
8、高锰酸钾在化工生产和环境保护等领域应用十分广泛。以软锰矿(主要成分是MnO2 , 含有Fe2O3和SiO2等杂质)为原料制备高锰酸钾的工艺流程如图:

回答下列问题:
(1)、基态Mn原子的价电子轨道表示式为。(2)、“焙烧”中有K2MnO4生成,该步骤主要反应的化学方程式为。(3)、若“焙烧”时未加入KClO3 , “水浸”后所得溶液中也含有K2MnO4 , 原因可能是。(4)、“水浸”时需要加热,其目的是。(5)、“滤渣2”含有MnO2和 , “歧化”过程中主要反应的离子方程式为。(6)、KMnO4可通过电解K2MnO4溶液的方法直接制得,相比“歧化法”,电解法的优点是。 -
9、实验测得0.1mol/LNaHCO3溶液的pH随温度升高的变化如图所示。

下列说法正确的是( )
A、由a点可知Ka1(H2CO3)•Ka2(H2CO3)>Kw B、a→b,HCO的水解程度减小 C、b→c,可能发生反应:2HCOCO+CO2↑+H2O D、a点溶液和d点溶液的c(OH-)相同 -
10、一水硫酸四氨合铜[Cu(NH3)4SO4•H2O]是一种易溶于水的晶体,可作高效安全的广谱杀菌剂,实验室制备流程如图:

下列说法错误的是( )
A、铜屑表面的油污可通过“碱煮水洗”去除 B、过程③中蓝色沉淀溶解,溶液变为绿色 C、过程④中加入的“溶剂X”可以是乙醇 D、玻璃棒摩擦的目的是加快结晶速率 -
11、已知反应S2O(aq)+2I-(aq)2SO(aq)+I2(aq),若起始向反应体系中加入含Fe3+的溶液,反应机理如图所示。下列说法正确的是( )
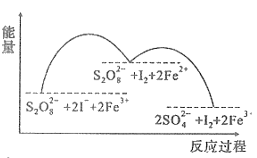 A、S2O中硫元素显+7价 B、反应速率与Fe3+浓度无关 C、由图可知氧化性:Fe3+>S2O D、若不加Fe3+ , 正反应的活化能比逆反应的小
A、S2O中硫元素显+7价 B、反应速率与Fe3+浓度无关 C、由图可知氧化性:Fe3+>S2O D、若不加Fe3+ , 正反应的活化能比逆反应的小 -
12、科学家近年发明了一种新型光电催化装置,它能将葡萄糖和CO2转化为甲酸盐,如图所示。光照时,光催化电极a产生电子(e-)和空穴(h+),图中的双极膜中间层中的H2O会解离产生H+和OH-。

下列说法错误的是( )
A、光催化电极a的反应为C6H12O6+12h++18OH-=6HCOO-+12H2O B、双极膜中间层中的H+在外电场作用下向催化电极b移动 C、理论上电路中转移4mole-时可生成2molHCOO- D、阳极区和阴极区的pH均减小 -
13、下列实验方案能达到实验目的的是( )
选项
实验目的
实验方案
A
探究葡萄糖的还原性
在一支试管中先加入2mL10%NaOH溶液,滴入5滴5%CuSO4溶液,再加入2mL10%葡萄糖溶液,加热。观察实验现象
B
检验苯中是否含有苯酚
在盛有苯和苯酚混合溶液的试管中滴加少量溴水。观察实验现象
C
探究不同盐的水解程度
用pH试纸分别测量等体积、等浓度的NaClO溶液和CH3COONa溶液的pH。比较大小
D
检验乙烯的还原性
在圆底烧瓶中加入乙醇和浓硫酸的混合溶液,并加入碎瓷片,迅速升温到170℃,将生成的气体通入高锰酸钾溶液中。观察实验现象
A、A B、B C、C D、D -
14、氧杂环丁基叠氮聚合物制备反应原理如图:



下列说法错误的是( )
A、反应①属于开环聚合反应 B、反应①的催化剂中含有配位键 C、可用红外光谱仪检测叠氮聚合物的生成 D、生成1mol叠氮聚合物需要消耗2molNaN3 -
15、下列关于物质的结构或性质及解释都正确的是( )
选项
物质的结构或性质
解释
A
第一电离能:Zn>Cu
元素金属性:Zn强于Cu
B
熔点:SiO2>CO2
相对分子质量:SiO2大于CO2
C
酸性:HCOOH>CH3COOH
O-H的极性:HCOOH强于CH3COOH
D
O2与O3分子极性相同
二者都是由非极性键构成的分子
A、A B、B C、C D、D -
16、某种离子液体的结构如图所示,其中X、Y、Z、W、Q是原子序数依次增大的短周期主族元素,Z与Q同主族。
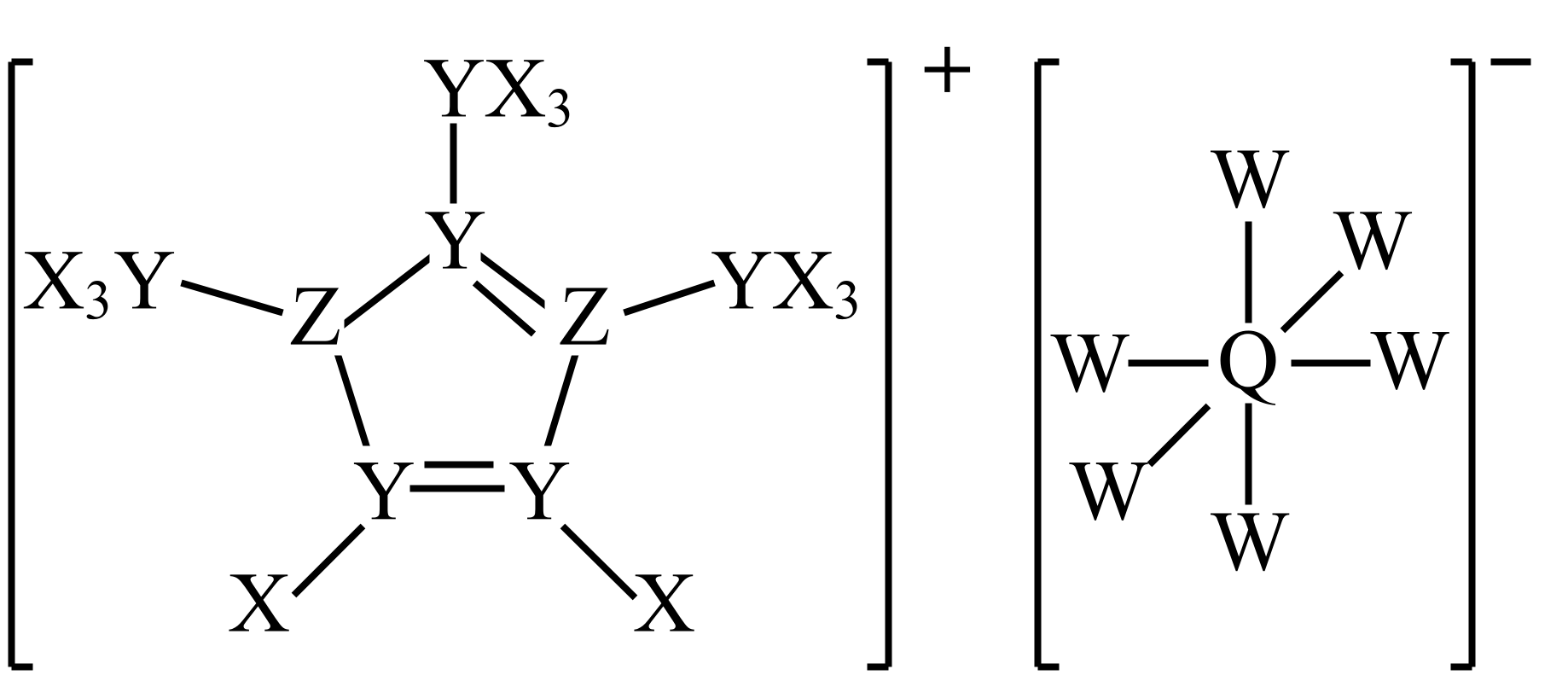
下列说法错误的是( )
A、简单离子半径:Q>Z>W B、简单氢化物键角:Y>Q>Z C、Z原子均满足8电子稳定结构 D、阴离子立体构型为正八面体形 -
17、东莨菪碱为我国东汉名医华佗创制的麻醉药“麻沸散”中的有效成分之一,其结构简式如图所示。下列有关该有机物说法正确的是( )
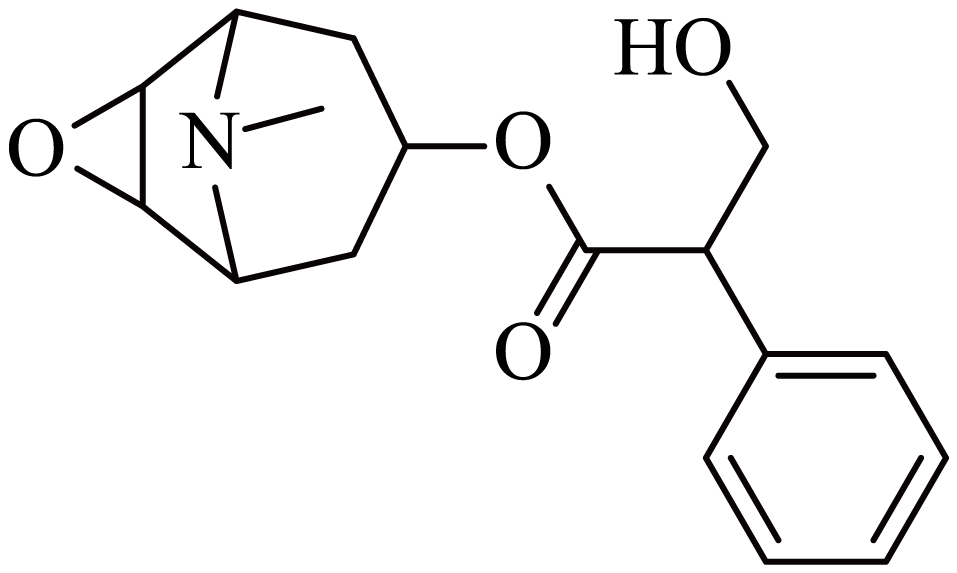 A、分子式为C17H22NO4 B、分子中含有3种官能团 C、分子中所有碳原子可能共平面 D、与强酸或强碱反应均能生成盐
A、分子式为C17H22NO4 B、分子中含有3种官能团 C、分子中所有碳原子可能共平面 D、与强酸或强碱反应均能生成盐 -
18、新研制出的石墨烯-C60揉和了C60分子与石墨烯的结构特点,有关结构如图所示。

下列有关这三种物质的说法错误的是( )
A、碳原子的杂化方式均为sp2 B、C60晶体的熔点最低 C、石墨烯的导电性最好 D、互为同素异形体 -
19、设NA为阿伏加德罗常数的值。下列说法正确的是( )A、24g乙烯和丙烯的混合气体中p-pσ键数目为2NA B、1L1mol/L氯化铵溶液中NH和H+数目之和为NA C、2molNO与1molO2在密闭容器中充分反应后的分子数为2NA D、标准状况下,11.2LCH4与22.4LCl2反应后分子总数为1.5NA
-
20、下列各组离子在指定环境中能大量共存的是( )A、0.1mol/L的NaOH溶液:Cl-、Ba2+、K+、NO B、0.1mol/L的AlCl3溶液:Mg2+、K+、AlO、Cl- C、0.1mol/L的FeCl2溶液:Na+、K+、SO、ClO- D、0.1mol/L的HI溶液:NO、Cl-、Na+、MnO