相关试卷
-
1、下列实验室药品的保存或实验安全应急措施错误的是( )A、漂白粉要避光、密封保存在阴凉处 B、浓溴水沾在皮肤上,先用大量水冲洗,再用酒精擦拭 C、AgNO3溶液应当保存在棕色细口瓶中 D、浓硫酸沾到皮肤上,先用大量水冲洗,然后涂抹稀NaOH溶液
-
2、开元寺铁佛像是世界上现存的最大古代铁佛像,开元大佛为中空铸铁件,外有泥塑涂层和贴金饰层。下列说法正确的是( )A、佛像腰部以上部位表面多呈红棕色,其主要成分为Fe3O4 B、泥塑涂层由黏土烧制而成,泥塑涂层属于硅酸盐材料 C、佛像贴金饰层所用材料为黄金金箔,金箔的制作过程属于化学变化 D、佛像中空铸铁件所用材料为生铁,生铁的含碳量比钢的含碳量低
-
3、有机物J是合成一种具有生物活性物质的中间体,其合成路线如下所示:

请回答下列问题:
(1)、I的含氧官能团名称为;J的分子式为;B的结构简式为。(2)、的名称为。(3)、写出F→G的化学反应方程式:。(4)、G→H的反应类型为。(5)、设置D→E及I→J的反应步骤的目的是。(6)、K比D的分子组成只少1个碳原子,符合下列条件的K的结构有种。(7)、ⅰ.苯环上有两个取代基;ⅱ.遇溶液显色,且能与溶液反应放出。
参照上述合成路线,以
 和
和 为原料,设计合成
为原料,设计合成 的路线:(无机试剂任选)。
的路线:(无机试剂任选)。 -
4、氮氧化物是常见的大气污染物,目前气态含氮化合物及相关转化成为科学家研究的热门问题。
Ⅰ.还原法。反应原理为:。该反应的能量变化过程如下图:
 (1)、(用图中字母a、b、c、d表示)。该反应在(填“高温”、“低温”或“任意温度”)条件下有利于自发进行。(2)、Ⅱ.氧化法。其原理为 。在T℃、条件下,向一恒压密闭容器中按物质的量之比为2:1通入和的混合气体,体系中气体的含量与时间变化关系如图所示。
(1)、(用图中字母a、b、c、d表示)。该反应在(填“高温”、“低温”或“任意温度”)条件下有利于自发进行。(2)、Ⅱ.氧化法。其原理为 。在T℃、条件下,向一恒压密闭容器中按物质的量之比为2:1通入和的混合气体,体系中气体的含量与时间变化关系如图所示。
反应达到平衡,则0~20min内的平约反应速率 , 该反应的平衡常数[对于反应为平衡物质的量分数]。
(3)、若起始条件相同,在恒容密闭容器中发生上述反应,则达到平衡时NO的含量符合上图中点(填“a”、“b”、“c”或“d”)。(4)、Ⅲ.配合物吸收法。其原理如下:
已知:对的配合能力很强,而对的配合能力极低。
与反应的和与反应的物质的量之比为。
(5)、钴氨溶液经过多次循环吸收NO后,其吸收NO的能力会降低,为了恢复钴氨溶液吸收NO的能力,需采取的方法是。(6)、Ⅳ.电解处理法。其原理为用6%的稀硝酸吸收生成亚硝酸,再将吸收液导入电解槽中进行电解,使之转化为硝酸。电解装置如右图所示。
阳极的电极反应式为。
-
5、某实验小组从某废旧锂离子电池正极活性材料(主要成分可表示为 , 还含有少量、的化合物)中分别回收处理金属元素,工艺流程如下图所示:
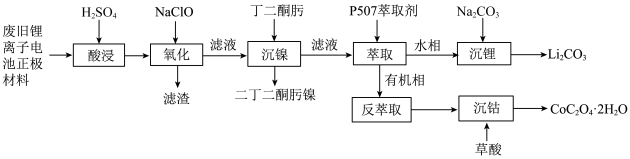
已知:①“酸浸”后滤液中主要金属阳离子为、、、;
②有关金属离子沉淀完全的见下表:
离子
9.3
3.2
9.0
8.9
③沉镍反应为

请回答下列问题:
(1)、丁二酮肟分子中杂化的碳原子个数为 , 二丁二酮肟镍中存在的化学键有(填序号)。A.链 B.氢键 C.金属键 D.配位键
(2)、“氧化”过程的操作为控制体系的在 , 加入溶液,写出反应的离子方程式。(3)、P507萃取剂(用HA表示)萃取的原理可表示为的浸出与水相的关系如图所示。分析较小时萃取率偏低的原因为。 (4)、和在空气氛围中焙烧可得到 , 该反应化学方程式为。(5)、将草酸钴晶体置于空气中加热,受热过程中固体残留率()变化如下图所示,则C点固体物质的化学式为。
(4)、和在空气氛围中焙烧可得到 , 该反应化学方程式为。(5)、将草酸钴晶体置于空气中加热,受热过程中固体残留率()变化如下图所示,则C点固体物质的化学式为。 (6)、的一种晶胞如图所示(仅标出与未标出)、该晶胞中占有O的个数为。
(6)、的一种晶胞如图所示(仅标出与未标出)、该晶胞中占有O的个数为。
-
6、葡萄糖酸钙是一种有机钙盐,主要用作食品的钙强化剂与营养剂、缓冲剂、固化剂、整合剂等。某实验小组在实验室以葡萄糖为原料制备葡萄糖酸钙的流程如下:
已知:相关物质的溶解性见下表:
物质名称
葡萄糖酸钙
葡萄糖酸
溴化钙
氯化钙
水中的溶解性
可溶于冷水,易溶于热水
可溶
易溶
易溶
乙醇中的溶解性
微溶
微溶
可溶
可溶
请回答下列问题:
(1)、实验室进行过程ⅰ时,加快其溶解的措施为。(2)、进行过程ⅱ的实验装置(加热装置已省去)如右图所示:
①写出此过程发生反应的化学方程式(有机物写出分子式即可);应采取的加热方式为。
②装置中仪器M的名称为;冷凝时冷凝水的入口为(填“a”或“b”);装置乙中倒扣漏斗的作用为。
(3)、操作为 , 其目的是;过程ⅴ加入乙醇的作用是。(4)、用电子天平称取葡萄糖酸钙(摩尔质量为)样品溶于水配制成溶液,取溶液置于锥形瓶中,加入指示剂,用的(用表示)标准溶液滴定至终点时,消耗标准溶液的体积为(已知:)。该样品中葡萄糖酸钙的质量分数为(用含有的代数式表示,不需化简)。 -
7、由、、等元素组成的钒基笼目金属在超导电性方面有广阔的应用前景,其晶胞结构如下图所示。下列说法错误的是( )
 A、钒基笼目金属的化学式为 B、分布在由构成的八面体空隙中 C、可以通过射线衍射实验测定晶体结构 D、1号、2号原子间的距离为
A、钒基笼目金属的化学式为 B、分布在由构成的八面体空隙中 C、可以通过射线衍射实验测定晶体结构 D、1号、2号原子间的距离为 -
8、饱和溶液中,随而变化,在温度下,与关系如右图所示。下列说法错误的是( )
 A、的溶度积 B、若忽略的第二步水解, C、饱和溶液中随增大而减小 D、点溶液中:
A、的溶度积 B、若忽略的第二步水解, C、饱和溶液中随增大而减小 D、点溶液中: -
9、铁铬液流电池(总反应为)实现了发电、环保一体化。某兴趣小组用该电池模拟工业处理废气和废水的装置如下图所示,下列说法正确的是( )
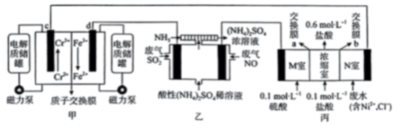 A、为正极,膜为阴离子交换膜 B、乙池中阴极的电极反应式为 C、标准状况下,若乙池中处理废气(和)的总体积为 , 则甲池有质子迁移到极 D、当浓缩室得到的盐酸时,室溶液的质量变化为(溶液体积变化忽略不计)
A、为正极,膜为阴离子交换膜 B、乙池中阴极的电极反应式为 C、标准状况下,若乙池中处理废气(和)的总体积为 , 则甲池有质子迁移到极 D、当浓缩室得到的盐酸时,室溶液的质量变化为(溶液体积变化忽略不计) -
10、用杯酚(表示为
 )分离和的过程如图甲所示,①~③各步骤在实验室中所用到的装置选择合理的是( )
)分离和的过程如图甲所示,①~③各步骤在实验室中所用到的装置选择合理的是( )
 A、①-a、②-a、③-d B、①-a、②-b、③-c C、①-b、②-a、③-d D、①-b、②-b、③-c
A、①-a、②-a、③-d B、①-a、②-b、③-c C、①-b、②-a、③-d D、①-b、②-b、③-c -
11、氨基甲铵()是化学工业中尿素生产过程的中间产物。向刚性密闭容器中加入一定量 , 在不同温度下发生反应 , 反应的压强平衡常数(用平衡时气体的分压代替平衡浓度表示的平衡常数)与反应热间存在关系式:(已知:R、C为常数,为热力学温度)。与关系的图像及相关数据如下图所示,判断下列说法正确的是( )
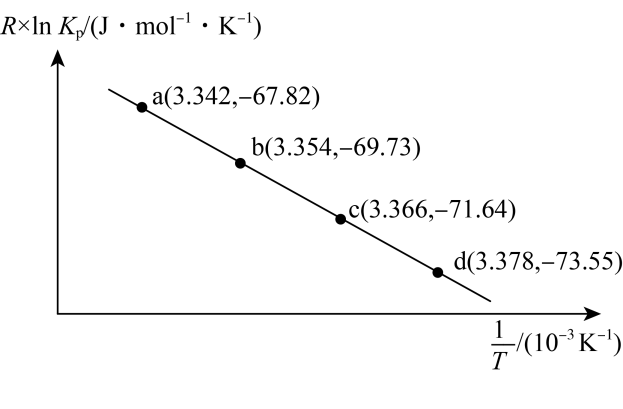 A、当容器内气体平均相对分子质量不再变化时,说明反应已经达到平衡状态 B、当温度一定时,向平衡后的容器内再加入 , 再次达到平衡时和的浓度增大 C、 D、若实验室利用与合成 , 则应选择低温环境进行
A、当容器内气体平均相对分子质量不再变化时,说明反应已经达到平衡状态 B、当温度一定时,向平衡后的容器内再加入 , 再次达到平衡时和的浓度增大 C、 D、若实验室利用与合成 , 则应选择低温环境进行 -
12、下列事实与解释相符的是( )
选项
事实
解释
A
相同条件下,乙醇与钠的反应没有水与钠反应剧烈
乙醇分子中氢氧键的极性比水分子中氢氧键的极性弱
B
与是同族元素,原子之间可以形成双键、三键,但原子之间难以形成双键或三键
易失去电子,不易形成共用电子对
C
在中的溶解度大于在水中的溶解度
是极性分子,而和均为非极性分子
D
充入氦、氖、氩等稀有气体的霓虹灯形成五颜六色的炫丽灯光
气体在外加电场激发下,形成了由电子和阳离子两种粒子组成且能导电的等离子体
A、A B、B C、C D、D -
13、某科研组研究利用碳催化烷烃脱氢反应的机理(其过程如图所示),建立起系统的非金属催化反应理论体系,切实推动了绿色非金属纳米碳催化领域的发展。下列有关碳催化烷烃脱氢过程分析正确的是( )
 A、反应中氧元素及部分碳元素价态有变化 B、生成总反应的化学方程式为 , 属于消去反应 C、
A、反应中氧元素及部分碳元素价态有变化 B、生成总反应的化学方程式为 , 属于消去反应 C、 、
、 、
、 等均是反应的催化剂
D、有极性键和非极性的断裂,但只有极性键形成
等均是反应的催化剂
D、有极性键和非极性的断裂,但只有极性键形成
-
14、轻质碳酸镁是广泛应用于橡胶、塑料、食品和医药工业的化工产品,以卤块(主要成分为 , 含、等杂质离子)为原料制备轻质碳酸镁的工艺流程如图。下列说法错误的是( )
 A、在实验室进行①操作所用的仪器为玻璃棒、烧杯 B、“氧化”工序中发生反应的离子方程式为 C、②和③工序名称均为“过滤” D、“沉镁”工序控制合适的温度,产生的气体主要为和
A、在实验室进行①操作所用的仪器为玻璃棒、烧杯 B、“氧化”工序中发生反应的离子方程式为 C、②和③工序名称均为“过滤” D、“沉镁”工序控制合适的温度,产生的气体主要为和 -
15、短周期X、Y、Z、M、W五种主族元素,其原子半径、简单氢化物的进点分别随原子序数变化的关系如下图所示,常温时,测得、、简单氢化物的水溶液分别为11、4、1。下列说法正确的是( )
 A、的最高价氧化物的空间填充模型为
A、的最高价氧化物的空间填充模型为 B、X、Y、Z的第一电离能:
C、M、W简单离子对水的电离平衡都无影响
D、M、W最高价氧化物的水化物的酸性;
B、X、Y、Z的第一电离能:
C、M、W简单离子对水的电离平衡都无影响
D、M、W最高价氧化物的水化物的酸性;
-
16、下列实验探究方案能达到探究目的的是( )
选项
探究方案
A
向溶液中加入少量固体,振荡,溶液由蓝色变为黄绿色
中的配位键稳定性大于中的配位键
B
向溶液中滴加淀粉溶液,再通入气体,观察现象
比较与氧化性的强弱
C
向和的混合溶液中,滴加12滴溶液,观察沉淀颜色
D
向2支分别盛有不同浓度溶液的试管中,同时加入溶液
探究反应物㳖度对反应速率的影响
A、A B、B C、C D、D -
17、为阿伏加德罗常数的值。我国化学家侯德榜改进国外的纯碱生产工艺,提高了原料利用率。其主要原理为。下列说法正确的是( )A、完全分解,产生气体的分子数目为 B、分子所含价层电子对的数目为3 C、含的和的混合物中,质子总数为28 D、标准状况下含键的数目为0.2
-
18、BAS是一种可定向运动的“分子机器”,其合成路线如下。下列说法正确的是( )
 A、M的分子式为 B、M既能与酸反应又能与碱反应 C、M、BAS均有一个手性碳原子 D、BAS苯环上的一溴代物共有8种
A、M的分子式为 B、M既能与酸反应又能与碱反应 C、M、BAS均有一个手性碳原子 D、BAS苯环上的一溴代物共有8种 -
19、现代高分子材料正向功能化、智能化、精细化方向发展,与各领域的需求密切相关,下列有关高分子的说法错误的是( )A、有“塑料王”之称的聚四氟乙烯是通过四氟乙烯发生加聚反应制得的 B、利用高分子分离膜进行海水淡化,比蒸馏法耗能少 C、制造阻燃或防火线缆的橡胶是通过加聚反应制得的线型结构的合成材料 D、应用于轻型飞机、消防服的芳纶“1414”的数字指单体对苯二胺和对苯二甲酸的官能团在苯环的位置
-
20、科学技术迅速发展,离不开化学知识,下列说法正确的是( )A、“朱雀二号”遥二成为全球首枚成功入轨的液氧甲烷运载火箭,液氧和甲烷作助燃剂 B、“神舟十七号”发动机的耐高温结构材料是一种熔沸点很高的分子晶体 C、火星直升机制造过程中使用的1500多块碳纤维结构件属于无机非金属单质 D、人造卫星和深空探测器强度要求高的零部件采用钛合金或不锈钢等合金材料