相关试卷
-
1、由硫酸铜溶液制取(硫酸四氨合铜晶体)的实验如下:
步骤1:向盛有溶液的试管中,滴加几滴氨水,有蓝色沉淀生成;
步骤2:继续滴加氨水并振荡试管,沉淀溶解,得到深蓝色溶液;
步骤3:向试管中加入乙醇,并用玻璃棒摩擦试管壁,有深蓝色晶体析出。
下列说法不正确的是
A、溶液呈蓝色的原因是是蓝色的 B、步骤2所发生反应的离子方程式为 C、步骤3中加入乙醇是因为乙醇与水可形成分子间氢键,易溶于水 D、与的配位能力弱于 -
2、最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为( )
 A、TiC B、Ti13C14 C、Ti4C7 D、Ti14C13
A、TiC B、Ti13C14 C、Ti4C7 D、Ti14C13 -
3、碱金属氯化物是典型的离子化合物,NaCl和CsCl的晶胞结构如图所示。其中的碱金属离子能够与冠醚形成超分子。


下列说法不正确的是
A、NaCl晶胞中a为Na+ B、CsCl晶体中Cs+周围紧邻8个Cl- C、碱金属离子与冠醚通过离子键形成超分子 D、不同空穴尺寸的冠醚可以对不同碱金属离子进行识别 -
4、部分含硫物质的分类与相应化合价关系如图所示。下列说法正确的是
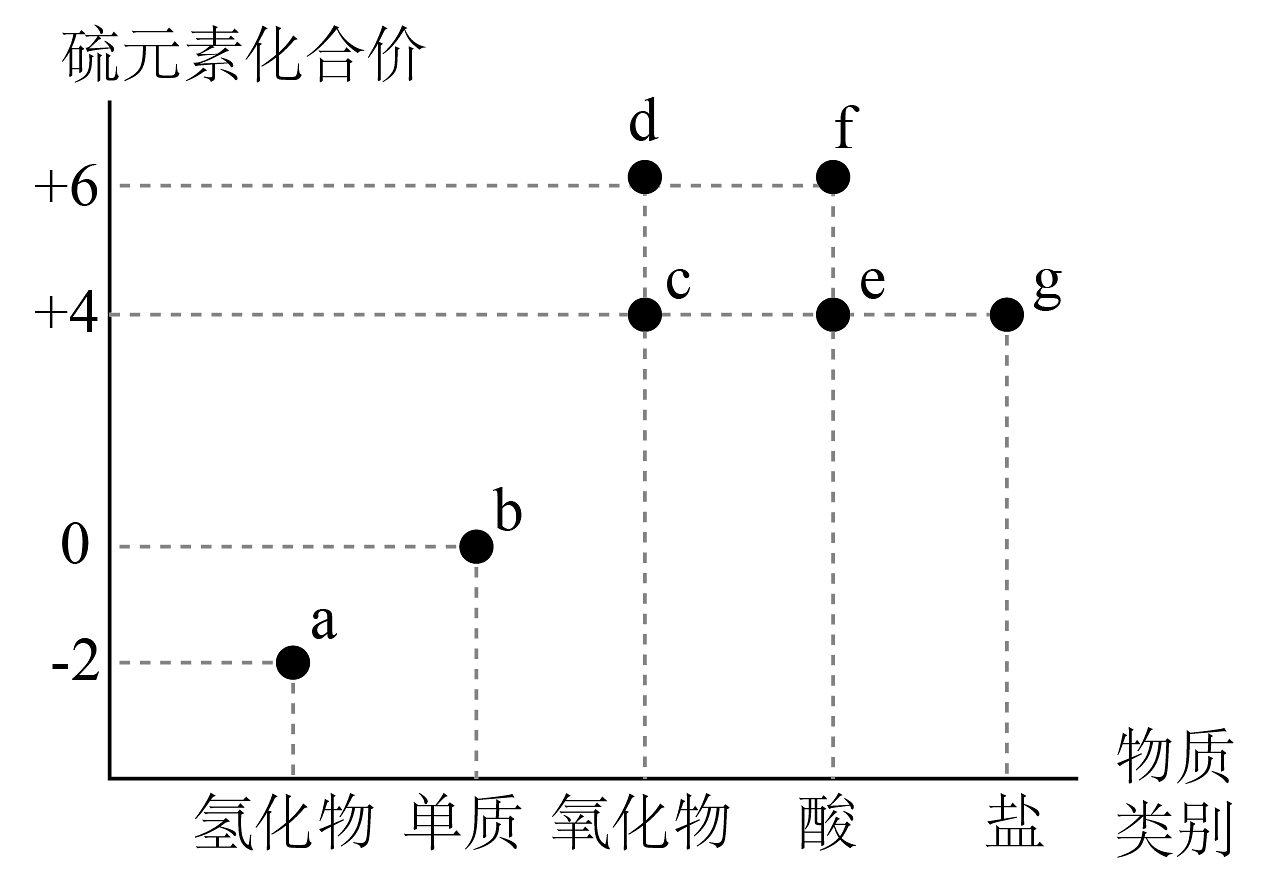 A、b与O2经过一步反应生成 d B、f的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色 C、c通入a的水溶液中出现浑浊,体现了c的氧化性 D、c均能使品红溶液和酸性高锰酸钾溶液褪色,其褪色原理相同
A、b与O2经过一步反应生成 d B、f的浓溶液具有脱水性,可使胆矾晶体由蓝色变为白色 C、c通入a的水溶液中出现浑浊,体现了c的氧化性 D、c均能使品红溶液和酸性高锰酸钾溶液褪色,其褪色原理相同 -
5、已知电离常数:Ka(HCN)=5×10-10 , H2CO3:Ka1=4.3×10-7 , Ka2=5.6×10-11 , 下列离子方程式书写正确的是A、向KCN(aq)中通入少量的CO2气体:CO2+H2O+2CN-=2HCN+CO B、少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO C、氢氧化铁沉淀溶解于过量氢碘酸溶液中:2Fe(OH)3+6H++2I-=2Fe2++6H2O+I2 D、向Ba(OH)2溶液中加入少量的NaHCO3溶液:2HCO+Ba2++2OH-=BaCO3↓+CO+2H2O
-
6、部分含氮、硫元素的化合物的“价—类二维图”如图所示。下列关于各物质的说法错误的是
 A、i的浓溶液可与a发生反应 B、e的浓溶液可用于干燥h、f C、g与在汽车催化转化器中会转化成两种无毒气体 D、将c、h同时通入水中,加入有白色沉淀生成
A、i的浓溶液可与a发生反应 B、e的浓溶液可用于干燥h、f C、g与在汽车催化转化器中会转化成两种无毒气体 D、将c、h同时通入水中,加入有白色沉淀生成 -
7、用下列装置进行实验,能达到实验目的的是
A
B
C
D




证明乙炔可使溴水褪色
制备溴苯并验证有产生
萃取振荡时放气
探究甲烷和的反应
A、A B、B C、C D、D -
8、下列化学用语或图示表达不正确的是A、顺式聚异戊二烯的结构简式:
 B、基态铜原子的价层电子轨道表示式:
B、基态铜原子的价层电子轨道表示式: C、的电子式:
C、的电子式: D、的简化电子排布式:
D、的简化电子排布式:
-
9、用下列装置进行相应实验,能达到实验目的的是
选项
A
B
C
D
实验装置




实验目的
比较N、C、Si的非金属性
制备并观察氢氧化亚铁
配制1.0mol/LNaOH溶液
模拟侯氏制碱法获得NaHCO3
A、A B、B C、C D、D -
10、下列说法不正确的是A、PCl3是极性键构成的极性分子 B、H+能与H2O以配位键形成H3O+ C、分子晶体中,分子间作用力越大,分子越稳定 D、对固体进行X射线衍射测定是区分晶体和非晶体最可靠的科学方法
-
11、如图化合物Q是一种表面涂层材料,其中W、X、Y、Z是分别处于三个短周期的主族元素,原子序数依次增大且不相邻,下列有关说法不正确的是
 A、电负性:Y>Z>X>W B、X的基态原子有6种空间运动状态的电子 C、Y的氢化物的沸点较高,主要是因为分子间存在氢键 D、Q在酸性条件下水解生成的气体为非极性分子
A、电负性:Y>Z>X>W B、X的基态原子有6种空间运动状态的电子 C、Y的氢化物的沸点较高,主要是因为分子间存在氢键 D、Q在酸性条件下水解生成的气体为非极性分子 -
12、一种“本宝宝福禄双全”的有机物曾经刷爆朋友圈,其结构简式为
 , 该物质的同分异构体中具有“本宝宝福禄双全”谐音且两个醛基位于苯环间位的有机物有 A、5种 B、6种 C、7种 D、8种
, 该物质的同分异构体中具有“本宝宝福禄双全”谐音且两个醛基位于苯环间位的有机物有 A、5种 B、6种 C、7种 D、8种 -
13、3-氨基-1-金刚烷醇可用于合成药物维格列汀(治疗2型糖尿病),其分子结构如图所示。下列说法不正确的是
 A、分子中0原子和N原子均为杂化 B、分子中的键角大于的键角 C、分子中的极性大于的极性 D、分子中含有手性碳原子
A、分子中0原子和N原子均为杂化 B、分子中的键角大于的键角 C、分子中的极性大于的极性 D、分子中含有手性碳原子 -
14、下列化学用语或图示表达正确的是A、基态N原子的轨道表示式:
 B、的VSEPR模型:
B、的VSEPR模型: C、的键的形成:
C、的键的形成: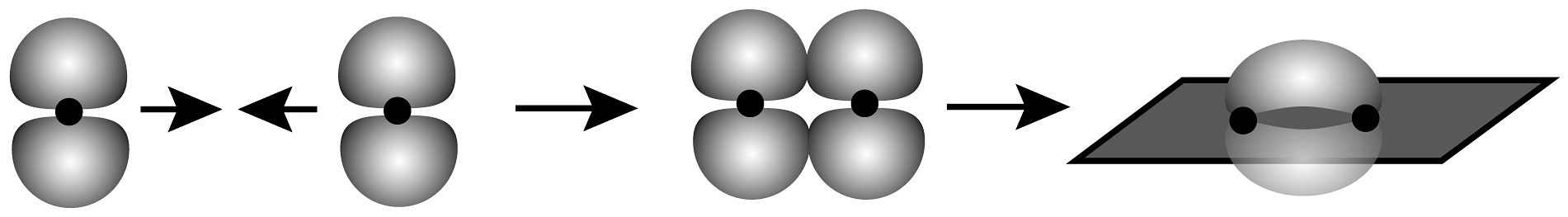 D、用电子式表示HCl的形成过程:
D、用电子式表示HCl的形成过程:
-
15、洋川芎内酯J具有抗炎镇痛的功效,其结构简式如图所示。下列有关洋川芎内酯J的说法错误的是
 A、该物质属于烃的衍生物,其分子式为 B、能使溴水褪色 C、能与酸性高锰酸钾溶液发生反应 D、含有羟基、碳碳双键、酯基三种官能团
A、该物质属于烃的衍生物,其分子式为 B、能使溴水褪色 C、能与酸性高锰酸钾溶液发生反应 D、含有羟基、碳碳双键、酯基三种官能团 -
16、苯甲酸是一种常用的食品防腐剂。某实验小组设计粗苯甲酸(含有少量NaCl和泥沙)的提纯方案如下:

下列说法不正确的是
A、操作I中依据苯甲酸的溶解度估算加水量 B、操作Ⅱ趁热过滤的目的是除去泥沙和NaCl C、操作Ⅲ缓慢冷却结晶可减少杂质被包裹 D、操作Ⅳ可用冷水洗涤晶体 -
17、牙膏是常见的日用化学品。某种牙膏中的摩擦剂为碳酸钙 , 它属于A、酸 B、碱 C、盐 D、单质
-
18、甲醇是一种用途广泛的基础有机原料和优质燃料。(1)、甲醇可以在铜做催化剂的条件下直接氧化成甲醛。
①基态原子的价层电子的轨道表示式为。
②甲醛中碳原子的杂化方式为杂化,其组成元素的电负性由小到大的顺序为。
(2)、在一定条件下,甲醇可转化为乙酸甲酯 , 一个乙酸甲酯分子中键和键个数之比为。(3)、由制备的可用于检验醛基。中配位原子为 , 的空间构型为。(4)、图中银晶胞的边长为 , 该晶胞中的配位数为;该晶胞密度为(用含、的代数式表示)。
-
19、设NA为阿伏加德罗常数的值。下列说法正确的是( )A、高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA B、室温下,1L pH=13的NaOH溶液中,由水电离的OH﹣离子数目为0.1NA C、氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA D、5NH4NO3
 2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
-
20、对氨基苯甲酸可用甲苯为原料合成。已知①苯环上的硝基可被还原为氨基:

 , 产物苯胺还原性强,易被氧化;②−CH3为邻、对位取代定位基,而−COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是 A、甲苯 X Y对氨基苯甲酸 B、甲苯XY对氨基苯甲酸 C、甲苯XY对氨基苯甲酸 D、甲苯XY对氨基苯甲酸
, 产物苯胺还原性强,易被氧化;②−CH3为邻、对位取代定位基,而−COOH为间位取代定位基。则由甲苯合成对氨基苯甲酸的步骤合理的是 A、甲苯 X Y对氨基苯甲酸 B、甲苯XY对氨基苯甲酸 C、甲苯XY对氨基苯甲酸 D、甲苯XY对氨基苯甲酸