相关试卷
-
1、设为阿伏加德罗常数值.下列有关叙述正确的是A、甲烷中的氢原子被氯原子完全取代,需要氯气分子数为 B、甘油(丙三醇)中含有羟基数为 C、乙烯和丙烯混合气体中的氢原子数为 D、标准状况下,含有的共价键数为
-
2、自从第一次合成稀有气体元素的化合物XePtF6以来,人们又相继发现了氙的一系列化合物,如XeF2、XeF4等。如图甲为XeF4的结构示意图,图乙为XeF2晶体的晶胞结构图。下列有关说法正确的是
 A、XeF4是极性分子 B、XeF2晶体属于离子晶体 C、一个XeF2晶胞中实际拥有2个XeF2 D、XeF2晶体中距离最近的两个XeF2之间的距离为a(a为晶胞边长)
A、XeF4是极性分子 B、XeF2晶体属于离子晶体 C、一个XeF2晶胞中实际拥有2个XeF2 D、XeF2晶体中距离最近的两个XeF2之间的距离为a(a为晶胞边长) -
3、下列说法正确的是A、
 的一溴代物和
的一溴代物和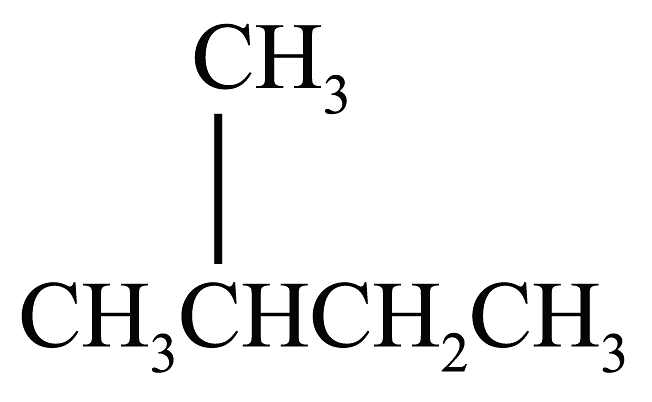 的一溴代物都有4种(不考虑立体异构)
B、等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C、按系统命名法,化合物
的一溴代物都有4种(不考虑立体异构)
B、等物质的量的苯和苯甲酸完全燃烧消耗氧气的量不相等
C、按系统命名法,化合物 的名称是2,3,4一三甲基-2-乙基戊烧
D、
的名称是2,3,4一三甲基-2-乙基戊烧
D、 和
和 互为同系物
互为同系物
-
4、石棉具有高度耐火性、电绝缘性和绝热性,是重要的防火、绝缘和保温材料,其化学式为 , 其组成也可写成余化物形式:。下列说法正确的是A、组成元素均位于元素周期表的p区 B、的熔点比的高 C、ⅣA族元素单质的晶体类型相同 D、基态硅原子核外电子有8种不同的空间运动状态
-
5、下列说法正确的是A、基态Cr原子的价层电子:3d54s1 , 违反能量最低原理 B、基态C原子的电子排布式:1s22s22px12pz1 , 违反能量最低原理 C、基态C原子的价层电子排布图:
 ,违反泡利原理
D、基态Fe3+的3d电子排布图:
,违反泡利原理
D、基态Fe3+的3d电子排布图: ,违反洪特规则
,违反洪特规则
-
6、溶于浓溶液中可得到配合物。下列说法错误的是A、提供空轨道 B、中心离子的配位数是4 C、含有键数目为 D、向溶液中逐滴滴加浓溶液至过量,先形成蓝色沉淀,后沉淀溶解
-
7、依据元素周期律,下列判断不正确的是A、原子半径:Mg<Na<K B、第一电离能:Li<Be<B C、电负性:N<O<F D、热稳定性:SiH4<PH3<HCl
-
8、下列关于水合氢离子的说法错误的是A、含有极性键 B、空间构型为三角锥形 C、键角: D、和中氧原子均为杂化
-
9、下列化学用语表示正确的是A、中子数为10的氧原子: B、的空间结构:(直线型) C、二甲基甲酰胺的结构简式:
 D、的电子式:
D、的电子式:
-
10、人类对核外电子运动的认知不断进步。下列说法正确的是A、电子在线性轨道上绕核运行 B、电子从激发态跃迁到基态时能产生吸收光谱 C、、、轨道相互平行、能量相等 D、轨道比轨道大,其空间包含了轨道
-
11、下列关于有机化合物的说法不正确的是
A
B
C
D



木糖醇()是一种天然甜味剂,属于糖类化合物
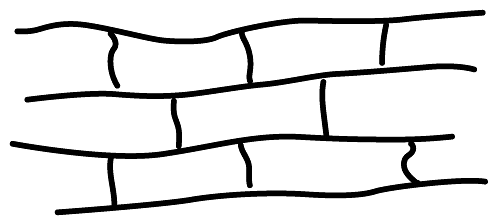
聚乙烯由线型结构转变为网状结构能够增加材料的强度
DNA分子复制过程中存在氢键的断裂和形成
烷基磺酸钠(表面活性剂)在水中聚集形成的胶束属于超分子
A、A B、B C、C D、D -
12、下列实验操作对应的现象预测正确或能达到有关实验目的的是
 A、①可比较、的稳定性 B、②焰色试验检验K元素 C、③分离氯化铁溶液和氢氧化铁胶体 D、④制备氢氧化铁胶体
A、①可比较、的稳定性 B、②焰色试验检验K元素 C、③分离氯化铁溶液和氢氧化铁胶体 D、④制备氢氧化铁胶体 -
13、为验证不同化合价铁的氧化还原能力,利用下列电池装置进行实验。

回答下列问题:
(1)由FeSO4·7H2O固体配制0.10 mol·L−1 FeSO4溶液,需要的仪器有药匙、玻璃棒、(从下列图中选择,写出名称)。

(2)电池装置中,盐桥连接两电极电解质溶液。盐桥中阴、阳离子不与溶液中的物质发生化学反应,并且电迁移率(u∞)应尽可能地相近。根据下表数据,盐桥中应选择作为电解质。
阳离子
u∞×108/(m2·s−1·V−1)
阴离子
u∞×108/(m2·s−1·V−1)
Li+
4.07
4.61
Na+
5.19
7.40
Ca2+
6.59
Cl−
7.91
K+
7.62
8.27
(3)电流表显示电子由铁电极流向石墨电极。可知,盐桥中的阳离子进入电极溶液中。
(4)电池反应一段时间后,测得铁电极溶液中c(Fe2+)增加了0.02 mol·L−1。石墨电极上未见Fe析出。可知,石墨电极溶液中c(Fe2+)=。
(5)根据(3)、(4)实验结果,可知石墨电极的电极反应式为 , 铁电极的电极反应式为。因此,验证了Fe2+氧化性小于 , 还原性小于。
(6)实验前需要对铁电极表面活化。在FeSO4溶液中加入几滴Fe2(SO4)3溶液,将铁电极浸泡一段时间,铁电极表面被刻蚀活化。检验活化反应完成的方法是。
-
14、下列关于物质的结构或性质及解释都正确的是
选项
物质的结构或性质
解释
A
金属活动性:Mg>Al
第一电离能:Mg>Al
B
熔点:SiO2>CO2
相对分子质量:SiO2大于CO2
C
酸性:HCOOH>CH3COOH
O-H的极性:HCOOH强于CH3COOH
D
熔点:Cl2<Br2<I2
键能:Cl-Cl>Br-Br>I-I
A、A B、B C、C D、D -
15、钴的一种化合物的晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点的为 , 晶胞边长为anm,下列说法中不正确的是
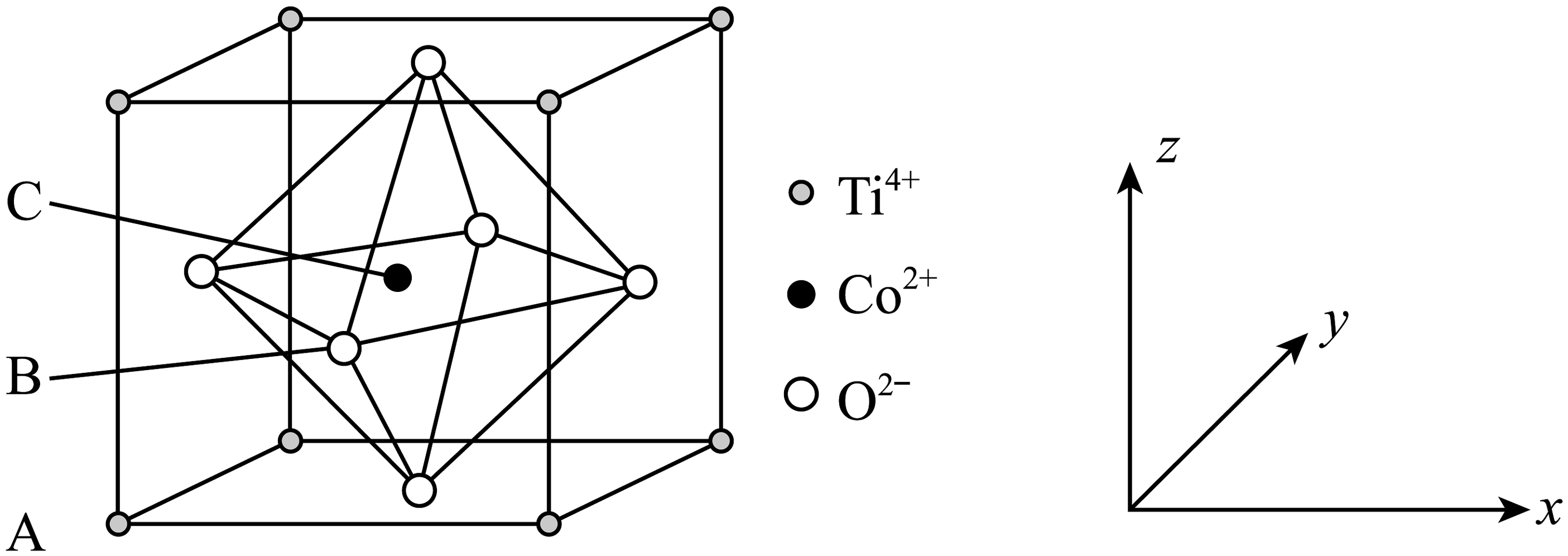 A、与之间的最短距离为 B、距离最近且等距的的数量为6 C、C点的原子坐标数为 D、该物质的化学式为
A、与之间的最短距离为 B、距离最近且等距的的数量为6 C、C点的原子坐标数为 D、该物质的化学式为 -
16、由化合物X、Y为起始原料可合成药物Z。下列说法正确的是( )
 A、X分子中所有碳原子可处于同一平面 B、X、Z分子中均含有2个手性碳原子 C、1molZ最多只能与2molBr2发生反应 D、X、Y、Z均可与NaOH稀溶液发生反应
A、X分子中所有碳原子可处于同一平面 B、X、Z分子中均含有2个手性碳原子 C、1molZ最多只能与2molBr2发生反应 D、X、Y、Z均可与NaOH稀溶液发生反应 -
17、下列陈述Ⅰ和陈述Ⅱ均正确且有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
的非金属性比Si强
溶液中滴加盐酸产生白色浑浊
B
的孤电子对数多于
的键角小于
C
共价键键能小于
晶体沸点高于
D
分子稳定性高于分子
分子间有氢键
A、A B、B C、C D、D -
18、矿物M中含有原子序数依次增大且均不大于20的X、Y、Z、W、E五种主族元素,X、W为同主族非金属元素,Y、Z、E为金属元素,Z的最高正化合价为+2价,Z和E同主族。下列说法错误的是A、最简单气态氢化物的稳定性:W<X B、简单离子半径:X>Y>Z C、最高价氧化物对应的水化物的碱性:Z<E D、X和Y形成的离子化合物中不可能含共价键
-
19、2024年4月28日,神舟十七号、神舟十八号航天员乘组顺利完成交接仪式。航天员的宇航服需要用到多种材料,下列有关叙述错误的是A、制纯棉内衣用到的棉花的主要成分是纤维素 B、保暖层所用的鹅绒属于天然高分子材料 C、水冷层所用的聚氯乙烯属于饱和烃 D、防护层所用的聚酰胺纤维属于合成纤维
-
20、Ni可活化制得 , 其反应历程如图所示:

下列关于活化历程的说法正确的是
A、总反应的 B、总反应的速率由“中间体2→中间体3”决定 C、该反应过程中有碳氢键、碳碳键的断裂和形成 D、使用更高效的催化剂可降低反应所需的活化能和焓变