相关试卷
-
1、下表为元素周期表的一部分,请参照元素①~⑥在表中的位置,用化学用语回答下列问题:
族
周期
IA
0
1
IIA
IIIA
IVA
VA
VIA
VIIA
2
①
②
③
3
④
⑤
⑥
⑦是短周期元素中原子半径最大的元素(稀有气体元素除外)。
(1)、⑦在元素周期表中的位置是。(2)、画出⑥的简单离子结构示意图:。(3)、①、③、⑤的原子半径由小到大的顺序为(用原子符号表示)。(4)、④和⑥组成的化合物中化学键类型是。(5)、化合物X由③和⑦组成且两种元素物质的量之比为 , X的电子式是。(6)、④的单质和⑦的最高价氧化物对应水化物反应的离子方程式是。(7)、下列化合物中属于强酸的有(填标号)。a.⑥的简单氢化物 b.②的简单氢化物
c.①的最高价氧化物对应水化物 d.②的最高价氧化物对应水化物
-
2、柠檬酸加热时可发生如下的转化:

下列说法正确的是
A、柠檬酸、顺乌头酸、异柠檬酸互为同分异构体 B、柠檬酸可以在Cu作催化剂、加热的条件下与O2发生催化氧化反应 C、1mol柠檬酸与足量NaOH溶液反应,最多可以消耗4molNaOH D、顺乌头酸转化为异柠檬酸的反应属于加成反应 -
3、工业上用某种氧化铝矿石(含Fe2O3杂质)为原料冶炼铝的工艺流程如下图所示:

对上述流程的判断正确的是
A、试剂X可以为NaOH溶液,“沉淀”中含有铁的化合物 B、CO2可以用稀硫酸或稀盐酸代替 C、Y为Na2CO3溶液 D、工业上还可采用Fe高温还原Al2O3的方法制Al -
4、工业上从含硒的废液中提取硒的方法之一是用硫酸和硝酸处理废料,获得亚硒酸和少量硒酸 , 再与盐酸共热,硒酸转化为亚硒酸,反应方程式为。在亚硒酸溶液中通入 , 有单质硒析出。下列说法错误的是A、氧化性: B、亚硒酸与生成单质硒的反应可能生成 C、析出硒需要消耗标准状况下 D、亚硒酸理论上既有氧化性,又有还原性,但还原性不及亚硫酸
-
5、W、X、Y和Z为原子序数依次增大的四种短周期元素。W与X可生成一种红棕色有刺激性气味的气体:Y是短周期主族元素中金属性最强的元素;Z原子最外层的电子数与W的电子总数相同。下列叙述正确的是A、X与W元素、X与Y元素都可形成不止一种二元化合物 B、W的氧化物对应的水化物是氧化性强酸 C、最简单氢化物的稳定性: D、最简单氢化物的沸点:
-
6、下图是实验室进行制备与性质实验的组合装置,部分固定装置和装置B前后的干燥装置未画出。下列有关说法确的是
 A、为防止环境污染,装置C和E中的试剂均取用饱和的石灰水 B、关闭 , 打开 , 滴加硫酸,则装置B中每消耗 , 转移电子 C、关闭 , 打开 , 试剂X是酸性溶液或溶液,均可证明有还原性 D、实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性
A、为防止环境污染,装置C和E中的试剂均取用饱和的石灰水 B、关闭 , 打开 , 滴加硫酸,则装置B中每消耗 , 转移电子 C、关闭 , 打开 , 试剂X是酸性溶液或溶液,均可证明有还原性 D、实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性 -
7、某温度下,化学反应的能量变化如下图所示,分子内原子均以单键结合。则下列说法正确的是
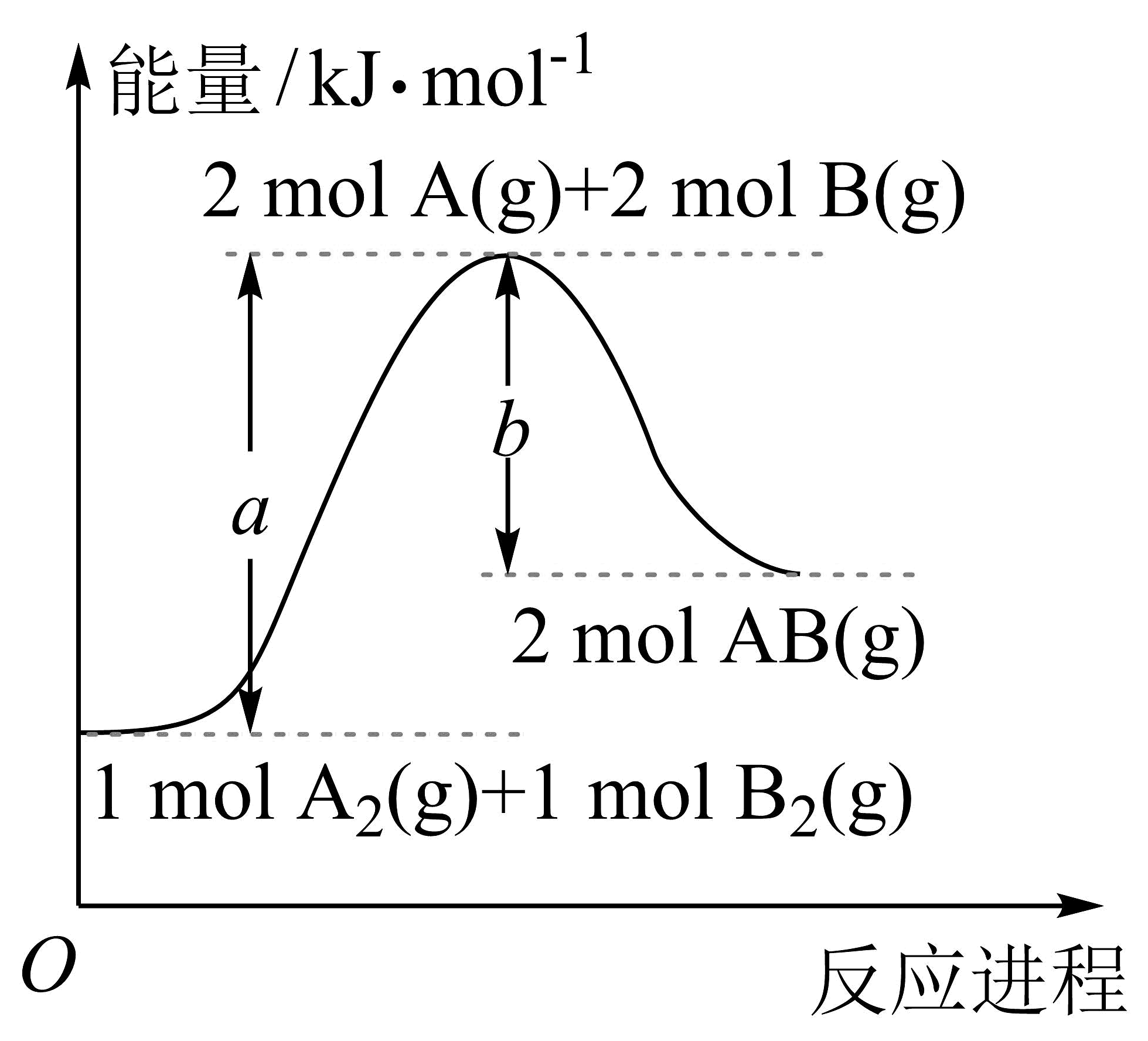 A、该反应是放热反应 B、加入催化剂可以改变反应的热效应 C、断裂需要吸收的能量 D、和具有的能量为
A、该反应是放热反应 B、加入催化剂可以改变反应的热效应 C、断裂需要吸收的能量 D、和具有的能量为 -
8、一种锌-溴电池原理示意图如下图所示,隔膜为阳离子交换膜(只允许阳离子通过)。下列说法错误的是
 A、电子从电极a经导线流向电极b B、在电池内部,阳离子由电极a往电极b方向移动 C、电极b为负极,发生的电极反应为 D、每消耗 , 理论上转移电子
A、电子从电极a经导线流向电极b B、在电池内部,阳离子由电极a往电极b方向移动 C、电极b为负极,发生的电极反应为 D、每消耗 , 理论上转移电子 -
9、反应在一可变容积的容器中进行反应,下列条件的改变对其反应速率几乎无影响的是A、将容器的体积缩小一半 B、保持体积不变,充入N2 C、保持体积不变,升高温度 D、压强不变,充入N2使体积增大
-
10、下列离子能大量共存的是A、 B、 C、 D、
-
11、下列有关电极方程式或离子方程式书写正确的是A、过量NaHSO3溶液与澄清石灰水混合: B、氯气与水反应: C、锌、铜和稀硫酸组成的原电池正极发生的反应: D、硝酸亚铁稀溶液中加入稀硫酸:
-
12、下列实验装置或操作正确且能达到实验目的的是(部分夹持装置已略去)


A.制取并收集NH3
B.除去Cl2气体中混有的少量HCl气体


C.分离粗盐中的不溶物
D.灼烧碎海带
A、A B、B C、C D、D -
13、下列说法不正确的是A、食用油在空气中放置过久产生“哈喇”味,是因为其中的某些有机物发生了氧化反应 B、糖类都能在加热条件下与新制氢氧化铜反应生成砖红色沉淀 C、聚乙烯不能使酸性高锰酸钾溶液褪色 D、医用酒精消毒的原理是使蛋白质变性
-
14、下列化学用语表达错误的是A、HClO的电子式:
 B、质量数为195、中子数为117的铂原子:
C、乙醇的球棍模型:
B、质量数为195、中子数为117的铂原子:
C、乙醇的球棍模型: D、乙醛的结构简式:CH3COH
D、乙醛的结构简式:CH3COH
-
15、日常生活中经常用到各类材料,下列说法正确的是A、铝制餐具不宜长时间存放酸性食物,适合长时间存放碱性食物 B、新能源汽车上使用的半导体材料是一种新型陶瓷 C、与石墨互为同分异构体 D、天然橡胶、聚丙烯纤维、玻璃纤维都属于有机高分子材料
-
16、下列过程中的化学反应,相应的离子方程式正确的是A、稀盐酸中加入碳酸镁浊液: B、少量溶液与澄清石灰水反应: C、稀硫酸中加入氢氧化钡溶液: D、次氯酸钙溶液中通入少量:
-
17、关于反应:的叙述不正确的是A、既是氧化剂又是还原剂 B、发生了分解反应 C、只有氮元素价态变化了 D、氧化产物和还原产物质量比为9∶7
-
18、氢硫酸()是二元弱酸,常温下,某同学做了如下三组实验:
实验I:向溶液中滴加溶液
实验II:向溶液中滴加溶液
实验III:向溶液中滴加溶液
已知:的电离平衡常数 , , , 。忽略溶液混合后体积变化。
下列说法不正确的是
A、实验I中溶液体积为时,溶液中 B、实验I中溶液体积小于时,会发生反应 C、实验II不可以选用甲基橙作为指示剂 D、实验III中溶液体积为时,溶液等于1 -
19、托伐普坦是一种治疗心血管疾病的药物,其前体(L)合成步骤如图(部分试剂和条件略去)。
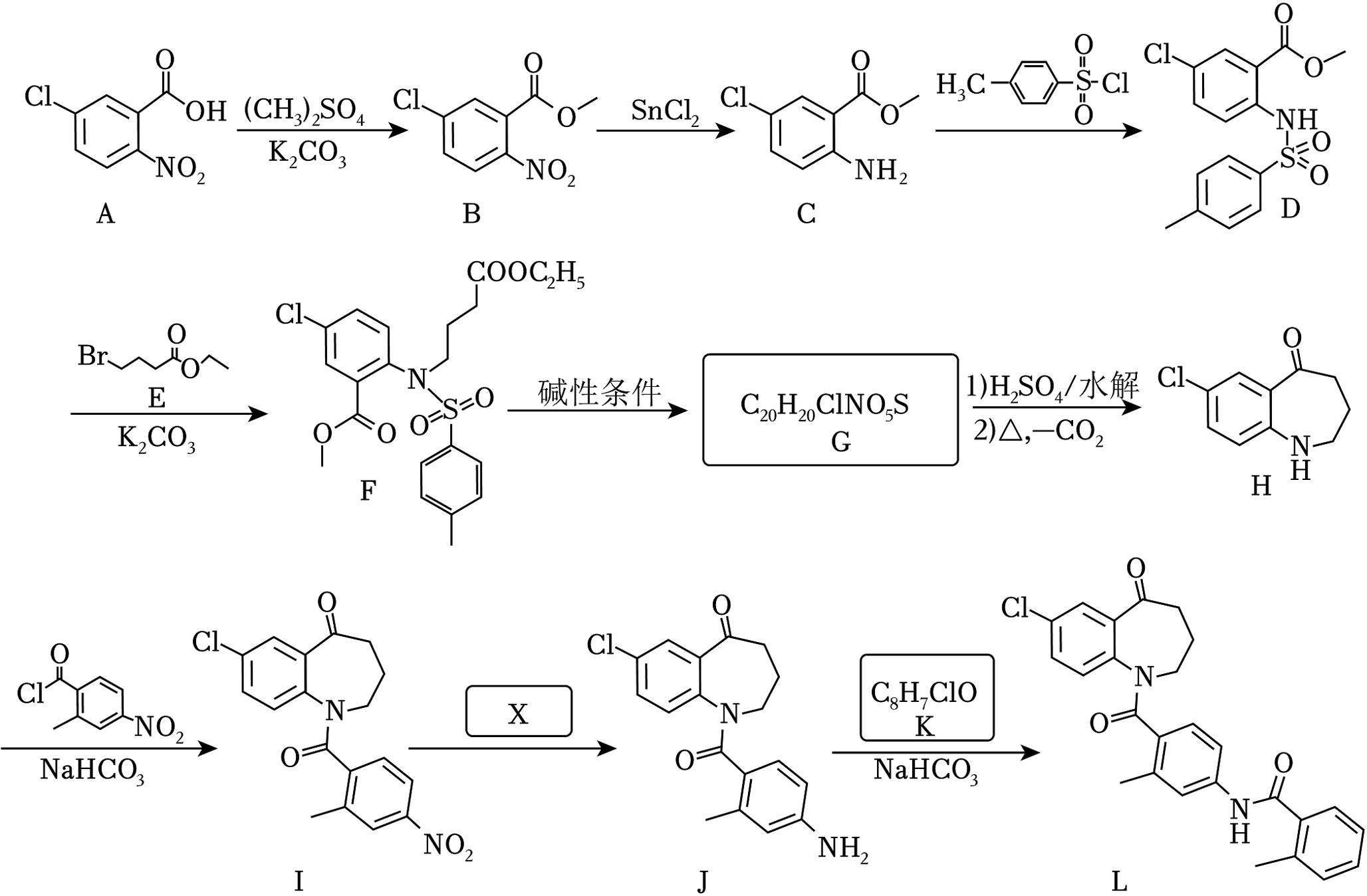
已知:

回答下列问题:
(1)、化合物A(填“能”或“不能”)形成分子内氢键。(2)、写出由C生成D的化学反应方程式。(3)、写出G的结构简式。(4)、H到I的反应类型是。(5)、参照上述合成路线,试剂X的化学式是。(6)、K完全水解后,有机产物的名称是。(7)、E的消去产物(C6H10O2)的同分异构体中,同时满足下列条件a、b和c的可能结构有种(立体异构中只考虑顺反异构);写出只满足下列条件a和c,不满足条件b的结构简式(不考虑立体异构)。a)能与饱和碳酸氢钠溶液反应产生CO2;
b)红外光谱中有碳碳双键特征吸收峰;
c)核磁共振氢谱峰面积比例为3∶3∶2∶1∶1。
-
20、氯及其化合物的“价-类”二维图。d、e属于钾盐。下列说法不正确的是
 A、b溶液久置后会转化为c B、电解饱和e溶液可以制取a C、往冷的溶液通入a可得到d和e D、d→e的转化可以用于制取氧气
A、b溶液久置后会转化为c B、电解饱和e溶液可以制取a C、往冷的溶液通入a可得到d和e D、d→e的转化可以用于制取氧气