相关试卷
-
1、某反应可有效降低汽车尾气污染物的排放,其反应热。一定条件下该反应经历三个基元反应阶段,反应历程如图所示(TS表示过渡态),下列说法不正确的是
 A、三个基元反应中只有①是吸热反应 B、
A、三个基元反应中只有①是吸热反应 B、 是该反应的中间产物
C、该过程的总反应为
D、
是该反应的中间产物
C、该过程的总反应为
D、
-
2、下列推论正确的是A、 ;则石墨比金刚石稳定 B、已知 , 则固体与稀盐酸完全反应,放出的热量即为 C、 , ;则 D、 、;则该反应在高温时才能自发进行
-
3、在25℃时,下列说法正确的是A、的醋酸溶液稀释100倍, B、向氨水中加入稀硫酸至 , 此时 C、溶液中,离子浓度大小关系为: D、同浓度的①②溶液,:①>②
-
4、恒容密闭容器中发生反应 , 转化率随时间变化如图所示,要使反应由过程a变为过程b,可采取措施是
 A、升高温度 B、增大压强 C、加催化剂 D、加大的投入量
A、升高温度 B、增大压强 C、加催化剂 D、加大的投入量 -
5、宏观辨识与微观探析是化学学科核心素养之一,下列说法正确的是A、在常温下,的溶液中能大量存在:Cl-、SO、Na+、NH B、水溶液中H2CO3的电离方程式:H2CO32H++CO C、NaHSO3溶液的水解平衡:HSO+H2OSO+H3O+ D、表示H2燃烧热的热化学方程式:2H2(g)+O2(g)=2H2O(g) =﹣483.6kJ/mol
-
6、用钌(Ru)基催化剂催化CO2(g)和H2(g)的反应时,反应机理如下图,下列说法正确的是
 A、该反应历程中包含6个基元反应 B、图示中参与循环的物质只有CO2和H2 C、总反应式为 D、图示中的物质Ⅰ可提高H2的平衡转化率
A、该反应历程中包含6个基元反应 B、图示中参与循环的物质只有CO2和H2 C、总反应式为 D、图示中的物质Ⅰ可提高H2的平衡转化率 -
7、下列实验或装置不能达到目的的是
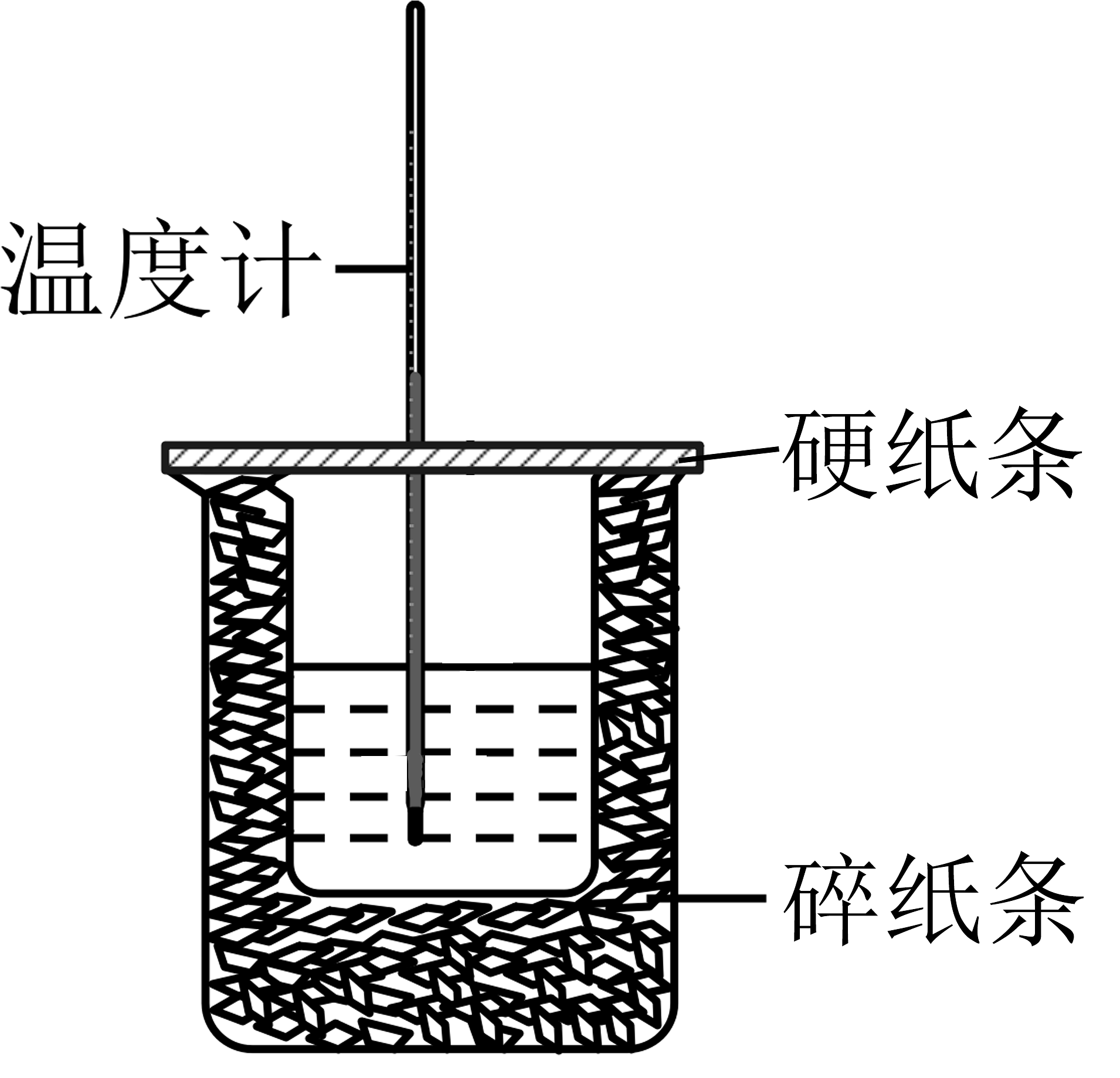
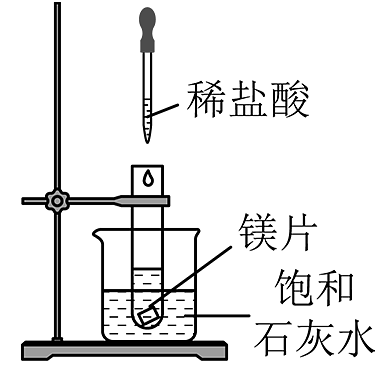
A.测定中和热
B.验证镁片与稀盐酸反应放热
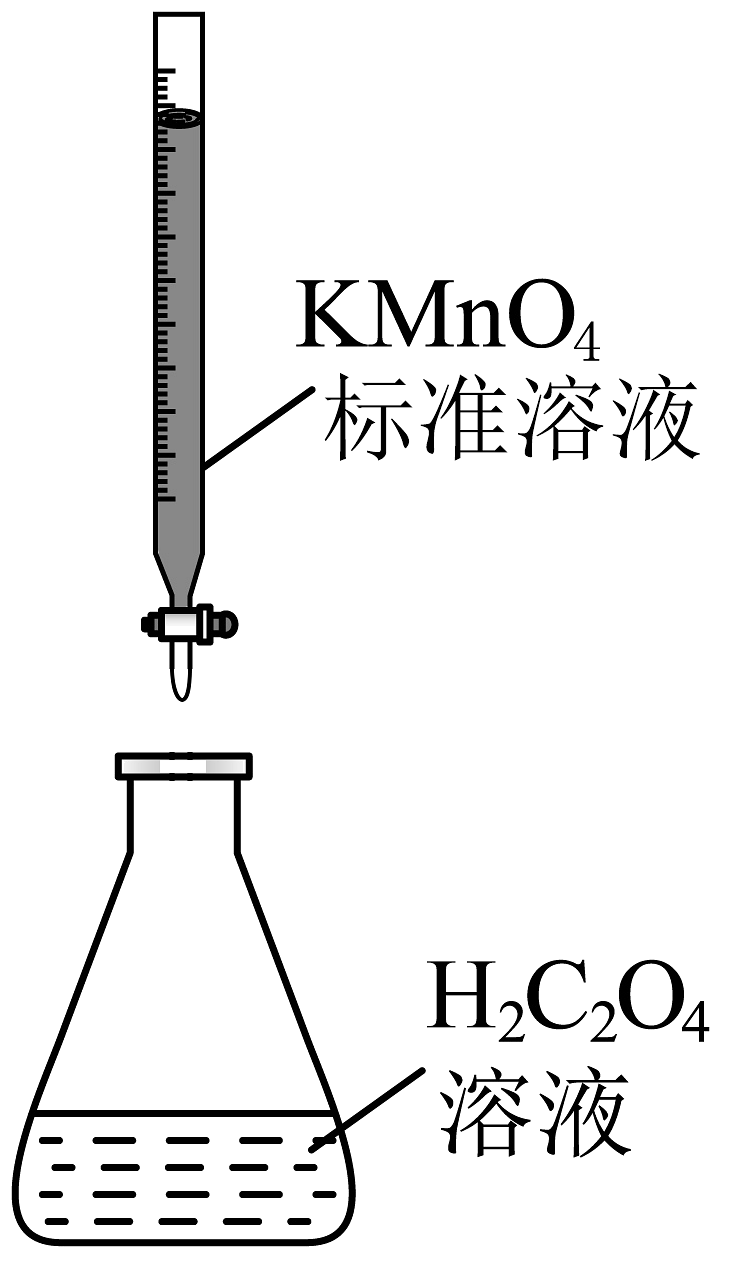
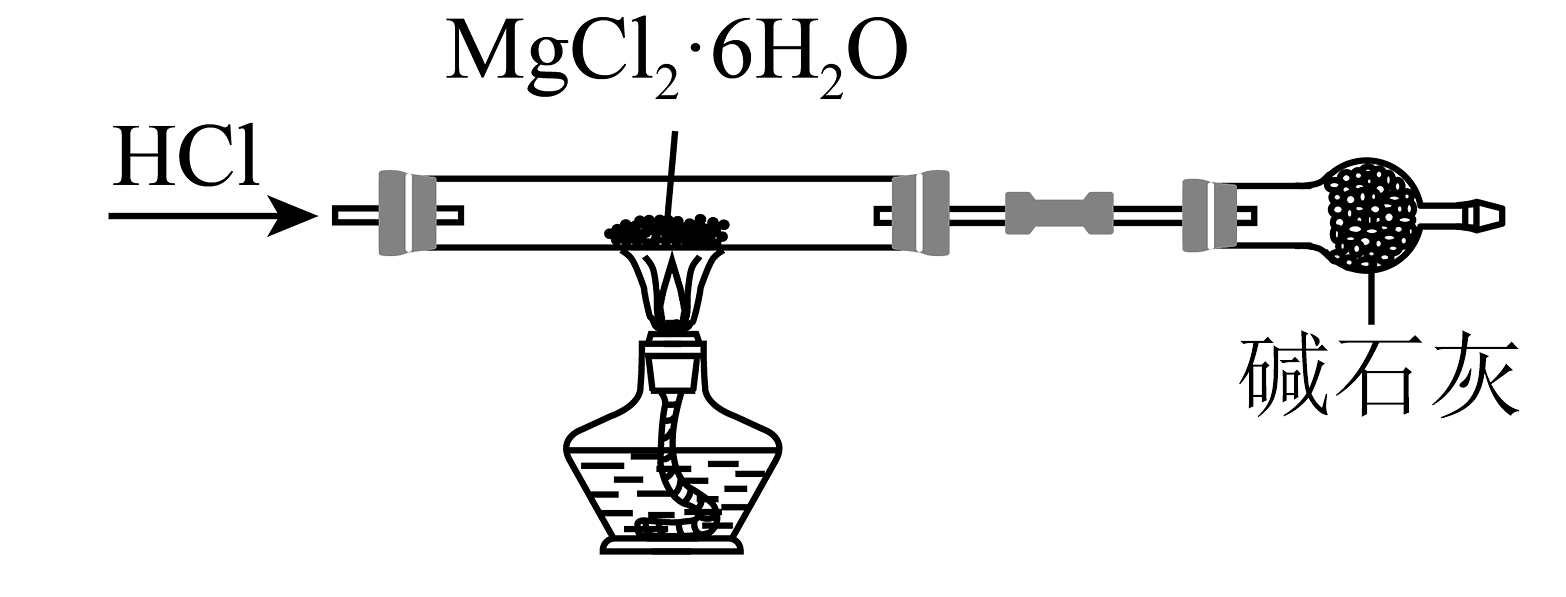
C.测定溶液的浓度
D.制备无水
A、A B、B C、C D、D -
8、劳动有利于“知行合一”。下列劳动项目与所述的化学知识没有关联的是
选项
劳动项目
化学知识
A
家务劳动:热纯碱液浸泡油烟机滤网
升温促进碳酸钠水解
B
社区服务:使用氯化铵溶液清洗铁锈
氯化铵可分解产生HCl
C
医药管理:用冰箱保存疫苗
温度越低,反应速率越慢
D
学农活动:野炊时将煤炭碾碎使用
增大煤炭与空气接触面积,加快燃烧
A、A B、B C、C D、D -
9、在“天宫课堂”中,王亚平老师用蘸有醋酸钠晶体的毛毡点在过饱和醋酸钠“水球”上,“水球”变成温热的“冰球”,“冰球”的成分为CH3COONa·3H2O和水。下列说法不正确的是A、“水球”显碱性 B、过饱和醋酸钠溶液易结晶 C、“水球”变成“冰球”的过程放热、熵增 D、醋酸钠是强电解质
-
10、下列事实不能用勒夏特列原理解释的是A、唾液可以使淀粉水解速率加快 B、打开碳酸饮料瓶盖时产生气泡 C、CO中毒的病人进入高压氧舱中接受治疗 D、氯水中加入粉末以提高氯水中的浓度
-
11、我国科学家设计出多孔石墨炔负载量子点(颗粒直径在2-20)光催化剂,使得合成氨取得了理想的产率。已知 , 下列说法错误的是A、使用催化剂可显著提高生产效率 B、升温能提高氨气的平衡产率 C、使用催化剂,活化分子百分含量增多 D、该催化剂表面积大,催化效果好
-
12、我国固体燃料运载火箭发射水平不断取得新突破。下列关于“该燃料”说法错误的是A、与液体燃料相比易存储和运输 B、固体燃料提供的能量一定比液体燃料的多 C、燃烧时能量转化形式为:化学能→热能→机械能 D、燃烧前后能量大小关系为:反应物总能量>生成物总能量
-
13、用下列方法均可制得氯气:
①MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O
②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
若要制得相同质量的氯气,①②③反应中电子转移数目之比为
A、6:5:6 B、1:3:5 C、15:5:3 D、1:6:10 -
14、下列各组中反应I和反应Ⅱ能用同一离子方程式表示的是
选项
反应Ⅰ
反应Ⅱ
A
Cu(OH)2与稀盐酸
NaOH与稀硫酸
B
BaCl2溶液与Na2SO4溶液
Ba(OH)2溶液与K2SO4溶液
C
Na2CO3溶液与稀盐酸
BaCO3与稀盐酸
D
CaCO3与稀硝酸
CaCO3与稀醋酸
A、A B、B C、C D、D -
15、KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如下:

上述流程中没有涉及的化学反应类型是
A、化合反应 B、分解反应 C、置换反应 D、复分解反应 -
16、研究人员在金星大气中探测到了磷化氢()气体、常作为一种熏蒸剂,在贮粮中用于防治害虫,一种制备的流程如图所示。下列说法正确的是
 A、上述流程中每一步均属于氧化还原反应 B、白磷与浓氢氧化钠反应中氧化剂和还原剂的质量比是3:1 C、已知次磷酸()为一元酸,则次磷酸钠()属于正盐 D、1个次磷酸分解时转移4个电子
A、上述流程中每一步均属于氧化还原反应 B、白磷与浓氢氧化钠反应中氧化剂和还原剂的质量比是3:1 C、已知次磷酸()为一元酸,则次磷酸钠()属于正盐 D、1个次磷酸分解时转移4个电子 -
17、某白色粉末中可能含有Ba(NO3)2、CaCl2、Na2CO3 , 现进行以下实验:
(1)将部分粉末加入水中,振荡,有白色沉淀生成;
(2)向(1)中的悬浊液中加入过量稀硝酸,白色沉淀消失, 并有气泡产生;
(3)取少量(2)的溶液滴入AgNO3溶液,有白色沉淀生成。
根据上述现象判断,下列说法中不正确的是
A、原白色粉末中肯定含有Na2CO3 B、原白色粉末中肯定含有CaCl2 C、实验(1)后的溶液中肯定不含Na2CO3 D、根据以上实验无法确定原白色粉末中是否含有Ba(NO3)2 -
18、下列反应中水既不是氧化剂又不是还原剂的氧化还原反应是A、Cl2+H2OHCl+HClO B、2Na+2H2O=2NaOH+H2↑ C、2F2+2H2O=4HF+O2 D、SO3+H2O=H2SO4
-
19、下列关于物质分类的正确组合是
分类组合
电解质
非电解质
碱
酸性氧化物
A
H2O
葡萄糖
纯碱
CO2
B
稀盐酸
乙醇
Ca(OH)2
SO2
C
KOH
液氯
Fe(OH)3
P2O5
D
BaSO4
CO2
NaOH
SO2
A、A B、B C、C D、D -
20、下列说法错误的是
 A、图1表示干燥的NaCl固体不导电,分析其原因是Na+、Cl-这些离子不能自由移动 B、图2表示熔融的NaCl能导电,分析其原因是随温度升高,离子运动加快,克服了离子间的相互作用,产生了自由移动的离子 C、图3表示NaCl溶液能导电,分析其原因是在水分子的作用下NaCl电离出了自由移动的离子 D、图2和图3说明NaCl固体溶于水和受热熔化时,均发生了电离,产生了完全相同的离子
A、图1表示干燥的NaCl固体不导电,分析其原因是Na+、Cl-这些离子不能自由移动 B、图2表示熔融的NaCl能导电,分析其原因是随温度升高,离子运动加快,克服了离子间的相互作用,产生了自由移动的离子 C、图3表示NaCl溶液能导电,分析其原因是在水分子的作用下NaCl电离出了自由移动的离子 D、图2和图3说明NaCl固体溶于水和受热熔化时,均发生了电离,产生了完全相同的离子