相关试卷
-
1、一定温度下,在2L恒容密闭容器中发生反应 , 反应过程中的部分数据如下表所示:
t/min
n (N2)/mol
n (H2)/mol
n (NH3)/mol
0
2.0
24
0
5
1.7
1.5
0.6
10
1.6
x
y
15
z
1.2
w
下列说法错误的是( )
A、升高温度、增大N2的浓度均可加快反应速率 B、内用NH3表示的平均反应速率为 C、时,反应已达到平衡状态 D、当混合气体的平均相对分子质量不变时,反应达到平衡 -
2、下列选项中的操作及现象与原因或结论不对应的是( )
选项
操作及现象
原因或结论
A
向中加入 , 产生气泡的速率加快
降低了反应所需的活化能
B
向溶液中加入溶液,溶液呈红色,再滴加几滴的溶液,溶液颜色变浅
增大生成物浓度,平衡向逆反应方向移动
C
将盛有气体的密闭容器浸泡在热水中,容器内气体颜色变深
, 平衡向生成方向移动
D
在密闭容器中发生反应: , 加压,气体颜色变深
增大压强,平衡不移动,但增大
A、A B、B C、C D、D -
3、常温下,向氨水中滴入的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知氨水的电离度为1.62%,下列有关叙述正确的是( )
 A、用量筒量取氨水 B、可根据该反应过程中放出的热量计算中和反应反应热 C、M点对应的盐酸体积为 D、N点处的溶液中
A、用量筒量取氨水 B、可根据该反应过程中放出的热量计算中和反应反应热 C、M点对应的盐酸体积为 D、N点处的溶液中 -
4、次氯酸(HClO)和亚氯酸(HClO2)是两种常见的弱酸,常温时的 , 的。现将pH和体积都相同的次氯酸溶液和亚氯酸溶液分别加蒸馏水稀释,pH随溶液体积的变化如图所示。下列叙述正确的是( )
 A、曲线Ⅰ为次氯酸稀释时pH变化曲线 B、取a点的两种酸溶液,中和相同体积、相同浓度的溶液,消耗亚氯酸的体积较小 C、b点溶液中水的电离程度比c点溶液中水的电离程度小 D、从b点到d点,溶液中保持不变(HR代表或)
A、曲线Ⅰ为次氯酸稀释时pH变化曲线 B、取a点的两种酸溶液,中和相同体积、相同浓度的溶液,消耗亚氯酸的体积较小 C、b点溶液中水的电离程度比c点溶液中水的电离程度小 D、从b点到d点,溶液中保持不变(HR代表或) -
5、对于可逆反应 , 下列图像中正确的是( )




A.反应体系中X的体积分数与时间的关系图
B.正逆反应速率与温度的关系图
C.不同温度下X的转化率与时间的关系图
D.正逆反应速率与压强的关系图
A、A B、B C、C D、D -
6、根据酸碱质子理论,给出质子(H+)的物质是酸,给出质子的能力越强,酸性越强;结合质子的物质是碱,结合质子能力越强,碱性越强。下表是常温下几种弱酸的电离常数:
依据上表数据,下列说法正确的是( )
A、酸性强弱顺序: B、向溶液中滴加少量溶液,发生反应生成和 C、根据酸碱质子理论,碱性强弱顺序: D、向溶液中通入足量的可生成大量的气体 -
7、如图所示的实验装置中烧杯内分别盛有以下4种溶液各:①自来水,②的盐酸,③的醋酸,④的溶液,如果将固体分别加入上述溶液中,灯泡亮度没有明显变化的是( )
 A、①② B、②④ C、③④ D、②③
A、①② B、②④ C、③④ D、②③ -
8、下列有关水的电离与pH的说法正确的是( )A、的溶液一定呈中性 B、温度升高,纯水中增大,显酸性 C、盐酸抑制水的电离,醋酸促进水的电离 D、常温下,的醋酸,其
-
9、常温下足量锌粒与稀硫酸发生反应: , 下列操作或加入的试剂能够加快反应速率但不影响生成的总量的是( )A、升高温度 B、增大压强 C、加入盐酸 D、加入溶液
-
10、含硫物质在医药、农业、能源等领域都有广泛的应用,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如图所示:

下列说法正确的是( )
A、反应Ⅰ、Ⅱ、Ⅲ均为放热反应 B、储能过程中被消耗 C、存储的能量不可能完全转化为电能 D、循环过程中为储能物质 -
11、下列叙述错误的是( )A、由正丁烷(g)→异丁烷(g) △H<0可知,异丁烷比正丁烷稳定 B、常温下,用铁分别与浓、稀硫酸反应探究浓度对化学反应速率的影响 C、冰在室温下自动熔化成水,这是熵增的过程 D、合成氨工业生产中原料气需净化以防止催化剂“中毒”
-
12、生活离不开化学。生活中的下列做法与化学反应速率控制无关的是( )A、夏天将食物保存在冰箱中 B、食品抽真空包装 C、加工馒头时加入碳酸氢钠 D、洗衣服时使用加酶洗衣粉
-
13、我国科学家从土曲霉中发现了一种抗阿尔茨海默症效果良好的药物,其中间体化合物IX的合成路线如下(部分反应条件省略):
 (1)、化合物Ⅰ中的含氧官能团的名称为。(2)、化合物Ⅰ还可与化合物M在一定条件下反应,生成化合物Ⅱ,原子利用率为100%,M的化学式为。(3)、在分子组成上比化合物Ⅳ()少的化合物N有多种同分异构体,能发生银镜反应且属于芳香族化合物的有种,其中核磁共振氢谱有4组峰的结构简式为(任写一种)。(4)、根据化合物Ⅴ的结构特征,分析预测其可能的化学性质,完成下表。
(1)、化合物Ⅰ中的含氧官能团的名称为。(2)、化合物Ⅰ还可与化合物M在一定条件下反应,生成化合物Ⅱ,原子利用率为100%,M的化学式为。(3)、在分子组成上比化合物Ⅳ()少的化合物N有多种同分异构体,能发生银镜反应且属于芳香族化合物的有种,其中核磁共振氢谱有4组峰的结构简式为(任写一种)。(4)、根据化合物Ⅴ的结构特征,分析预测其可能的化学性质,完成下表。序号
反应试剂、条件
反应形成的新结构
反应类型
a
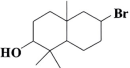
b
浓 , 加热
消去反应
(5)、下列与反应⑦相关的描述不正确的有____(填标号)。A、反应过程中,有断裂和键形成 B、中的空间结构为正四面体形 C、化合物Ⅶ和Ⅷ的分子中均含有手性碳原子 D、化合物Ⅶ分子中,存在由p轨道“头碰头”形成的键(6)、参照上述合成路线,请设计以 为主要原料合成
为主要原料合成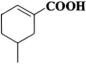 的路线(不用注明反应条件)。
的路线(不用注明反应条件)。 -
14、用“氧化-萃取法”可从卤水中提取碘,其方法为向酸化的卤水中加入溶液,再加入萃取剂(R)进行萃取。该过程涉及以下反应:
(ⅰ)
(ⅱ)
(ⅲ)
(1)、根据盖斯定律,反应 。(2)、基态碘原子价层电子的轨道表示式为。(3)、①反应条件会影响碘的萃取率。其他条件不变时,不同温度下达平衡时碘萃取率]曲线如图所示: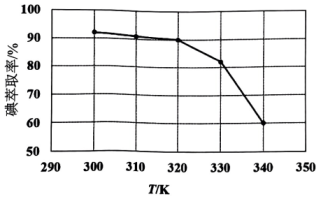
萃取温度从300K升高至320K,碘萃取率缓慢下降。结合平衡移动原理,分析其原因(忽略萃取剂的挥发、的挥发及分解产生的影响)。当萃取温度超过320K时,的分解导致碘萃取率明显下降。
②下列说法不正确的是(填标号)。
A.增大溶液的pH,碘萃取率降低 B.增大萃取剂用量,碘萃取率升高
C.萃取体系平衡后加水稀释,变小 D.增大的浓度,反应(ⅰ)的速率增大
(4)、未加萃取剂时,固定总碘浓度为 , 平衡时溶液中的、、分布系数与溶液中初始关系如图所示。[总碘浓度=各组分折合为后的浓度之和, , 如]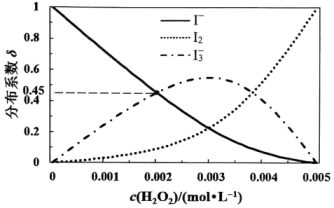
①设平衡时、、分别为、、 , 则a、b、c之间的关系式为=0.01。
②计算反应的平衡常数(结果保留3位有效数字)。
(5)、测定卤水中的方法:取25.00mL卤水于锥形瓶中,加适量氧化剂恰好将全部氧化为加溶液酸化后,再加入适量KI溶液,密闭静置后,用标准溶液滴定至溶液呈微黄色,加入淀粉指示剂,继续滴定至终点;平行测定3次,平均消耗 , 则卤水中。(已知:) -
15、锆被称为原子时代的头号金属。一种以氧氯化锆(主要含 , 还含有少量Fe、Cr、Hf等元素)为原料生产金属锆的工艺流程如下:

已知:
①“酸溶”后溶液中各金属元素的存在形式为:、、、;
②25℃时, , ;
③部分易升华物质在接近沸点时升华速率较快。“加氢还原”前后相关物质沸点如下:
物质
沸点/℃
331
315
1300
700
1150
回答下列问题:
(1)、“酸溶”后,Hf元素的化合价为。(2)、“萃取”时,锆元素可与萃取剂形成多种络合物,写出生成的离子方程式:。(3)、“沉淀”后,“废液”中 , 则“废液”中。(4)、“沸腾氯化”时,转化为 , 同时生成一种还原性气体,该反应的化学方程式为。(5)、①“还原”的主要目的是。②沸点远低于的可能原因为。
(6)、某种掺杂CaO的晶胞如图所示,Ca位于晶胞的面心。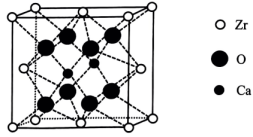
①晶体中每个O周围与其最近的O个数为。
②已知该晶胞为立方晶胞,晶胞中O与Zr的最小间距为anm,设为阿伏加德罗常数的值,该晶体的密度为(列出计算式)。
③如图所示结构(
 -Zr
-Zr  -O
-O  -Ca)与上述晶胞结构不一致的是(填标号)。
-Ca)与上述晶胞结构不一致的是(填标号)。A.
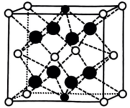 B.
B.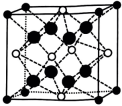
C.
 D.
D.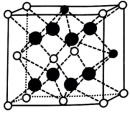
-
16、实验室利用以铜为电极电解稀溶液的方法测定的值。(1)、Ⅰ.电解液的配制:
将溶液配制为溶液。①量取浓时,适宜的量筒规格为(填标号)。
A.10mL B.25mL C.50mL D.100mL
②配制溶液时,进行如下操作:
溶解→冷却→操作ⅰ→洗涤→注入→混匀→定容→操作ⅱ→装瓶贴标签下图、(填标号)所示操作依次为操作ⅰ、操作ⅱ。
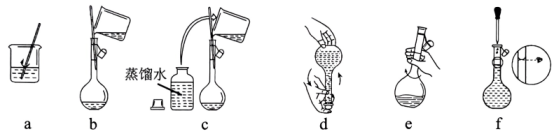 (2)、Ⅱ.值的测定:通过测定阳极铜片质量的变化量和通过电路的电量Q , 结合两者之间的关系进行计算(已知:一个电子的电量为q , )。
(2)、Ⅱ.值的测定:通过测定阳极铜片质量的变化量和通过电路的电量Q , 结合两者之间的关系进行计算(已知:一个电子的电量为q , )。在20℃、101kPa下,电流为0.2A,以精铜片为电极,电解溶液,10min后关闭电源。观察和测量结果如下:
a.阳极上有少量气泡产生,且铜片质量减少mg;
b.阴极上有大量气泡产生;
c.电解质溶液变蓝。
①为准确测量,电解前需将已除去油污的铜片 , 并用蒸馏水洗净擦干后再称重。
②经检验,阳极上产生的气体为 , 电极反应为;该副反应的发生,可能导致的测定值比其理论值(填“偏大”或“偏小”)。
(3)、为避免阳极副反应的发生,探究实验条件的影响。查阅资料:电解过程中,电解电压低将导致反应速率慢,电压高则易引发电极副反应。电流强度相同时,电压与电解质溶液的浓度成反比。
提出猜想:猜想ⅰ:电流强度越大,越容易引发电极副反应。
猜想ⅱ:硫酸浓度越低,越容易引发电极副反应。
进行实验:其他条件相同时,进行如下表实验,利用电流传感器测定通过电路的电量Q , 并测算3min内阳极铜片质量的减少量。
实验编号
理论电流I/A
实测电量Q/C
溶液的体积/mL
蒸馏水的体积/mL
阳极铜片减少的质量/g
1
0.1
18.33
a
0
0.0060
2
0.1
18.34
20
180
0.0055
3
0.2
36.70
b
c
0.0095
4
0.3
55.02
20
180
0.0130
①根据表中信息,补充数据:a= , b=。
②由实验2、3和4可知,猜想ⅰ成立,结合表中数据,给出判断理由:。
③根据实验1~4相关数据,由实验(填实验编号)测算的值误差最小。
实验结论:
④根据最优实验条件的数据计算,(已知:)。
-
17、常温下,向某溶剂(不参与反应)中加入一定量X、Y和M,所得溶液中同时存在如下平衡:(ⅰ)(ⅱ)(ⅲ)X、Y的物质的量浓度c随反应时间t的变化关系如图所示,300s后反应体系达到平衡状态。下列说法正确的是( )
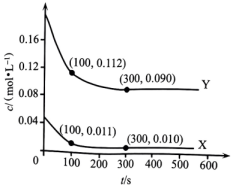 A、100~300s内, B、时,反应(ⅲ)的逆反应速率大于正反应速率 C、若反应(ⅲ)的 , 则X比Y更稳定 D、若再向容器中加入上述溶剂,则、均不变
A、100~300s内, B、时,反应(ⅲ)的逆反应速率大于正反应速率 C、若反应(ⅲ)的 , 则X比Y更稳定 D、若再向容器中加入上述溶剂,则、均不变 -
18、我国科学家研发了一种由废水(含、等)提铀并同步产电的工艺,其工作原理和相关物质转化关系如图所示。下列有关该过程的说法不正确的是( )
 A、电子从Fe电极经导线流向CCF电极 B、CCF电极上发生的反应有: C、生成的反应中, D、利用电解法再次获得含溶液,需将附着、的电极置于阳极
A、电子从Fe电极经导线流向CCF电极 B、CCF电极上发生的反应有: C、生成的反应中, D、利用电解法再次获得含溶液,需将附着、的电极置于阳极 -
19、W、X、Y、Z是原子序数依次增大的主族元素,在前三周期均有分布。基态X原子有四种不同空间运动状态的电子;Y为地壳中含量最多的元素,其简单离子与Z的简单离子具有相同电子数;工业上常通过电解Z的氧化物制取其单质。下列说法不正确的是( )A、元素电负性:Y>X>Z B、简单氢化物的沸点:Y>X C、原子半径:X>Y>W D、与Z同周期且第一电离能小于Z的元素有2种
-
20、光催化氧化甲烷制甲醛的机理如图所示。设为阿伏加德罗常数的值。下列说法不正确的是( )
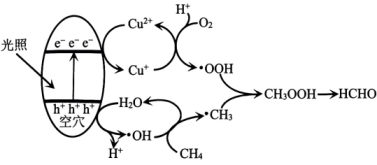 A、在光催化剂表面会发生反应 B、为中间产物 C、上述过程中有非极性键的断裂与生成 D、每生成30gHCHO,总反应转移电子数目为
A、在光催化剂表面会发生反应 B、为中间产物 C、上述过程中有非极性键的断裂与生成 D、每生成30gHCHO,总反应转移电子数目为