相关试卷
-
1、回答下列问题:(1)、①金刚砂的主要成分的化学式是。(2)、分子的空间结构为 , 共价键为键(填“极性”或“非极性”)(3)、比较还原性强弱:(填“>”“<”或“=”);用一个离子方程式说明与与的还原性相对强弱。(4)、科学家已获得了气态分子,其结构为正四面体。已知断裂1molN-N吸收193kJ能量,断裂1molN≡N吸收946kJ能量,则完全转化为时(填“吸收”或“放出”)能量

-
2、下列实验目的、操作、现象及结论合理的是( )
实验目的
实验操作
现象及结论
A
比较与氧化性强弱
取少量溶液于试管中,滴入硫酸酸化的溶液
溶液由浅绿色变为黄色氧化性:
B
比较Mg与Al金属性强弱
向同浓度等体积的、溶液中分别滴加同浓度的过量的NaOH溶液
溶液中有白色沉淀生成且不溶解,溶液中有白色沉淀生成后溶解,则金属性:Mg>Al
C
检验溶液中是否含有
向溶液中滴加酸性溶液
若紫红色退去,则溶液中含有
D
检验溶液中是否含有
取少量溶液于试管中,滴加稀盐酸
若产生的气体能使澄清石灰水变浑浊,则溶液中含有
A、A B、B C、C D、D -
3、溶液X中含有下表中离子若干种,且离子浓度均为相等(不考虑水的电离与离子水解)。向X中加入足量稀盐酸,有气体生成,经分析反应前后阴离子种类没有变化,下列说法正确的是( )
阳离子
、、、、、
阴离子
、、、、、
A、溶液X中一定有 B、原溶液一定没有、 , 但、不确定 C、溶液X中可能有或中的一种或两种都有 D、溶液X中至少1种阳离子,2种阴离子,最多2种阳离子,3种阴离子 -
4、下列选项描述与对应图像相符的是( )
①
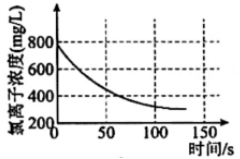 ②
②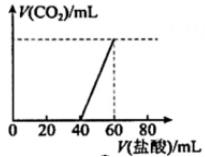 ③
③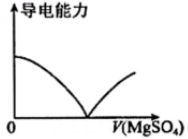 ④
④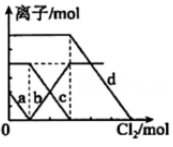 A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为、NaOH混合液中滴加盐酸产生的图像,且 C、图③为溶液中滴加溶液的导电性变化图像,导电能力约为0的原因是两者恰好完全反应且生成物都不是电解质 D、图④为、混合液,各离子物质的量随氯气通入的变化图像,c代表的是
A、图①为新制氯水在阳光直射时,溶液中浓度随着时间变化的曲线 B、图②为、NaOH混合液中滴加盐酸产生的图像,且 C、图③为溶液中滴加溶液的导电性变化图像,导电能力约为0的原因是两者恰好完全反应且生成物都不是电解质 D、图④为、混合液,各离子物质的量随氯气通入的变化图像,c代表的是 -
5、将20.6gAl、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体6.72L(标况)。另取等质量的合金溶于过量的稀硝酸中生成8.96L(标况)NO,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量是( )A、25.4g B、41.0g C、30.8g D、28.3g
-
6、合成氨及其衍生物工业是化工生产的重要门类,请结合图示判断下列说法正确的是( )
 A、湿润的淀粉-KI试纸可以鉴别气体2和溴蒸气 B、饱和NaCl溶液中先通入过量再通入过量可以得到固体1 C、1L气体1、2的混合气与在一定条件下转化为对坏境无害的物质,混合气中二者的体积比为1:1 D、气体2能与水反应生成故气体2是酸性氧化物
A、湿润的淀粉-KI试纸可以鉴别气体2和溴蒸气 B、饱和NaCl溶液中先通入过量再通入过量可以得到固体1 C、1L气体1、2的混合气与在一定条件下转化为对坏境无害的物质,混合气中二者的体积比为1:1 D、气体2能与水反应生成故气体2是酸性氧化物 -
7、由一种阳离子与两种酸根阴离子组成的盐称为混盐,是一种常见的混盐。下列说法不正确的是( )A、有较强的氧化性 B、有类似于漂白粉的性质,也是混合物 C、由氯气为原料,每生成 , 转移的电子为1mol D、的溶液中加入足量浓硫酸,可有黄绿色的气体产生
-
8、关于反应: , 下列说法正确的是( )A、若有参加反应,则生成 B、中氮元素为-1价 C、氧化产物与还原产物的物质的量之比为15:1 D、若参加反应,转移电子的物质的量为10mol
-
9、下列离子方程式书写正确的是( )A、大理石与稀硝酸反应: B、碳酸氢钠溶液和过量的澄清石灰水混合: C、少量通入溶液中: D、过量铁粉投入稀硝酸中:
-
10、向用盐酸酸化的溶液中加入溶液,产生的沉淀质量m与加入的体积V之间的关系,不可能是下图中的( )A、
 B、
B、 C、
C、 D、
D、
-
11、下列“类比”合理的是( )A、和反应是氧化还原反应,则BrCl和反应生成HBrO和HCl也是氧化还原反应 B、Mg、Al与浓盐酸构成的原电池中较活泼的Mg作负极,故Mg、Al与氢氧化钠构成的原电池中也是Mg作负极 C、与能反应生成S,故与能在一定条件下反应生成 D、中Cl的化合价为+1价,则中F的化合价为+1价
-
12、短周期元素W、X、Y、Z和Q在周期表中的相对位置如表所示,这五种元素原子的最外层电子数之和为24。下列说法正确的是( )
W
X
Q
Y
Z
A、简单氢化物稳定性:X<W B、氧化物对应水化物的酸性:Z>W C、Y的氧化物和W单质在高温下反应生成Y单质,可以说明非金属性W>Y D、简单离子的半径:Q<X -
13、设为阿伏加德罗常数的值,下列说法正确的是( )A、1mol/L的溶液中所含数目为 B、(离子化合物)中含有的共价键数目为 C、标况下和组成的混合物中含有氧原子的数目为 D、与足量反应转移的电子数目为
-
14、下列说法正确的是( )A、由于固态水中水分子以氢键结合成排列规整的晶体,所以冰的密度比水小 B、N、H、O三种元素组成的化合物一定只含共价键 C、NaOH和中的化学键类型完全相同,都属于离子化合物 D、和分子中,各原子均满足最外层8电子的稳定结构
-
15、为除去括号内少量的杂质,所用的试剂或方法正确的是( )A、Fe粉(Cu粉):盐酸,过滤 B、:氧气,点燃 C、除去KCl溶液中的少量:加入适量NaOH溶液,过滤 D、:饱和碳酸氢钠溶液,洗气
-
16、下列实验操作或装置正确的是( )
 A、图甲可用于实验室制备 B、图乙装置可用于完成过滤操作 C、图丙可用于验证氨气在水中的溶解性 D、图丁表示为配制一定物质的量浓度NaOH溶液时称量溶质的操作
A、图甲可用于实验室制备 B、图乙装置可用于完成过滤操作 C、图丙可用于验证氨气在水中的溶解性 D、图丁表示为配制一定物质的量浓度NaOH溶液时称量溶质的操作 -
17、下列说法不正确的是( )A、储氢合金要求储氢量大,金属氢化物既容易形成,受热又不容易分解 B、二氧化硫可用于杀菌消毒,还是一种食品添加剂 C、中国华为集团自主研发的“麒麟”芯片生产时需要用到硅 D、硬铝是一种铝合金,是制造飞机和宇宙飞船的理想材料
-
18、下列说法正确的是( )A、当L层上的电子数为奇数时,M层上不可能有电子 B、同一主族中,相邻周期元素原子的核电荷数相差值一定为8或18或32 C、同一周期中,随着核电荷数的增加,元素的原子半径逐渐增大 D、同一周期中,ⅡA与ⅢA族元素原子的核电荷数都相差1
-
19、某兴趣小组以相同大小的铜片和锌片为电极研究水果电池,装置如图,实验所得数据如下:
实验编号
水果种类
电极间距离/cm
电流/μA
1
番茄
1
98.7
2
番茄
2
72.5
3
苹果
2
27.2
电池工作时,下列说法不正确的是( )
 A、负极的电极反应为 B、电子从锌片经水果流向铜片 C、化学能全部转化为电能 D、水果种类和电极间距离对电流的大小均有影响
A、负极的电极反应为 B、电子从锌片经水果流向铜片 C、化学能全部转化为电能 D、水果种类和电极间距离对电流的大小均有影响 -
20、在某透明的酸性溶液中,能大量共存的离子组是( )A、、、、 B、、、、 C、、、、 D、、、、