相关试卷
-
1、化学与科学、技术、社会、生活等密切相关。下列有关说法正确的是A、用于清洗伤口、杀菌、消毒的医用酒精有强氧化性 B、我国“神舟十二号”飞船返回舱的舱体外壳部件材料是由金属复合材料——专业的铝合金材料制成的,主要是利用了其硬度大的特性 C、食品袋中放置的CaO可直接防止食品氧化变质 D、客家围屋建造过程中用作黏稠剂的糯米和鸡蛋清都属于混合物
-
2、明代《天工开物》中介绍了炉甘石(主要成分).按分类法,属于A、碱 B、化合物 C、酸 D、氧化物
-
3、在固体、熔融状态、溶于水三种状态下的导电实验,如图所示
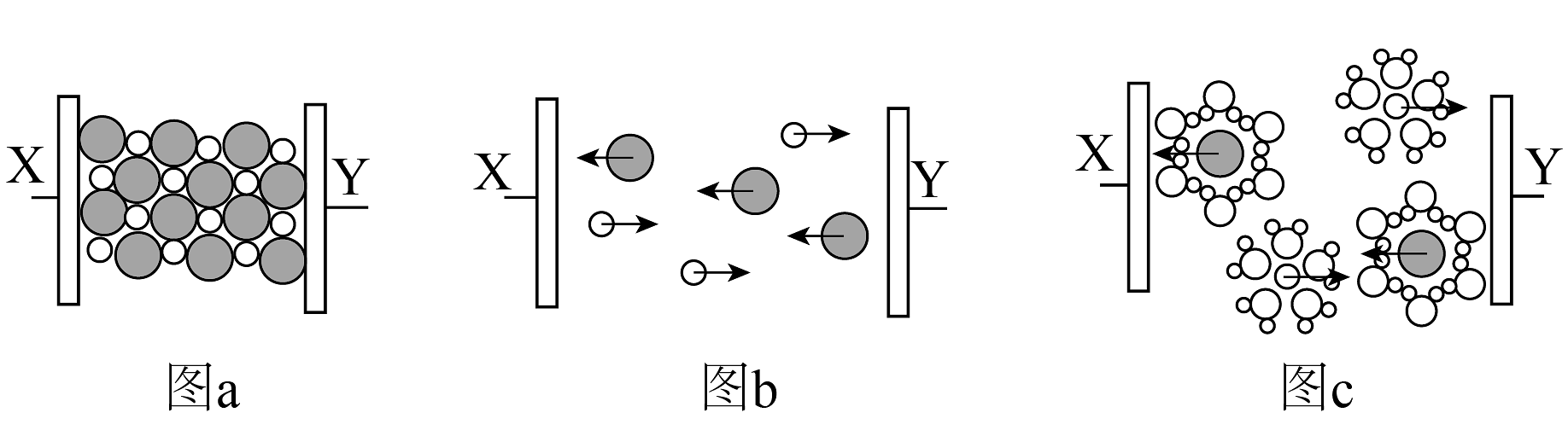
下列说法正确的是
A、固体中不存在离子,不能导电 B、通电情况下才能电离 C、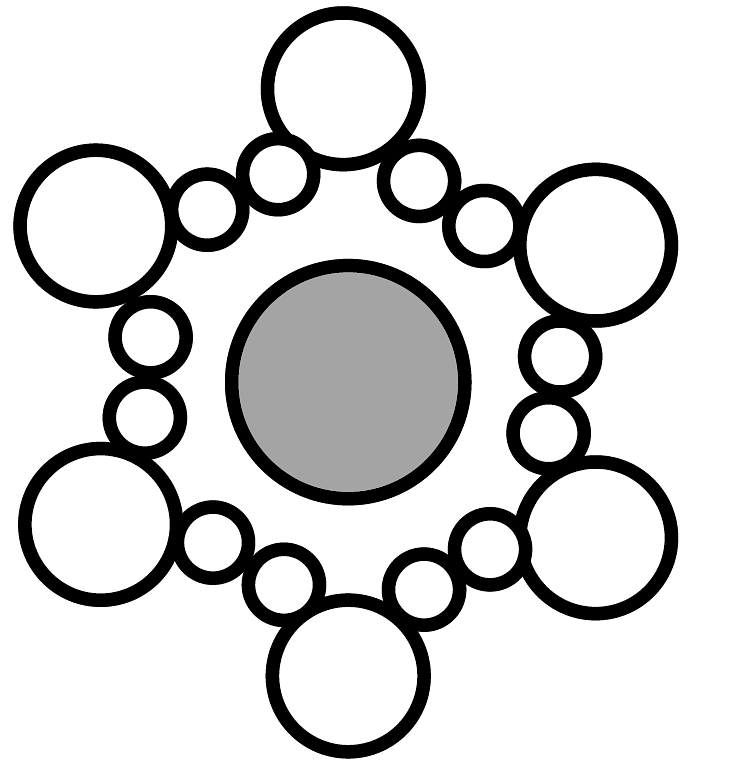 表示水合氯离子
D、、、分别溶于少量的水后,都有明显的放热现象
表示水合氯离子
D、、、分别溶于少量的水后,都有明显的放热现象
-
4、常温下,向溶液中逐滴加入0.1mol/L的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化关系如图所示。下列说法不正确的是
 A、a点的 B、反应过程中的值不断增大 C、c点时, D、b点时,
A、a点的 B、反应过程中的值不断增大 C、c点时, D、b点时, -
5、已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,在酸性溶液中的还原性顺序为:SO2>I->Fe2+>H2O2>Cl- , 则下列反应不可能发生的是A、2Fe3++SO2+2H2O=2Fe2++SO+4H+ B、2Fe2++I2=2Fe3++2I- C、I2+SO2+2H2O=H2SO4+2HI D、H2O2+SO2=H2SO4
-
6、青蒿素是高效的抗疟疾药,为无色针状晶体,易溶于丙酮、氯仿和苯中,甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为156-157℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为:

下列有关此工艺操作不正确的是
A、破碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率 B、操作I需要用到的玻璃仪器有漏斗、玻璃棒、烧杯 C、操作II是蒸馏,利用了乙醚与青蒿素的沸点相差较大 D、操作III的主要过程加水溶解,蒸发浓缩、冷却结晶、过滤 -
7、如果ag某气体中含有的分子数为b,则cg该气体在标准状况下的体积是(式中为阿伏加德罗常数)A、 B、 C、 D、
-
8、硫化氢的转化是资源利用和环境保护的重要研究课题将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如图所示(CuS溶于水)。下列说法正确的是
 A、过程①中,Cu2+起催化剂作用 B、过程②中,发生反应为S2-+2Fe3+=S↓+2Fe2+ C、过程③中,氧气被还原 D、回收S的总反应为H2S+O2=H2O+S↓
A、过程①中,Cu2+起催化剂作用 B、过程②中,发生反应为S2-+2Fe3+=S↓+2Fe2+ C、过程③中,氧气被还原 D、回收S的总反应为H2S+O2=H2O+S↓ -
9、下列图示实验装置和原理能达到实验目的的是
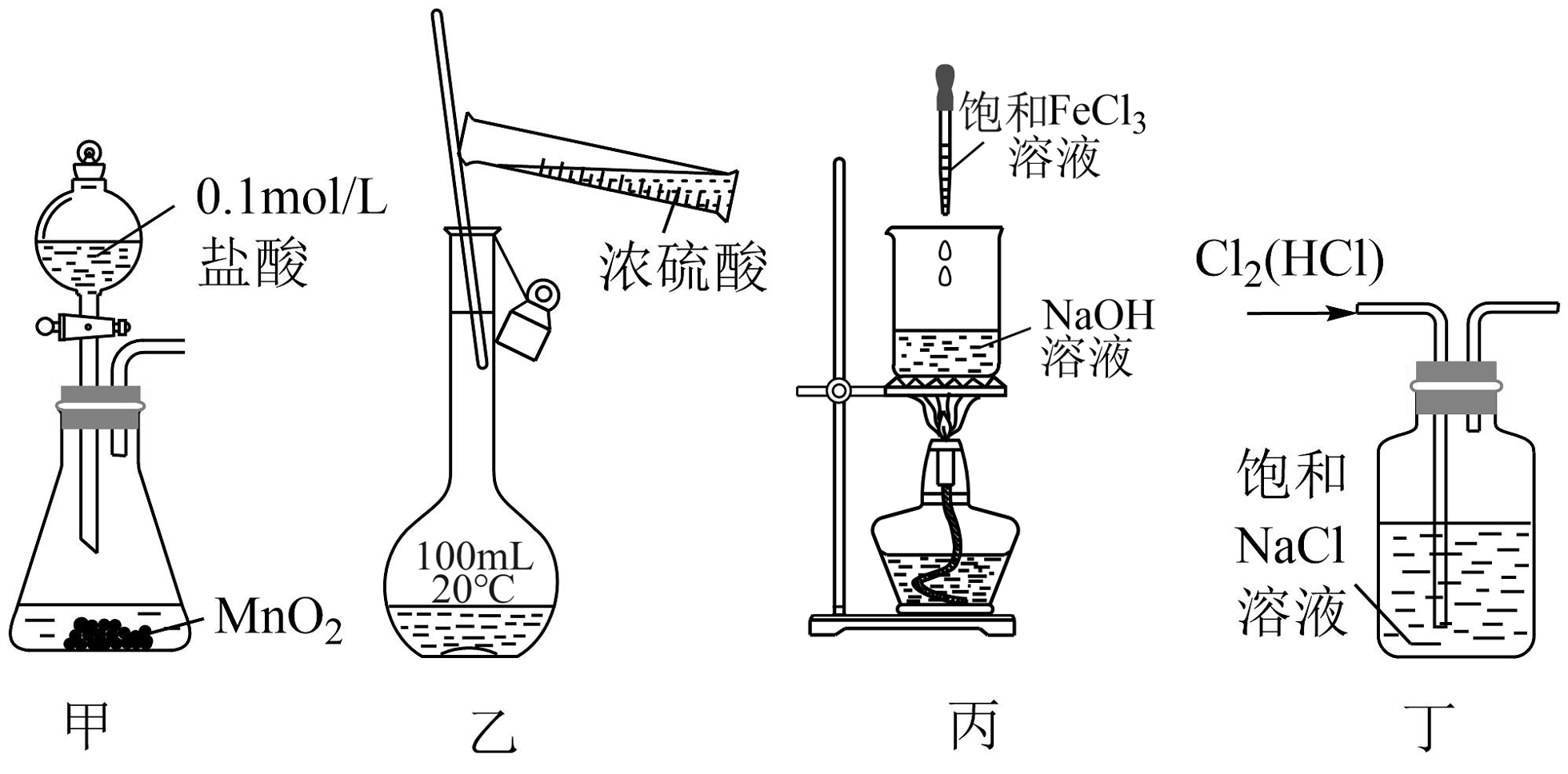 A、装置甲:实验室制取少量Cl2 B、装置乙:用浓硫酸配制一定物质的量浓度的稀硫酸 C、装置丙:制备氢氧化铁胶体 D、装置丁:除去氯气中混有的少量HCl
A、装置甲:实验室制取少量Cl2 B、装置乙:用浓硫酸配制一定物质的量浓度的稀硫酸 C、装置丙:制备氢氧化铁胶体 D、装置丁:除去氯气中混有的少量HCl -
10、下列关于Na2CO3和NaHCO3的性质说法正确的是A、碳酸氢钠晶体中加少量水会溶解,并伴有放热现象 B、碳酸钠溶液中逐滴滴加稀盐酸,开始无明显现象,一段时间后产生大量气泡 C、等物质的量的碳酸钠和碳酸氢钠固体分别与足量盐酸反应,相同条件下产生CO2体积后者多 D、可用澄清石灰水鉴别Na2CO3和NaHCO3溶液
-
11、下列有关描述对应的离子方程式书写正确的是A、食醋除去瓶胆内的水垢: B、碳酸氢钙溶液与过量的澄清石灰水混合: C、向中投入固体: D、乙醇被酸性溶液氧化成乙酸:
-
12、
将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一,煤转化为水煤气的主要化学反应为:。C(s)、CO(g)和完全燃烧的热化学方程式分别为:
① ;
② ;
③ 。
试回答:
(1)请你根据以上数据,写出C(s)与水蒸气反应生成CO和的热化学方程式:。(2)比较反应热数据可知,和完全燃烧放出的热量之和,比完全燃烧放出的热量(填“多”或“少”)。甲同学据此认为:“煤炭燃烧时加少量水,可以使煤炭燃烧放出更多的热量”。
乙同学根据盖斯定律作出了下列循环图
 (3)请你写出、、、之间存在的关系式。(4)乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是。
(3)请你写出、、、之间存在的关系式。(4)乙同学据此认为:“将煤转化为水煤气再燃烧放出的热量,最多与直接燃烧煤放出的热量相同。”请分析:甲、乙两同学的观点正确的是(填“甲”或“乙”)同学,另一同学出现错误观点的原因是。 -
13、超细氮化铝粉末被广泛应用于大规模集成电路生产等领域。其制取原理为: , 下列说法正确的是A、AlN是氧化产物 B、C在反应中被还原 C、Al2O3在反应中得到电子 D、生成1mol AlN时,转移3mol电子
-
14、25℃时,用0.1000mol/L的NaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的CH3COOH溶液和HCN溶液,所得滴定曲线如图。下列说法不正确的是
 A、点①和点②所示溶液中:c(CH3COO﹣)﹣c(CN﹣)═c(HCN)﹣c(CH3COOH) B、④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 C、HCN酸性比CH3COOH弱,所以点①溶液中水的电离程度小于点②溶液 D、点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣)
A、点①和点②所示溶液中:c(CH3COO﹣)﹣c(CN﹣)═c(HCN)﹣c(CH3COOH) B、④⑤为两个反应的滴定终点,两个反应均可采用酚酞作指示剂 C、HCN酸性比CH3COOH弱,所以点①溶液中水的电离程度小于点②溶液 D、点②和点③间(不含端点)存在离子浓度大小关系:c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) -
15、反应H2O2+H2S=2H2O+S中,氧化剂是A、H2O2 B、H2S C、H2O D、S
-
16、如图所示为氟利昂破坏臭氧层的过程,下列说法不正确的是
 A、过程Ⅳ中既有极性共价键的断裂又有非极性共价键的形成 B、整个过程可用方程式表示为 C、的电子式为
A、过程Ⅳ中既有极性共价键的断裂又有非极性共价键的形成 B、整个过程可用方程式表示为 C、的电子式为 D、上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂
D、上述过程说明氟利昂产生的氯原子是破坏臭氧层的催化剂
-
17、将图2中的物质补充到图1中,可得到一个氧化还原反应的离子方程式(未配平)。下列对该反应的说法不正确的是
 A、具有氧化性,在该反应中作氧化剂 B、发生了还原反应,每生成转移个电子 C、随着反应的进行,溶液酸性减弱 D、和的化学计量系数之比为
A、具有氧化性,在该反应中作氧化剂 B、发生了还原反应,每生成转移个电子 C、随着反应的进行,溶液酸性减弱 D、和的化学计量系数之比为 -
18、已知温度T时水的离子积常数为KW , 该温度下,将浓度为a mol·L-1的一元酸HA与b mol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是A、a=b B、混合溶液的pH=7 C、混合溶液中,c(H+)=mol.L-1 D、混合溶液中c(H+)+c(B+)=c(OH-)+c(A-)
-
19、下列变化一定不涉及电子转移的是A、天然气燃烧 B、用生石灰干燥氢气 C、食物变质 D、KClO3分解制氧气
-
20、下列离子在指定条件下的溶液中,一定能大量共存的是A、无色澄清溶液中:K+、Fe3+、SO、Mg2+ B、使石蕊变红色的溶液中:NO、Cl-、K+、SO C、含有大量Ba2+的溶液:NH、Na+、CO、I- D、加入Na2O固体的溶液中:Ba2+、Cu2+、NO、Cl-