相关试卷
-
1、在催化剂的作用下,利用合成气(主要成分为和)合成甲醇时涉及了如下反应:
I.
II.
III.
(1)、反应I在(填“高温”、“低温”或“任意温度”)下可自发进行。(2)、若向恒容密闭容器中按初始进料比投入反应物,只发生反应I和II。在不同温度下达到平衡,体系中的选择性和的平衡转化率与温度的关系如图(1)所示。
(已知:的选择性)
回答下列问题:
①某温度下,下列能说明反应II已达平衡状态的是(填序号)。
A.气体的平均摩尔质量不变
B.混合气体密度不再改变
C.体系中和的浓度比不变
D.容器内压强不再改变
②图中表示选择性变化的曲线是(填“a”或“b”)。
③当 , 平衡时的体积分数(答案保留两位有效数字),计算该温度下反应I的(用平衡分压代替平衡浓度,分压=总压各组分的物质的量分数,答案保留两位有效数字)。
④经测定,当温度高于的平衡转化率会升高,其可能的原因为。
(3)、某实验小组依据甲醇燃烧的反应原理,设计如图(2)所示的电池装置,写出该燃料电池负极的电极反应式:。
-
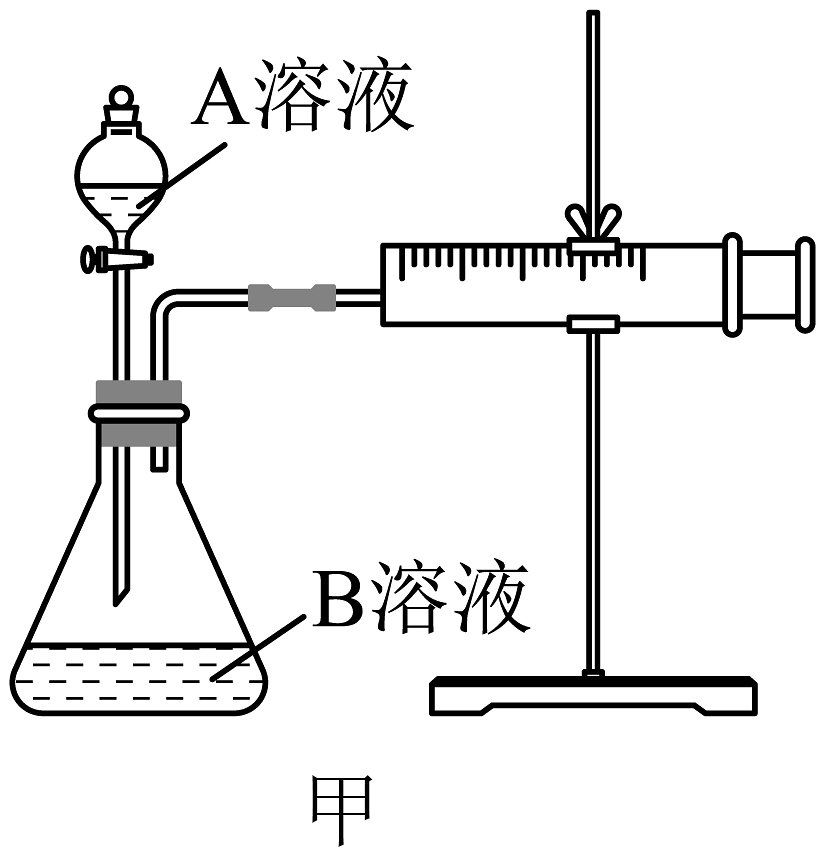
2、某实验小组欲通过测定酸性和(草酸)溶液在单位时间内生成的体积,来探究影响化学反应速率的因素,实验装置如图甲所示:
实验序号
A溶液
B溶液
①
溶液
溶液
②
溶液
溶液
回答下列问题:
(1)、检查装置甲气密性的方法。(2)、装置甲中发生反应的离子方程式为:。(3)、该实验探究的是因素对化学反应速率的影响。(4)、小组同学发现反应速率变化如图乙,其中时间内速率变快的主要原因可能是: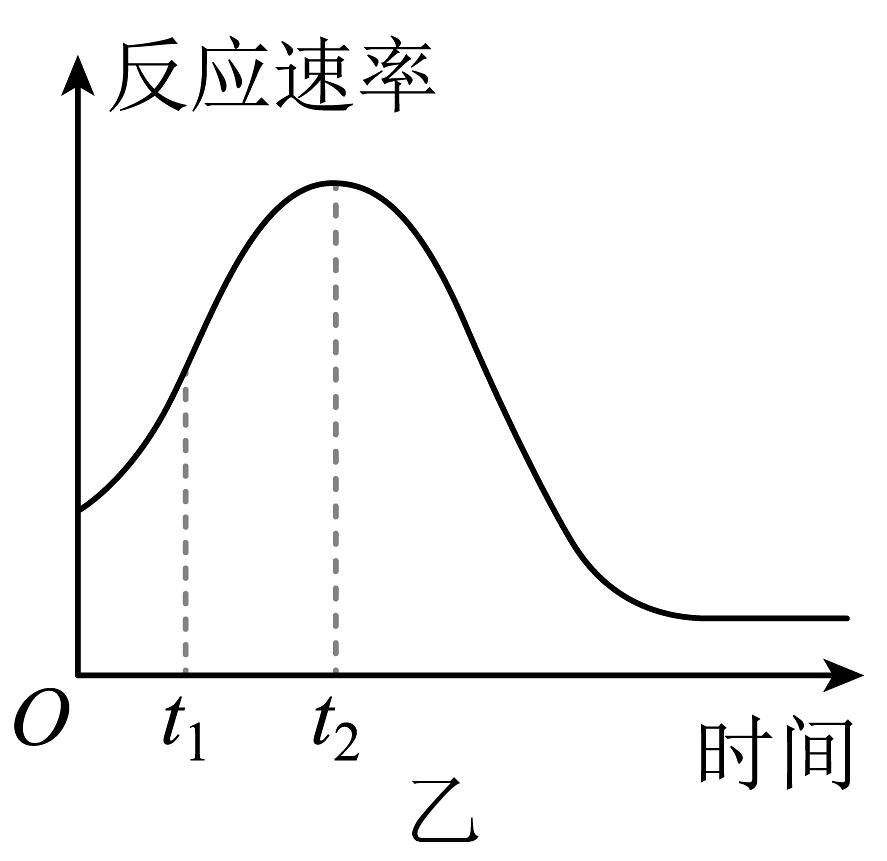
①产物是反应的催化剂;②。
-
3、氨气的性质非常广泛,以下是氨气的部分转化:
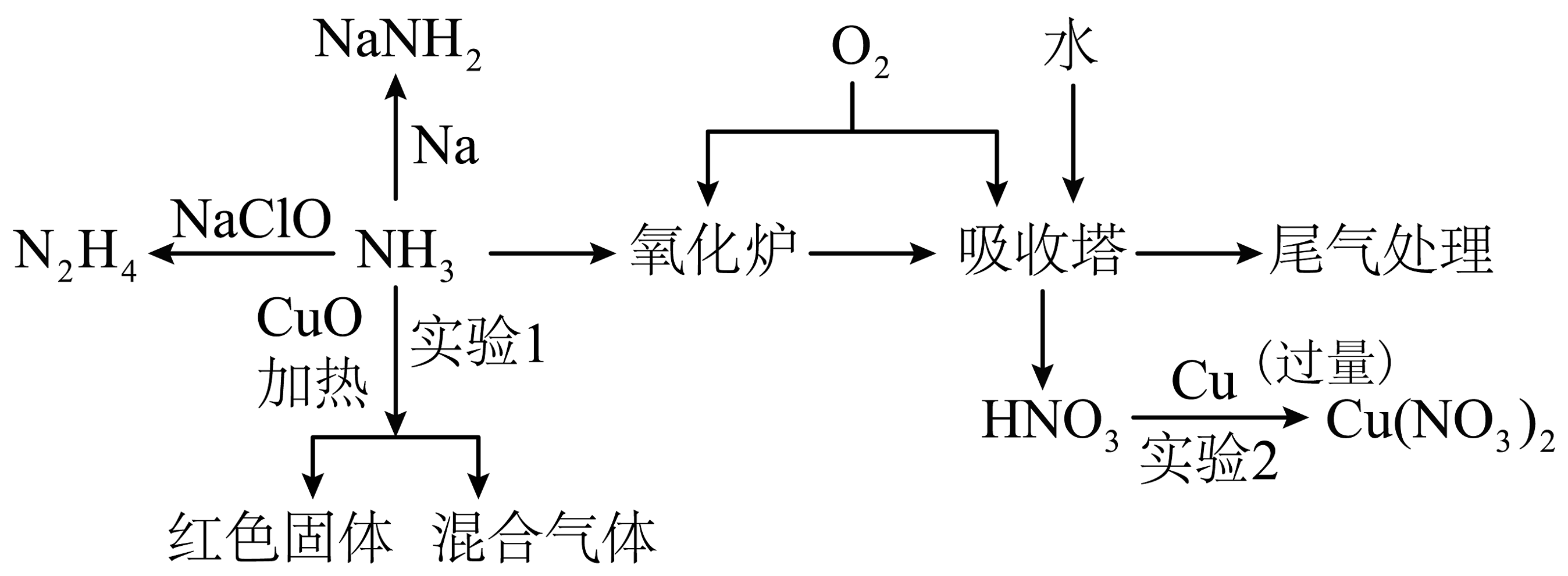
已知:肼又称联氨,还原性强于氨气。
(1)、请写出的电子式。(2)、N2H4可看成二元弱碱,请写出N2H4与足量硫酸生成酸式盐的化学式:。(3)、下列说法不正确的是。A.将投入液氨中制备
B.氨气存在分子间氢键,所以沸点高,是良好的制冷剂
C.为了提高的产量,需加入过量的
D.在氧化炉中直接生成 , 被水吸收后转化为硝酸
E.向实验2结束后的溶液中继续加入稀硫酸,可以观察到又有气泡产生
(4)、若实验2中产生的与体积比为3:1,请写出气体被溶液完全吸收的离子方程式:。(5)、已知实验1的混合气体中含有一种单质。设计用一种试剂(含试纸)验证反应后混合气体中比较活泼的两种气体的方案:。 -
4、下列装置可用于粗略测量物质的燃烧热。25℃时,将9克葡萄糖()放入该装置中充分燃烧,放出的热量能使燃烧室外5kg的水中温度计读数最高至31.7℃,已知水的比热容为。
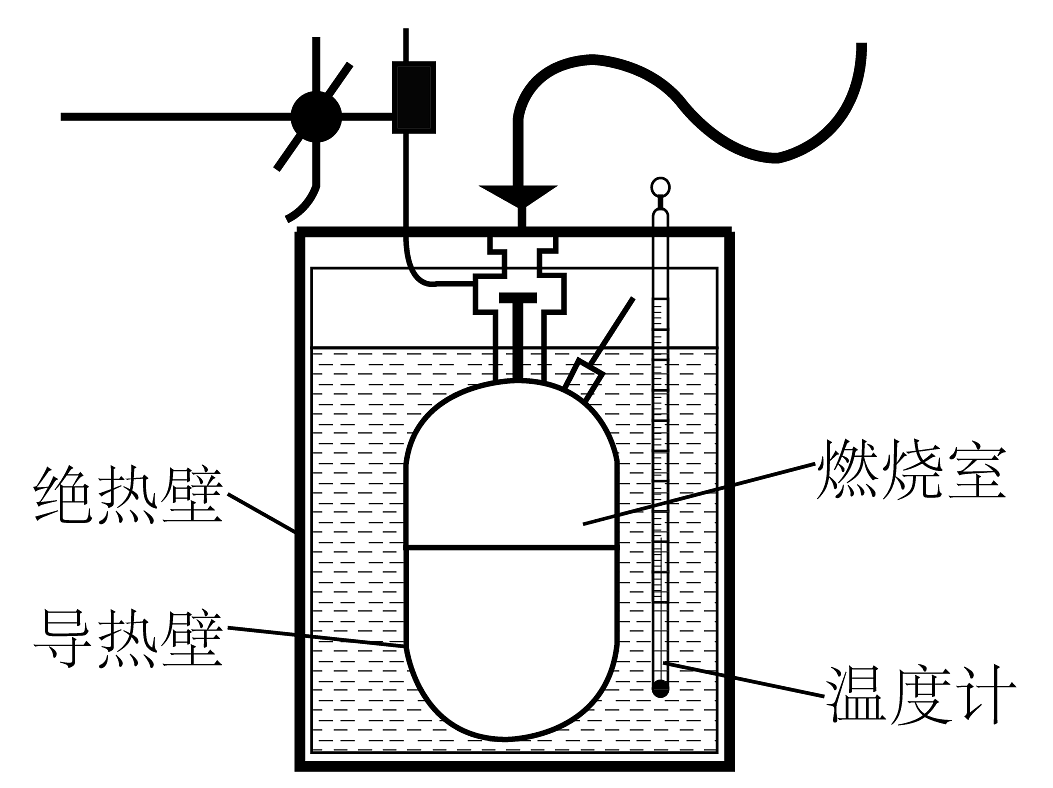 (1)、反应放出的热量Q=kJ(结果取整数)。(2)、写出葡萄糖燃烧热的热化学方程式。
(1)、反应放出的热量Q=kJ(结果取整数)。(2)、写出葡萄糖燃烧热的热化学方程式。 -
5、根据下列实验操作和现象所得出的结论正确的是
选项
实验操作
实验现象
实验结论
A
向含0.1molFeI2溶液中通入0.1molCl2 , 再滴加2滴淀粉溶液
溶液变蓝
还原性:Fe2+<I-
B
等体积等物质的量浓度的Na2S2O3与H2SO4溶液在不同温度下反应
温度高的溶液中先出现乳白色浑浊
升高温度,反应速率加快
C
向某固体中加入过量的盐酸,再滴加KSCN溶液
溶液未出现红色
该固体中不含+3价Fe元素
D
将红热的木炭放入浓硝酸中
产生红棕色气体
浓硝酸与碳在加热条件下生成NO2
A、A B、 C、 D、D -
6、向绝热恒容密闭容器中通入和 , 一定条件下反应:达到平衡,在此过程中正反应速率随时间变化的曲线如图所示。下列由图得出的结论正确的是
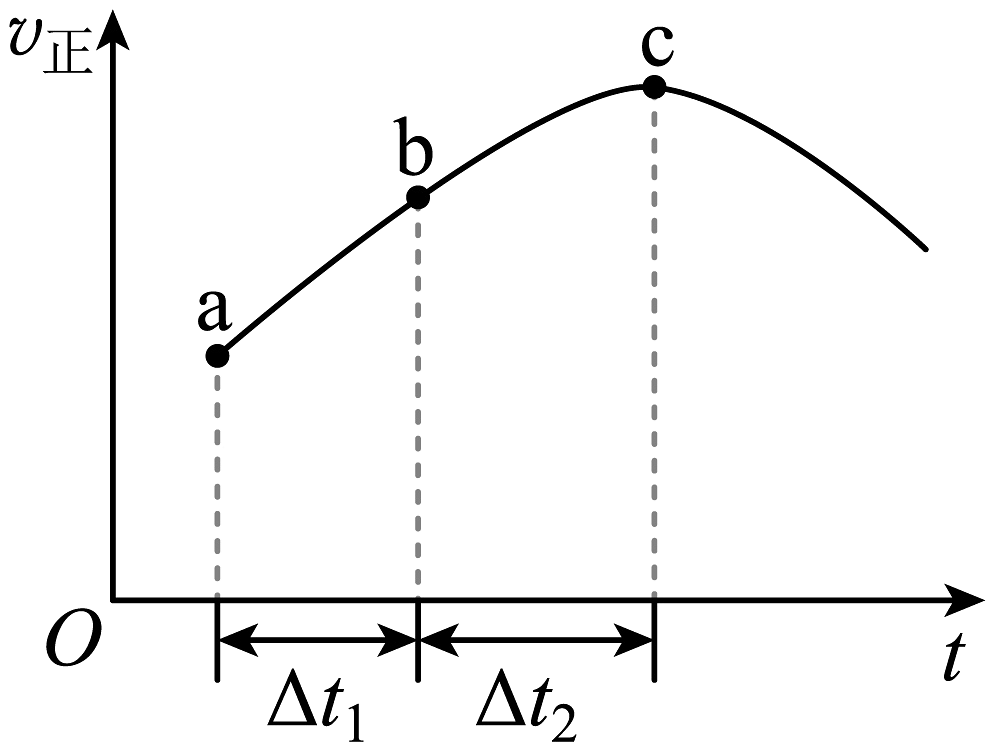 A、反应在点时达到平衡状态 B、反应物的总能量低于生成物的总能量 C、容器内的压强保持不变时,反应达到平衡状态 D、的浓度:点小于点
A、反应在点时达到平衡状态 B、反应物的总能量低于生成物的总能量 C、容器内的压强保持不变时,反应达到平衡状态 D、的浓度:点小于点 -
7、对于有机物:
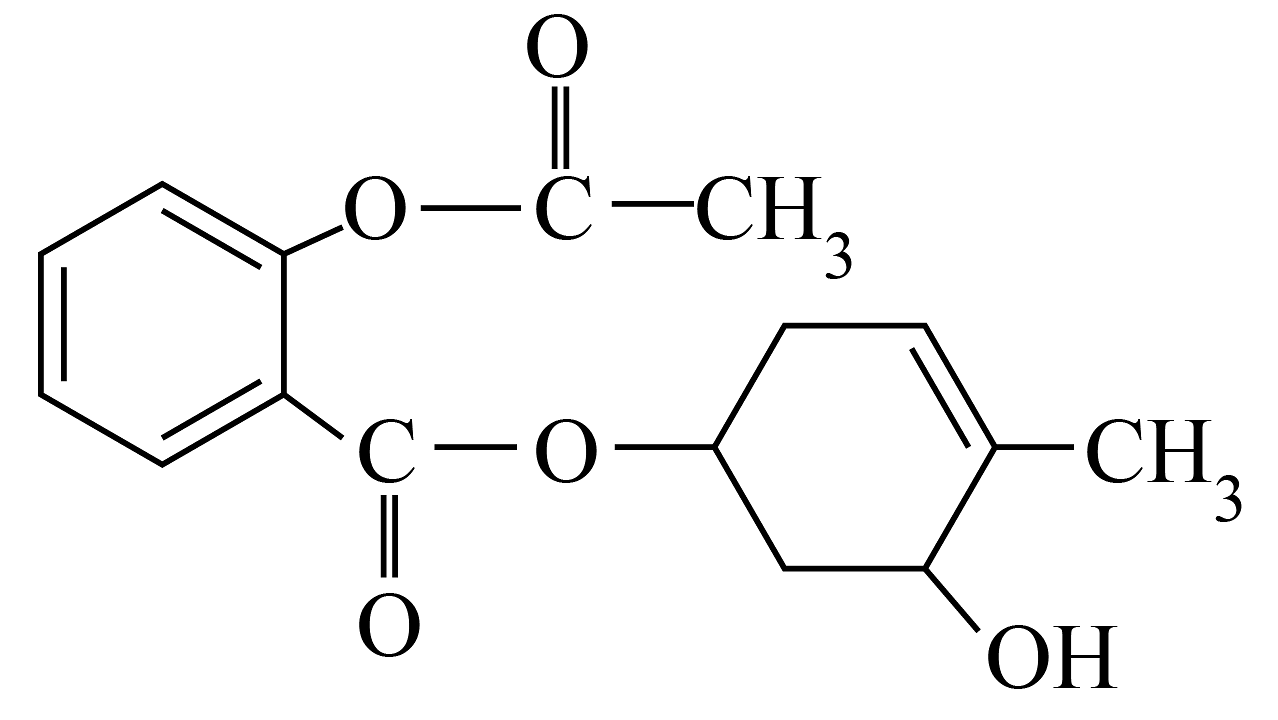 , 下列说法不正确的是 A、该有机物的分子式为: B、该有机物能发生加成、氧化、取代和加聚反应 C、该有机物最多能与氢气加成 D、该有机物能使酸性溶液褪色
, 下列说法不正确的是 A、该有机物的分子式为: B、该有机物能发生加成、氧化、取代和加聚反应 C、该有机物最多能与氢气加成 D、该有机物能使酸性溶液褪色 -
8、用绿矾()制备电池电极材料的流程如下:

下列说法正确的是
A、反应1中转化为 B、可用酸性溶液检验反应1中是否完全反应 C、可以使用KSCN溶液检验沉淀是否洗涤干净 D、反应2中氧化剂与还原剂的物质的量之比为2:1 -
9、甲醇与水蒸气重整可获得清洁能源,在催化剂作用下发生两步反应:
反应①:
反应②:
根据能量变化示意图,下列说法不正确的是
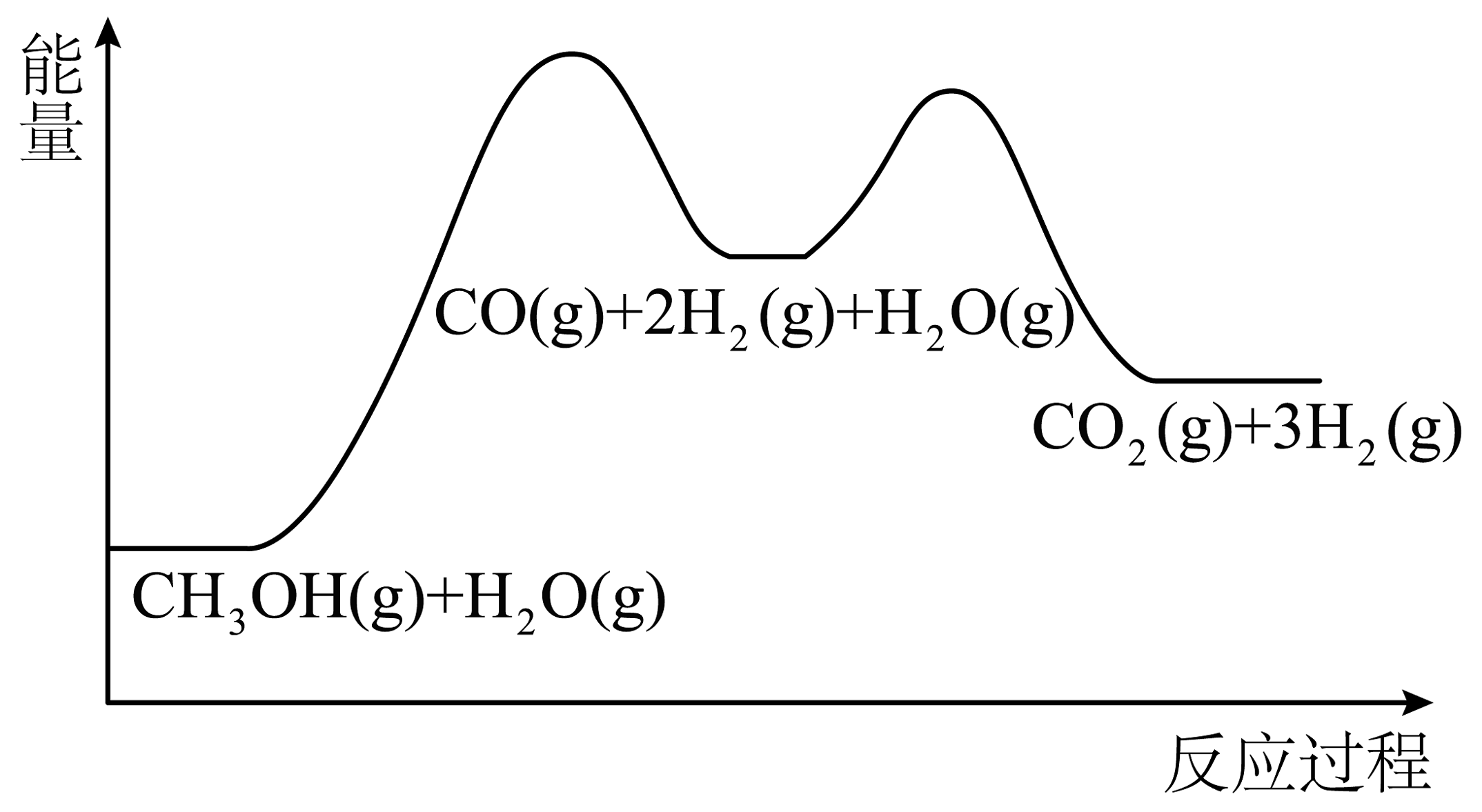 A、总反应的热化学方程式为: B、和的总键能大于和的总键能 C、甲醇与水蒸气催化重整的总反应速率取决于反应① D、使用催化剂,能提高单位体积内活化分子的百分数
A、总反应的热化学方程式为: B、和的总键能大于和的总键能 C、甲醇与水蒸气催化重整的总反应速率取决于反应① D、使用催化剂,能提高单位体积内活化分子的百分数 -
10、NA为阿伏加德罗常数的值,下列说法正确的是A、苯和苯乙烯的混合物中含有的碳氢键数一定为6NA B、过量铜与含的浓硝酸反应,则反应中电子转移数为0.2NA C、将完全溶于水中,所得溶液中的粒子数之和为0.1NA D、 , 则每生成时转移电子0.4NA
-
11、下列化学反应与方程式不相符的是A、黑火药爆炸: B、向红色溶液中加入过量铁粉至溶液浅绿色: C、黄铁矿的燃烧: D、以水杨酸为原料生产阿司匹林(乙酰水杨酸):

-
12、结构决定性质,性质决定用途。下列事实解释错误的是
选项
物质的性质
解释
A
沸点:乙醇>乙烷
乙醇分子间形成氢键而乙烷不能
B
N2可用作反应的保护气
N2中N≡N键能大
C
用浸泡过酸性高锰酸钾溶液的硅藻土吸收乙烯,保鲜水果
C2H4分子中含碳碳双键,易发生加成反应
D
稀有气体的化学性质稳定
原子的最外层电子达到稳定结构
A、A B、B C、C D、D -
13、在密闭容器中,反应 分别在三种不同实验条件下进行,它们的起始浓度均为;②、③与①比较只有一个实验条件不同。反应物的浓度随时间的变化如图所示。下列说法不正确的是
 A、与实验①相比,实验②可能使用了催化剂 B、实验③进行后,用表示的平均反应速率 C、实验②平衡时的转化率为 D、该反应的
A、与实验①相比,实验②可能使用了催化剂 B、实验③进行后,用表示的平均反应速率 C、实验②平衡时的转化率为 D、该反应的 -
14、二氧化硫在食品工业中可用作漂白剂、防腐剂、抗氧化剂等。某研究小组利用如图所示装置制备并检验SO2的部分性质。下列说法正确的是
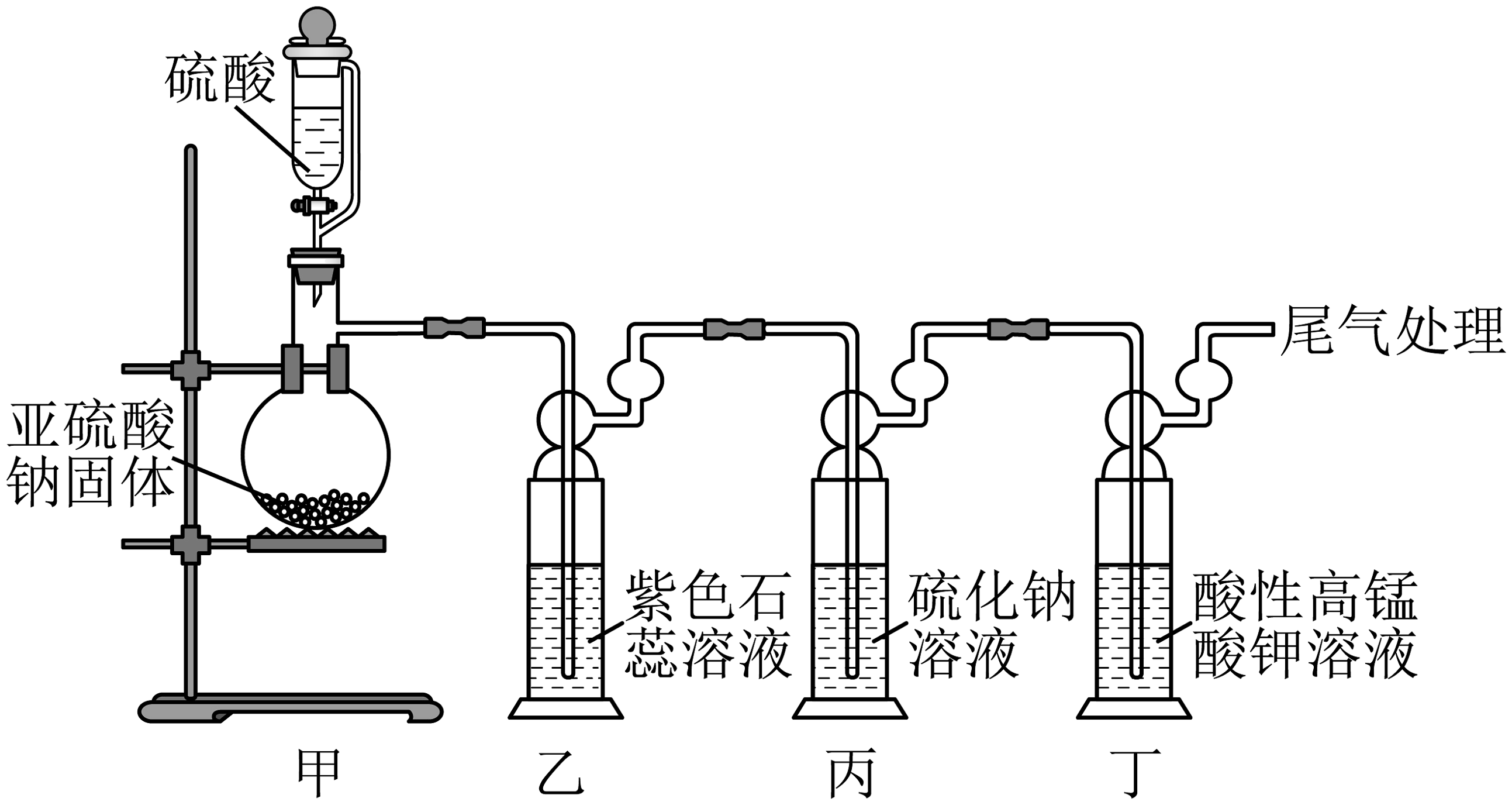 A、装置甲中常用的稀硫酸溶液 B、装置乙中溶液颜色变化:先变红后褪色 C、装置丙中发生的最终总反应为: D、装置丁中酸性溶液褪色的原理与用于食品漂白剂的原理相同
A、装置甲中常用的稀硫酸溶液 B、装置乙中溶液颜色变化:先变红后褪色 C、装置丙中发生的最终总反应为: D、装置丁中酸性溶液褪色的原理与用于食品漂白剂的原理相同 -
15、对反应(I为中间产物),相同条件下:①加入催化剂,反应达到平衡所需时间大幅缩短;②提高反应温度,增大,减小
。基于以上事实,可能的反应历程示意图(——为无催化剂,------为有催化剂)为
A、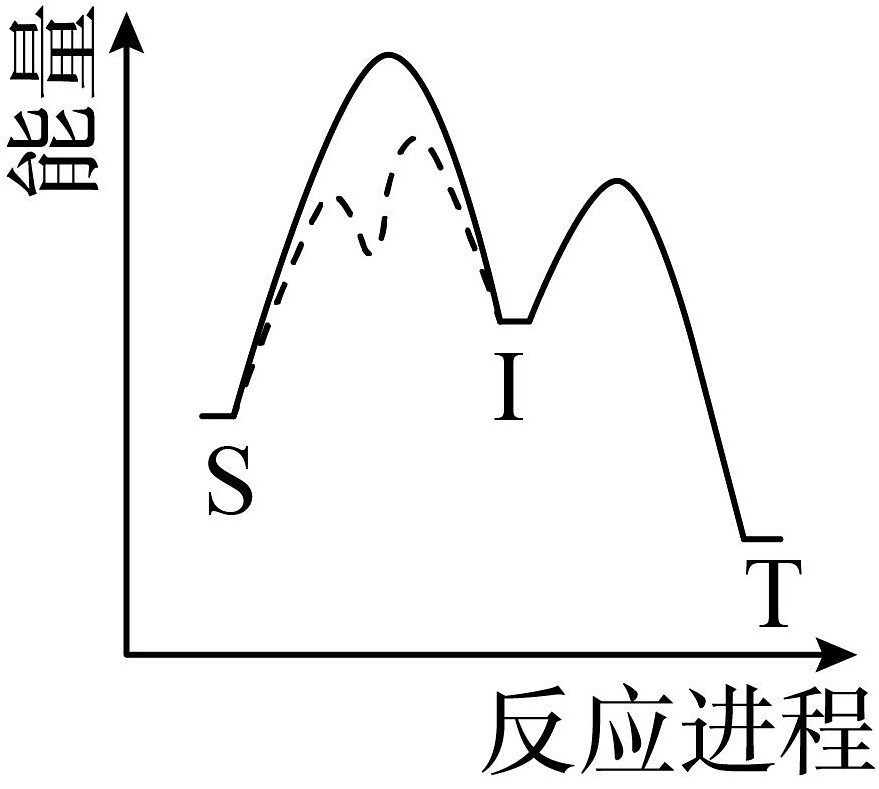 B、
B、 C、
C、 D、
D、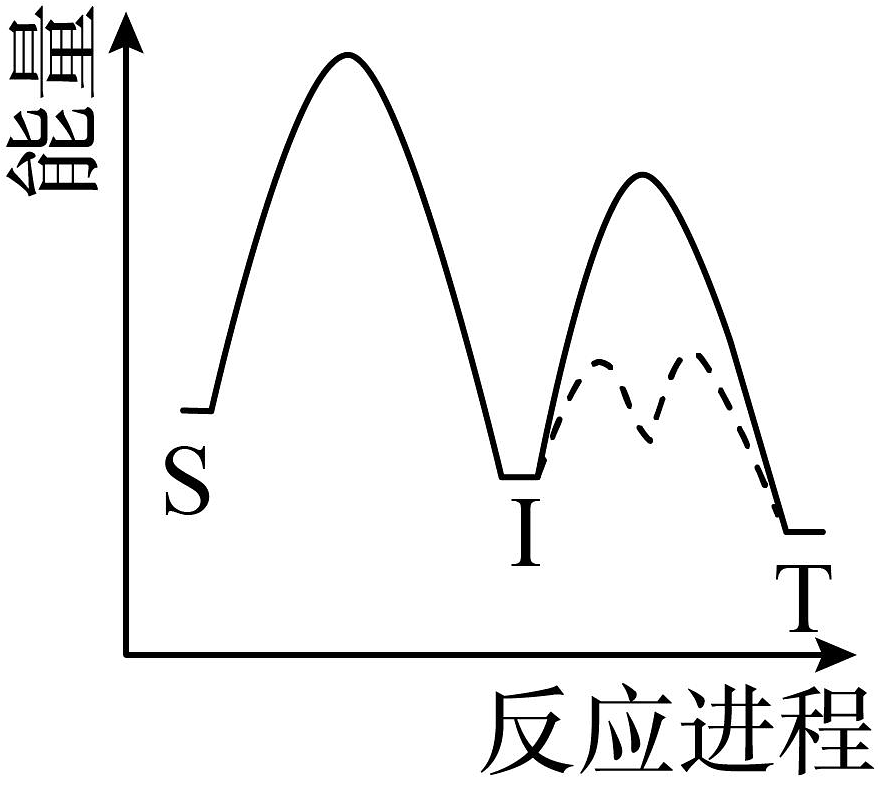
-
16、在溶液中不能大量共存的离子组是A、 B、 C、 D、
-
17、下列实验装置正确且能达到相应实验目的的是
 A、装置用于实验室制备 B、装置可验证非金属性 C、装置可制取氢氧化铁胶体 D、装置可用于测定中和反应的反应热
A、装置用于实验室制备 B、装置可验证非金属性 C、装置可制取氢氧化铁胶体 D、装置可用于测定中和反应的反应热 -
18、下列化学用语表示正确的是A、甲烷的分子结构模型:
 B、离子的结构示意图:
B、离子的结构示意图: C、羟基的电子式:
C、羟基的电子式: D、醛基:-COH
D、醛基:-COH
-
19、下列说法不正确的是A、观察烧杯中钠与水反应的实验现象时,不能近距离俯视 B、混凝剂聚合氯化铝可使污水中的细小悬浮物等聚集成较大的颗粒 C、甲醛水溶液具有杀菌防腐性质,可用于制作生物标本 D、溶液比溶液稳定
-
20、下列材料中属于新型无机非金属材料的是A、光学玻璃 B、储氢合金 C、光导纤维 D、聚氯乙烯塑料