相关试卷
-
1、实验室用如下原理制备:(浓) , 下列说法正确的是A、该反应中氧化产物是 B、该反应中还原剂与氧化剂物质的量之比为1:2 C、该反应中每生成转移电子1mol D、随反应进行硫酸浓度逐渐减低,则可能发生反应
-
2、下列各物质所含原子数由多到少的顺序是
①(标准状况) ②个氦气分子 ③ ④(标准状况)
A、①③②④ B、①②③④ C、③④①② D、④②③① -
3、“价-类”二维图是学习元素及其化合物知识的重要模型。氯元素的“价-类”二维图如图所示。下列说法错误的是
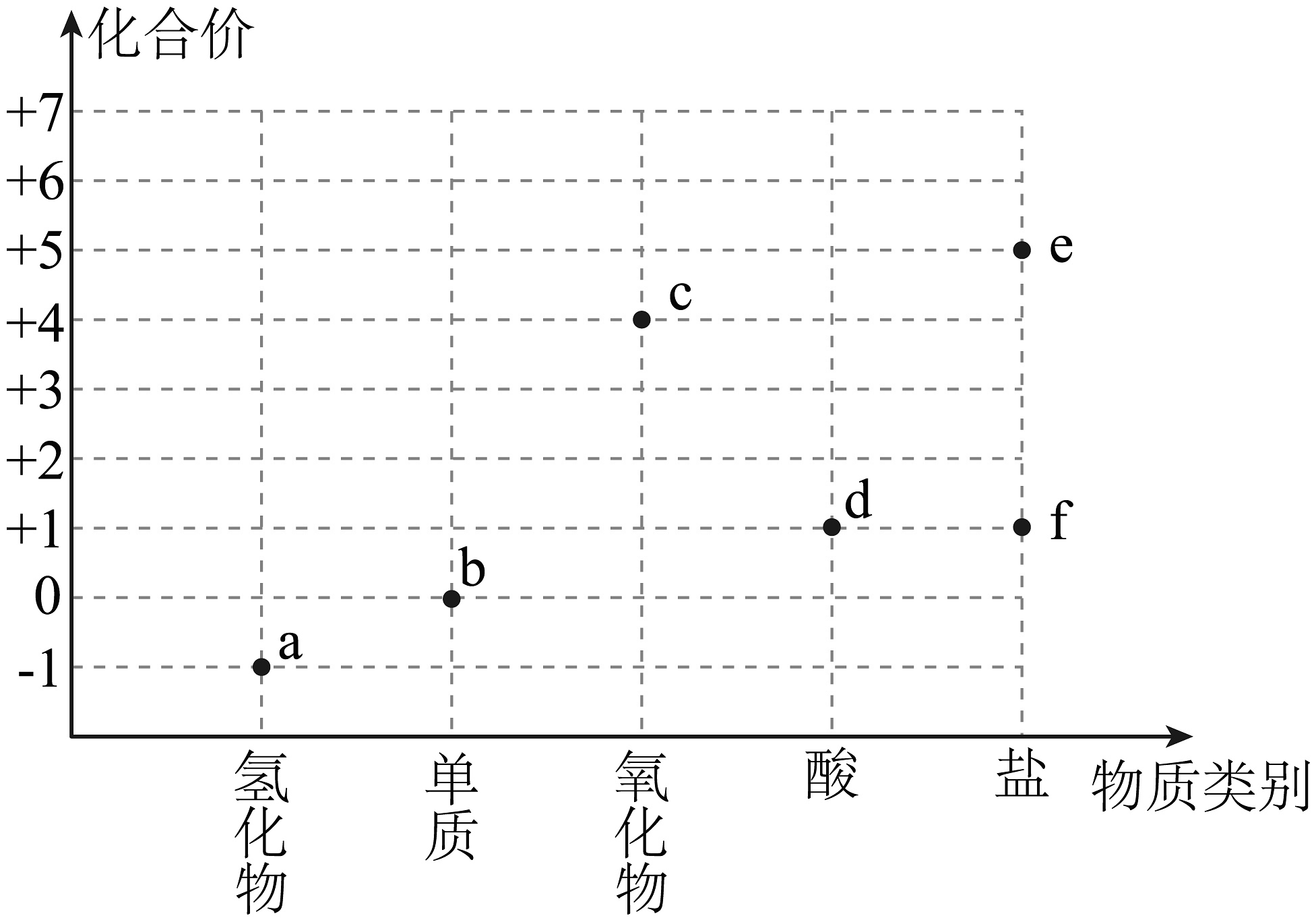 A、从氧化还原反应角度分析:a与d反应制取b B、从类别的角度分析:a与f反应制取b C、d的水溶液性质不稳定,其溶液久置后酸性减弱 D、b、c、d、f都具有强氧化性,可用于杀菌消毒
A、从氧化还原反应角度分析:a与d反应制取b B、从类别的角度分析:a与f反应制取b C、d的水溶液性质不稳定,其溶液久置后酸性减弱 D、b、c、d、f都具有强氧化性,可用于杀菌消毒 -
4、在做“氢气在氯气中燃烧”实验时,不需要标识的图标是A、
 B、
B、 C、
C、 D、
D、
-
5、下列说法正确的是A、中含有分子 B、标准状况下,所占的体积约为44.8L C、中含有的氢原子数目约为 D、硫酸溶液中含有个氧原子,则硫酸的物质的量是0.125mol
-
6、下列两种物质间的反应,不可用离子方程式“”表示的是A、NaOH溶液与溶液 B、澄清石灰水与盐酸 C、溶液与稀硝酸 D、KOH溶液与次氯酸
-
7、下列各组离子在水溶液中一定能大量共存的是A、、、、 B、、、、 C、、、、 D、、、、
-
8、下列关于和的性质说法正确的是
 A、时,碳酸氢钠在水中的溶解度比碳酸钠大 B、分别向和溶液中滴加溶液产生白色沉淀 C、分别向和固体中加入少量水,温度变化不同 D、可利用图示装置来比较和的热稳定性
A、时,碳酸氢钠在水中的溶解度比碳酸钠大 B、分别向和溶液中滴加溶液产生白色沉淀 C、分别向和固体中加入少量水,温度变化不同 D、可利用图示装置来比较和的热稳定性 -
9、下列关于金属钠的叙述不正确的是A、金属钠保存在石蜡油或煤油中 B、钠未用完应放回原试剂瓶 C、钠具有强还原性,能置换出溶液的Cu D、当火灾现场存放有大量金属钠时,需用干燥的沙土来灭火
-
10、下列转化中,需要加入氧化剂才能实现的是A、 B、 C、 D、
-
11、下列说法正确的是A、液氯可储存在钢瓶中 B、若泄露,应向下风口地区转移,并用湿毛巾护住口鼻 C、为增加漂白粉的杀菌消毒作用,通常将其置于阴凉处敞口保存 D、纯净的氢气可以在氯气中安静地燃烧,发出棕黄色火焰
-
12、羟基氧化铝是一种“纳米材料”,粒子直径为之间。若将其均匀地分散到蒸馏水中,形成某一分散系,下列描述不正确的是A、能产生丁达尔效应 B、属于液溶胶 C、静置后,会析出沉淀 D、能透过滤纸
-
13、下列物质中,属于电解质的是A、Al B、NaCl C、KOH溶液 D、蔗糖溶液
-
14、下列仪器名称为“坩埚”的是A、
 B、
B、 C、
C、 D、
D、
-
15、下列物质中属于碱性氧化物的是A、 B、 C、 D、
-
16、在给定条件下,下列物质间转化均能实现的是A、 B、 C、 D、
-
17、室温时用稀硝酸可将苯酚直接硝化,转化关系及部分产物产率表示如下。

反应历程:

下列说法不正确的是
A、工业生产中产物Ⅱ由于存在分子内氢键,易先被水蒸气蒸出,容易与产品Ⅰ分离 B、反应生成产物Ⅱ过程中最大能垒为 C、反应足够长的时间,升高温度会提高体系中产物Ⅰ的产率 D、反应体系中加入浓硫酸有利于产生活性中间体 , 可催化反应进行 -
18、化学与生活密切相关。下列说法正确的是A、“84”消毒液具有强氧化性,能用于饮用水杀菌消毒 B、维生素C用作抗氧化剂,说明维生素C具有氧化性 C、放映机到银幕间产生光柱是因为丁达尔效应 D、用盐酸除铁锈,是因为Fe2O3溶于水后,其溶液显碱性
-
19、工业上以铝土矿(主要成分为 , 含少量、FeO、等杂质)为主要原料制备氧化铝,流程如下:
 (1)、酸浸:用稍过量的稀硫酸酸浸后溶液中存在的阳离子有。(2)、用溶液浸取铝土矿中的铝元素和铁元素,溶液的用量不宜过量太多,其原因是。(3)、氧化:溶液的作用是将二价铁转化为三价铁,反应的离子方程式为: 能在酸性环境下将Fe2+氧化为Fe3+的氧化剂有KMnO4、KClO3、Cl2等。已知下列三种氧化剂氧化Fe2+后对应的还原产物如下:
(1)、酸浸:用稍过量的稀硫酸酸浸后溶液中存在的阳离子有。(2)、用溶液浸取铝土矿中的铝元素和铁元素,溶液的用量不宜过量太多,其原因是。(3)、氧化:溶液的作用是将二价铁转化为三价铁,反应的离子方程式为: 能在酸性环境下将Fe2+氧化为Fe3+的氧化剂有KMnO4、KClO3、Cl2等。已知下列三种氧化剂氧化Fe2+后对应的还原产物如下:氧化剂
KMnO4
KClO3
Cl2
还原产物
Mn2+
Cl-
Cl-
判断等物质的量的三种氧化剂分别与足量的酸性FeSO4溶液反应,得到Fe3+最多的是(填化学式)。
(4)、沉淀:用溶液调节pH,将Al元素和Fe元素转化为沉淀析出。溶液中的pH对铝、铁沉淀率的影响如图所示。
①为获得较高的铝、铁沉淀率,应控制溶液pH为 左右。
②检验沉淀完全的操作:为。
(5)、碱溶:用NaOH溶液溶解沉淀,分离出 , 下列措施中能提高单位时间内铝元素浸出率的有: (填序号)。A.适当增大NaOH溶液浓度 B.适当加快搅拌速率 C.适当降低温度
-
20、
已知是一种棕黄色固体,可用于医药,在有机化学中常用作催化剂。某研究性学习小组对进行了如下实验:
I.配制溶液
(1)完成该实验所需要的玻璃仪器除了烧杯、玻璃棒、量筒外,还需要________。
(2)若在配制过程中出现下列情况,会使所配制溶液的浓度偏低的是 _______ (填标号)。
A. 定容时俯视刻度线 B. 转移溶液后,未洗涤烧杯和玻璃棒就直接定容 C. 没有冷却到室温就立即开始转移溶液 D. 定容摇匀后,发现液面低于刻度线,再加入蒸馏水至刻度线 (3)某实验小组人员用98%的浓硫酸配制250 mL 1.0 mol/L的稀硫酸,在如图所列配制过程中,错误的是 ________ (填选项字母)。

II.某小组利用下图装置制备和 , 并探究其氧化还原性质。已知氯气与碱液在温度高时反应生成 , 低温时生成。

(4)实验开始后,装置a中反应的化学方程式是________;装置b试管内的溶液中,逐渐增多的阴离子是________ (填离子符号)。
(5)各取少量和溶液,分别置于1号和2号试管中,均滴入足量溶液,振荡后滴加足量稀盐酸,再滴入少量溶液,观察到1号试管中无沉淀,2号试管中有白色沉淀。
①请用离子方程式依次表示2号试管中生成沉淀的有关反应:________。
②该条件下的氧化能力:________。(填“>”“<”或“=”)
③d装置的作用是:________。