相关试卷
-
1、某制药厂的废钯催化剂含、、、、和活性炭,提取贵金属的流程如下:

已知:①铂系元素(包括Pt、Pd等六种元素)的单质均为惰性金属;
②性质较稳定,难溶于酸、碱,可溶于王水;
③、。
回答下列问题:
(1)、“焙烧”步骤的主要目的是除去活性炭,通常控制温度600℃、焙烧时间约 , 焙烧温度过高或时间过长均导致钯浸出率降低,原因是。(2)、“浸渣”的成分是少量及。(3)、“浸出”步骤中生成配合物 , 写出该反应的化学方程式。(4)、“氨化”步骤中转化为 , 反应后溶液 , 此时溶液中。(5)、“沉钯”步骤中的离子方程式为。(6)、存在两种平面结构,将其记为A和B。查得25℃时A、B在水中的溶解度分别为0.2577g、0.0366g,A具有广谱的抗癌活性,写出A的结构式(中共价键不必画出)。 -
2、菠萝“扎嘴”的原因之一是菠萝中含有一种难溶于水的草酸钙针晶。常温下,草酸钙在不同下体系中与关系如图所示(代表),已知。下列有关说法正确的是( )
 A、数量级为 B、溶液时, C、时,曲线①呈上升趋势的原因是部分转化为 D、点时,体系中
A、数量级为 B、溶液时, C、时,曲线①呈上升趋势的原因是部分转化为 D、点时,体系中 -
3、为了保护环境、充分利用铅资源,科学家设计了如下的-铅化合物燃料电池实现铅单质的回收。

下列有关说法错误的是( )
A、正极区溶液pH升高,负极区溶液pH降低 B、电子流向:电极b→负载→电极a C、阴极区电极反应式为 D、为了提高的回收率,离子交换膜为阴离子交换膜 -
4、一种硼镁化合物具有超导性能,晶体结构属于六方晶系,其晶体结构、晶胞沿c轴的投影图如下所示(晶胞边长为apm,晶胞高为cpm,为阿伏加德罗常数的值)。

下列说法正确的是( )
A、该物质的化学式为 B、硼原子间最近距离为 C、的配位数为12 D、该物质的摩尔体积为 -
5、(可表示为)催化剂的催化原理如下图所示(为烃基)。
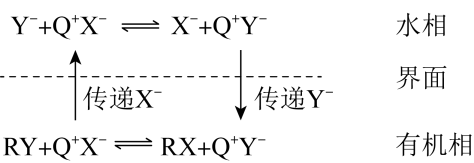
下列说法错误的是( )
A、总反应为: B、易溶于水相而难溶于有机相 C、与、之间的离子键强度要适中 D、PTC催化剂可用作相转移倠化剂 -
6、下列实验方法或操作能达到实验目的的是( )
实验目的
实验方法或操作
A.
在水溶液中存在
向的溶液中加入浓溶液,振荡试管,观察颜色变化
B.
检验中的碳碳双键
取样,加入适量酸性高锰酸钾溶液后观察是否褪色
C.
比较与
常温,测浓度均为的和溶液的
D.
比较Mg和Al的金属性强弱
向浓度均为和溶液中滴加浓氨水至过量
A、A B、B C、C D、D -
7、纳米催化制备甲酸钠的机理如下图所示:

下列说法错误的是( )
A、纳米尺寸有利于加快反应速率 B、反应过程中有极性键的断裂与形成 C、反应过程中不需要持续补充 D、总反应的原子利用率为100% -
8、下列方程式书写错误的是( )A、漂白粉在空气中生效: B、水解制取 C、线型酚醛树脂的制备:
 D、硅橡胶单体的制备:
D、硅橡胶单体的制备:
-
9、推理是一种重要的思维方法。下列推理合理的是( )
已知
推论
A
电负性:F>O>H
键角:OF2>H2O
B
键能:H-Cl>H-Br
酸性:HCl>HBr
C
溶解性:MgSO4>CaSO4
溶解性:SrSO4>BaSO4
D
极性:NH3>PH3
极性:NCl3>PCl3
A、A B、B C、C D、D -
10、是宇宙中最丰富的元素,位于第四周期且基态原子中有5个未成对电子,基态原子的能级与能级的电子数相等,是的等电子体,四种元素形成的配合物结构如下图所示,下列说法错误的是( )
 A、第一电离能: B、电负性: C、配体ZW中配位原子为Z D、Y的最高价氧化物为碱性氧化物
A、第一电离能: B、电负性: C、配体ZW中配位原子为Z D、Y的最高价氧化物为碱性氧化物 -
11、CaCN2可以作为固态氮肥,并改善土壤酸性,通过反应制备。下列说法错误的是( )A、该反应为熵增过程 B、该反应实现了氮的固定 C、该反应需在无水条件下进行 D、的电子式为

-
12、溴是一种重要的基础化工原料,下列有关溴的实验装置及原理正确的是( )


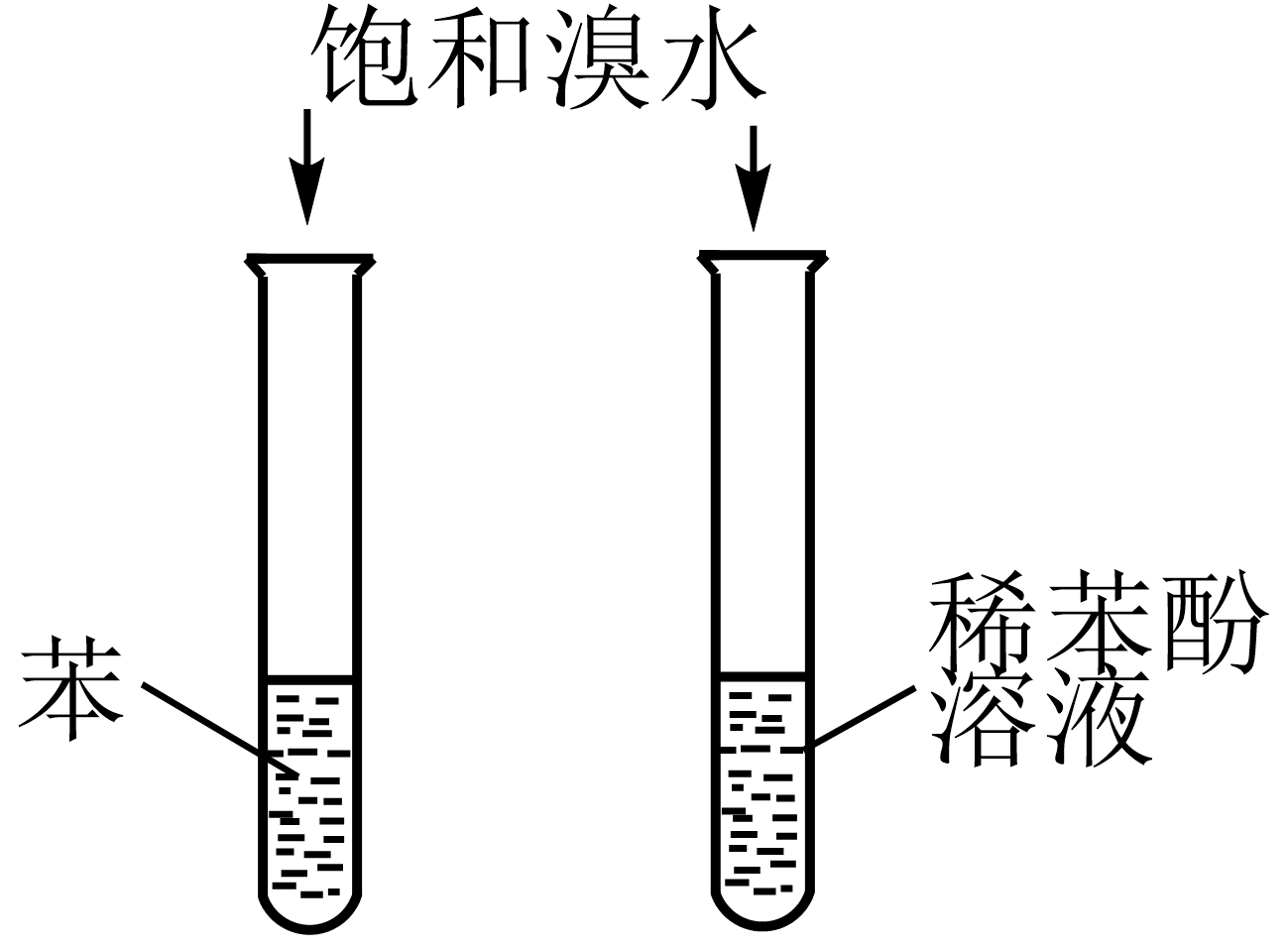

A.实验室保存液溴
B.验证二氧化硫的漂白性
C.验证苯环对羟基的活化作用
D.验证醛基的还原性
A、A B、B C、C D、D -
13、蕲艾是十大楚药之一,所含精油有很好的抗虫作用,其有效成分之一的结构简式如下图所示。下列说法错误的是( )
 A、存在顺反异构现象 B、有特征红外吸收峰 C、最多有21个原子共平面 D、该物质能消耗
A、存在顺反异构现象 B、有特征红外吸收峰 C、最多有21个原子共平面 D、该物质能消耗 -
14、生活中处处有化学,下列说法错误的是( )A、医药、农药、食品添加剂属于精细化学品 B、自然界存在的多糖甲壳质是不可再生资源 C、压电陶瓷能实现机械能与电能的相互转化 D、高分子分离膜已广泛应用于饮用水的制取
-
15、下列化学用语表示正确的是( )A、键的电子云形状:
 B、固体HF中的链状结构:
B、固体HF中的链状结构: C、二聚中的杂化方式:
D、石墨的层状结构:
C、二聚中的杂化方式:
D、石墨的层状结构:
-
16、湖北盐业历史悠久,早在唐代已有零星的产盐记载。下列说法错误的是( )A、既可做调味品也可做防腐剂 B、焰色试验可用于区分和 C、电解食盐水的产物可用于生产漂粉精 D、医疗上生理盐水是含0.9%的溶液
-
17、氙及其化合物在工业生产中有重要用途。(1)、1962年,化学家巴特利特合成了氙的第一个化合物 , 其在熔化时电离出和。Xe和混合制得的反应可以表示如下:

已知:①在标准状态下将1mol离子型晶体(如NaCl)拆散为1mol气态阳离子()和1mol气态阴离子()所需要的能量叫做晶格能,的晶格能为。
②Xe的第一电离能为。
③ 。
根据以上信息,计算反应 。
(2)、不久,在三个不同实验室里又分别合成了、、三种简单化合物。其中一种化合物的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为90°,表示阿伏加德罗常数的值。则该化合物的化学式为 , 中心原子的价层电子对数为 , 晶体密度为。 (3)、一定条件下,向恒容密闭容器中充入Xe和混合气体,反应体系中存在的平衡及相应部分数据如下表所示。
(3)、一定条件下,向恒容密闭容器中充入Xe和混合气体,反应体系中存在的平衡及相应部分数据如下表所示。已知:分压=总压×该组分物质的量分数;
对于反应
其中 , 、、、为各组分的平衡分压。
标准压强平衡常数
反应平衡
反应I:
360
反应II:
反应III:
①0(填“>”或“<”)。为提高平衡混合物中的含量,应投料比(填“增大”或“减小”)。
②673K时充人23.77molXe和 , 达平衡时容器内总压强 , 各产物的物质的量如下表所示:
化学式
物质的量/mol
3.60
19.80
0.36
则平衡转化率(保留三位有效数字),。
-
18、颠茄酮是合成麻醉剂阿托品的重要原料。20世纪初,化学家维尔施泰特通过十余步反应合成颠茄酮,但总产率仅有0.75%,部分合成步骤如下:

十几年后,化学家罗宾逊改进了合成思路,仅用3步反应便完成合成,总产率达90%。主要合成步骤如下:
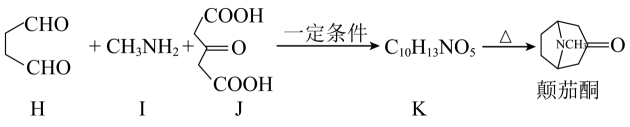
已知:

回答下列问题:
(1)、I的名称为;J的官能团名称为。(2)、C→D、G→颠茄酮的反应类型分别为、。(3)、B→C转化的第①步反应中,B的碳碳键断裂(填“σ”或“π”)。第②步反应方程式为。(4)、颠茄酮的分子式为。K的结构简式为。(5)、写出一种同时满足以下条件的颠茄酮的同分异构体的结构简式。①属于酰胺类物质
②核磁共振氢谱有三组峰,且峰面积之比为9:2:2
③能使溴的四氯化碳溶液褪色
-
19、我国科研人员合成出了尺寸可调、品质高的CdE(E=S,Se,Te)量子点,并发展成为如今镉基量子点合成的通用方法。(1)、基态S原子的价电子排布式为。CdSe量子点直径尺寸在8~12nm,所以CdSe量子点常被称为(填分散系名称)量子点。(2)、在一定条件下可由和Se反应生成 , 再由与反应制得CdSe颗粒,制备流程和生成的实验装置如图所示:

①仪器a的名称是。
②与配位剂L形成配合物的化学方程式为。
③研究表明,CdSe的生成分两步,其中第二步是与反应生成CdSe,则在碱性条件下发生的第一步反应的离子方程式为。
④某化学小组通过实验探究了60℃下,其他条件相同时,反应时间、配位剂浓度分别对纳米颗粒平均粒径的影响,结果如图1、图2所示。

根据以上实验结果预测,若要在60℃下得到平均粒径3.0nm的颗粒,最适宜的方法是。
(3)、配位剂L是一种组成人体内蛋白质的氨基酸,其质谱图如图所示,分子中含硫质量分数为26.45%且巯基(-SH)与β-碳原子直接相连,则配位剂L的结构简式为。实验室中,还可以用(填现代仪器分析法名称)获得其化学键或官能团的信息。
-
20、镍基合金是一种适宜于制造涡轮喷气发动机叶片的重要材料。某工厂用红土镍矿(主要成分为NiO,还含有FeO、、、MgO等)制取金属镍和高效催化剂黄铵铁矾 , 工艺流程如下:

已知:①在本工艺条件下,、不能氧化。
②常温下, , 。
(1)、提高红土镍矿“酸浸”浸取率的措施是(任写一种)。(2)、滤渣的主要成分为 , 其重要用途为(任写一种)。(3)、“氧化”时反应的离子方程式为。“沉铁”时反应的离子方程式为。(4)、“沉镁”前加入MgO将溶液pH调节至5.5~6.0的原因是。若调节pH后的溶液中 , 则至少需要加入molNaF 固体“沉镁”,使1L“沉镁”后的溶液中(忽略体积的变化)。(5)、工业上可用如图所示的装置电解溶液制备Ni和较浓的硫酸,则该电解池的阳极反应式为。