相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、对下列事实的解释,错误的是A、湿衣服在夏天比冬天易晾干——温度越高,分子运动越快 B、液化石油气被压缩储存于钢瓶中——分子间间隔变小 C、水结成冰——分子停止运动 D、金刚石硬,石墨软——碳原子的排列方式不同
-
2、热爱劳动从我做起。对下列家务劳动中所涉及的化学知识叙述错误的是
选项
家务劳动
化学知识
A
用厨余垃圾自制花肥
物质发生缓慢氧化
B
油锅着火,用锅盖盖灭
隔绝氧气(或空气)灭火
C
清理家中鱼缸并通入空气
氧气易溶于水
D
使用煤炉时,用扇子往炉中扇风
空气流通,提供充足的氧气
A、A B、B C、C D、D -
3、学习化学的一个重要途径是科学探究,实验是科学探究的重要手段。下列化学实验操作错误的是A、滴加液体
 B、量取液体
B、量取液体 C、检查气密性
C、检查气密性 D、倾倒液体
D、倾倒液体
-
4、在科学实验中,科研人员在20℃、1个标准大气压和其他一定的条件下,给水施加一个弱电场,水就可以结成冰,称为“热冰”。下列说法正确的是A、“热冰”是一种混合物 B、“热冰”在任何条件下都不会融化 C、“热冰”与水的化学性质相同 D、结成“热冰”后,水分子停止运动
-
5、过氧化钙(CaO2)作为供氧剂,能增加水中溶解氧,改善水质,常用于鱼池急救、越冬等。过氧化钙中氧元素的化合价为A、+4 B、0 C、-1 D、-2
-
6、维生素C(C6H8O6)能促进人体生长发育,增强人体对疾病的抵抗力,主要存在于蔬菜和水果中。下列关于维生素C的说法中,错误的是A、维生素C由碳、氢、氧三种元素组成 B、维生素C由6个碳原子、8个氢原子、6个氧原子构成 C、维生素C中C、H、O三种元素的质量比为9:1:12 D、维生素C中碳元素的质量分数约为40.9%
-
7、汕尾盛产的紫菜是一种硒含量丰富的食品。硒在元素周期表中的部分信息如图所示,下列说法正确的是
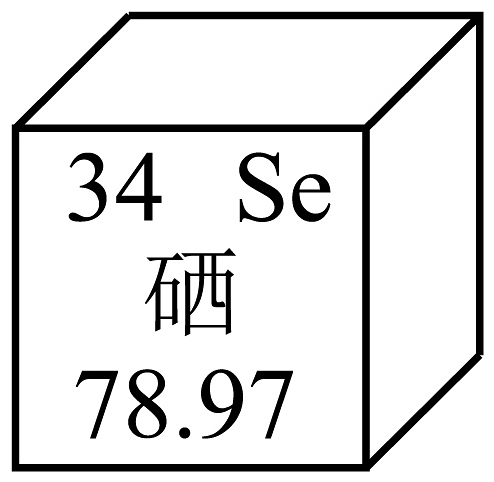 A、硒元素的相对原子质量为78.97g B、硒原子的质子数为34 C、硒原子的中子数为34 D、硒属于金属元素
A、硒元素的相对原子质量为78.97g B、硒原子的质子数为34 C、硒原子的中子数为34 D、硒属于金属元素 -
8、中国“天宫”空间站中的梦天舱燃烧科学柜采用a作燃料成功实施首次在轨点火实验。a完全燃烧的反应微观示意图如图所示。下列说法错误的是
 A、反应前后元素种类不变 B、参与反应的a和b分子的个数比为1:1 C、a分子中C、H原子的个数比为1:4 D、反应生成c、d的质量比为11:9
A、反应前后元素种类不变 B、参与反应的a和b分子的个数比为1:1 C、a分子中C、H原子的个数比为1:4 D、反应生成c、d的质量比为11:9 -
9、实验安全提示是确保实验室操作安全的重要措施。下列实验安全提示图标中不正确的是A、
 护目镜
B、
护目镜
B、 洗手
C、
洗手
C、 用电
D、
用电
D、 锐器
锐器
-
10、用图1所示装置制取氢气,将100.0g稀硫酸全部加入锥形瓶中,天平示数的变化如图2所示,请计算:
 (1)、共制取氢气g。(2)、参加反应的锌的质量。(写出计算过程)
(1)、共制取氢气g。(2)、参加反应的锌的质量。(写出计算过程) -
11、
学习了MnO2对过氧化氢有催化作用的知识后。小鑫同学想:氧化铜(CuO)能否起到类似MnO2的催化作用呢?于是进行了如下探究。
【作出猜想】猜想Ⅰ.CuO不是催化剂,也不参与反应,反应前后质量和化学性质不变;
猜想Ⅱ.CuO参与反应产生O2 , 反应前后质量和化学性质发生了改变;
猜想Ⅲ.CuO是反应的催化剂,反应前后质量和化学性质。
【进行实验】用天平称量0.2gCuO取5mL5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
步骤③现象
步骤⑥结果
步骤⑦现象
结论
带火星的木条复燃
猜想溶液中有气泡冒出,
猜想Ⅰ、Ⅱ不成立,猜想Ⅲ成立
(2)步骤(填序号)的对比能证明CuO能加快过氧化氢溶液分解的速率。
(3)步骤⑦的目的是。
(4)过氧化氢能被CuO催化分解生成氧气的符号表达式为。
【拓展】
(5)过氧化氢溶液完全分解后得到的液体是(填“纯净物”或“混合物”)。
-
12、我们学过的六种可以制得氧气的途径,如图1所示。
 (1)、若A是无色液体,生成氧气需要加入MnO2 , 则反应⑥的化学方程式为。(2)、若B为人体中含量最多的物质,则转化③属于基本反应类型中的反应;转化⑤的原理是利用液氮和液氧的(填“熔点”或“沸点”)不同。(3)、转化④靠的是植物的。(4)、空间站中常用水气整合系统实现CO2的清除和O2的再生流程,如图2所示。
(1)、若A是无色液体,生成氧气需要加入MnO2 , 则反应⑥的化学方程式为。(2)、若B为人体中含量最多的物质,则转化③属于基本反应类型中的反应;转化⑤的原理是利用液氮和液氧的(填“熔点”或“沸点”)不同。(3)、转化④靠的是植物的。(4)、空间站中常用水气整合系统实现CO2的清除和O2的再生流程,如图2所示。
i.分析流程可知,可循环利用的化合物为(填化学式),航天员呼吸属于氧化过程,并热量。
ii.理论上,电解分解等质量的下列氧化物,产生氧气最多的是(填字母序号)。
A.Al2O3 B.FeO C.CaO D.H2O
-
13、验证可燃物燃烧的条件。已知:白磷、红磷的着火点分别是40℃、260℃。
I.将80℃的热水从长颈漏斗注入集气瓶,但不浸没燃烧匙,此时白磷燃烧,红磷不燃烧。
II.继续加水,浸没两支燃烧匙,白磷火焰熄灭。
III.从注射器将空气推入瓶内,热水回流至长颈漏斗,白磷露出水面,再次燃烧。
 (1)、白磷燃烧的化学方程式为。(2)、对比步骤II、III,白磷熄灭再次复燃,说明可燃物燃烧需要的条件是。(3)、实验中红磷不燃烧的原因是。(4)、推入空气后瓶内热水回流至长颈漏斗的原因是。
(1)、白磷燃烧的化学方程式为。(2)、对比步骤II、III,白磷熄灭再次复燃,说明可燃物燃烧需要的条件是。(3)、实验中红磷不燃烧的原因是。(4)、推入空气后瓶内热水回流至长颈漏斗的原因是。 -
14、阅读下列科普短文,回答问题。
碳捕捉与封存技术。“碳捕捉与封存”是我国的一项先进技术(如图所示)。我国能源消耗的70%来自煤炭。每秒有100吨煤在燃烧,年消耗量超过30亿吨。

如果任由煤炭资源在诸多领域利用,将对大气、河流、土地产生污染,温室效应增强。为实现节能减排、绿色环保的目标,我国政府举全国之力,积极倡导并大力发展新的绿色经济。比如:电厂中的煤在极高的温度下充分燃烧,会产生大量的CO2 , 每年的排放量大约1600万吨,运用“碳捕捉与封存”技术,这些CO2将不会进入大气。被封存的CO2有许多用途,如用于食品保鲜、气体肥料、冷藏食物、物品灭火等,以此来消除资源的巨大浪费。我国正以超世界一流的目光发展经济,完善环保体制。
(1)、二氧化碳由(填微粒的名称)构成。(2)、“碳捕捉与封存”技术有利于控制的增强。(3)、煤(主要成分是碳)在空气中充分燃烧,主要发生反应的化学方程式为。(4)、将分离聚集的CO2压入地下的过程中,分子间间隔会。(5)、将CO2封入蓄水层中发生反应的化学方程式为。(6)、“碳捕捉与封存”技术的先进之处是。 -
15、航天员在太空生活需要氧气和水。氧气和水的相互转化,体现了“合”与“分”的思想。(1)、“合”的思想
液氢和液氧反应产生的能量可为返回舱返回提供动力,该反应的微观示意图如下:

①该化学反应的基本类型是反应。
②返回舱返回的动力采用液氢作为能源的优点是(写一条即可)。
(2)、“分”的思想航天员在空间站生活所需氧气主要通过电解水获得,该反应的化学方程式是
(3)、“合”与“分”的思想通过以上事实,证明了水是由组成。
-
16、化学用语是学习化学的重要工具。请用适当的化学符号填空。(1)、保持氩气化学性质的最小粒子:。(2)、地壳中含量最多的金属元素和含量最多的非金属元素组成的物质:。(3)、标出氧化铁中铁元素的化合价:。(4)、两个钙离子:。(5)、高铁酸钾由K+和FeO构成,则高铁酸钾的化学式为。(6)、硫酸铝:。(7)、乙醇:。
-
17、将CO和铁的氧化物FexOy置于密闭容器中,一定条件下充分反应至完全。反应过程中容器内部分物质的质量变化如图所示。下列说法正确的是
 A、m的值为12.6 B、铁的氧化物中x:y=3:4 C、参加反应的铁的氧化物的质量为16g D、当CO2质量为4.4g时,容器内CO质量为14g
A、m的值为12.6 B、铁的氧化物中x:y=3:4 C、参加反应的铁的氧化物的质量为16g D、当CO2质量为4.4g时,容器内CO质量为14g -
18、推理是学习化学常用的思维方法。下列有关说法正确的是A、金属阳离子带正电荷,则带正电荷的微观粒子都是金属阳离子 B、H2O和H2O2的组成元素相同,则它们的化学性质相同 C、氧化物中都含有氧元素,则含有氧元素的化合物一定是氧化物 D、元素的种类由质子数决定,则质子数相同的原子一定属于同种元素
-
19、在一密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生反应,测得反应前及t1、t2时各物质质量的变化如图所示,下列说法正确的是
 A、丙是该反应的催化剂 B、该反应属于分解反应 C、参加反应的甲、乙的质量比是2:1 D、生成丁的质量为7g
A、丙是该反应的催化剂 B、该反应属于分解反应 C、参加反应的甲、乙的质量比是2:1 D、生成丁的质量为7g -
20、在2A+B=3C+2D的反应中,适量的A和16g的B恰好完全反应生成18gC和50gD,若B的相对分子质量为32,则A的相对分子质量为A、52 B、54 C、104 D、208