相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、下列化学用语的意义描述正确的是A、2N2:2个氮原子 B、Ba2+:1个钡离子带2个单位正电荷 C、2H:2个氢元素 D、Na+:钠元素的化合价为+1
-
2、变瘪的气球充入氦气,气球鼓胀起来。从分子角度描述球内发生的变化正确的是A、氦气分子的体积变大 B、氦气分子间的间隔变大 C、氦气分子个数增多 D、氦气分子分裂生成了新的分子
-
3、诺贝尔化学奖获得者List曾用有机催化剂脯氨酸(C5H9NO2)研究催化反应,其结构模型如图,有关脯氨酸的说法正确的是
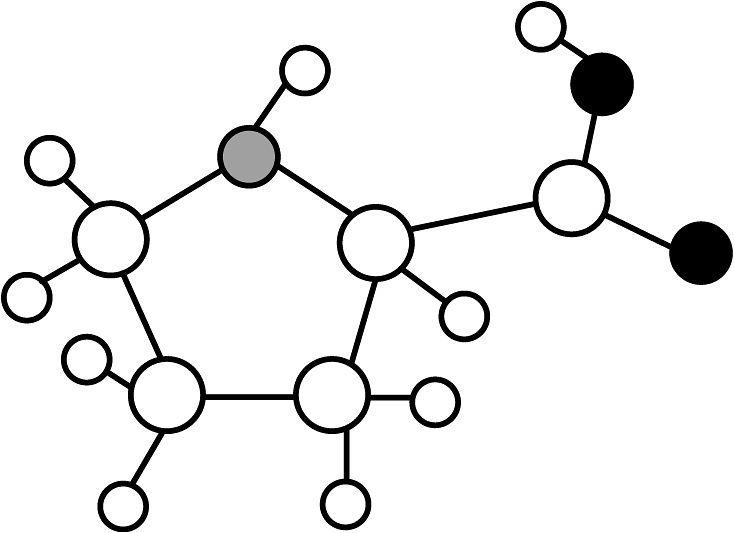 A、脯氨酸由17个原子构成 B、脯氨酸结构中含有NO2分子 C、氢元素的质量分数最小 D、催化剂反应后其化学性质发生改变
A、脯氨酸由17个原子构成 B、脯氨酸结构中含有NO2分子 C、氢元素的质量分数最小 D、催化剂反应后其化学性质发生改变 -
4、空气和水是一切生命体生存所必需的物质。下列关于空气和水的说法,正确的是A、空气中氮气的质量分数约为78% B、氧气可以用于卫星发射的助燃剂 C、为节约用水,直接用工业废水灌溉农田 D、电解水实验中,正极与负极产生气体的质量比约为1:2
-
5、高锰酸钾( KMnO4)常用于实验室制取氧气。高锰酸钾属于A、化合物 B、氧化物 C、单质 D、混合物
-
6、能造成酸雨的气体是A、二氧化碳 B、一氧化碳 C、氮气 D、二氧化硫
-
7、中华文明源远流长,以下我国古代发明或技术应用的原理中发生化学变化的是A、木器涂漆 B、烧制陶瓷 C、炭黑制墨 D、竹编花篮
-
8、测定硫酸钠溶液的溶质质量分数
实验室有一瓶标签被腐蚀的Na2SO4溶液。某化学兴趣小组的同学为测定该Na2SO4溶液的溶质质量分数,取10gNa2SO4溶液于烧杯中,然后加入BaCl2溶液。生成沉淀的质量与加入BaCl2溶液的质量关系如图所示,试计算该Na2SO4溶液的溶质质量分数。

-
9、
探究镁条变黑的条件
镁条在空气中久置表面会变黑,对镁条变黑的条件及黑色物质成分作如下探究。
【查阅资料】①氮化镁(Mg3N2)是黄色固体。②常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
(1)同学们认为镁条变黑与N2无关,其理由是。
【实验】先将镁条用砂纸打磨光亮,用如图所示装置(镁条长度均为3cm,试管容积均为20mL。)分别进行下列实验。(B、C、D中通入CO2体积均为4mL。)

(2)试管C中,Na2SO3溶液的作用是(用化学方程式表示)。
(3)对照实验指除了自变量以外,其它的量都保持不变的实验。该实验方案中采用了对照实验的方法。请指出其中的对照实验(填ABCD实验代号)和自变量。
第①组对照实验 , 自变量。
第②组对照实验 , 自变量。
第③组对照实验 , 自变量。
(4)实验现象:试管A、B、C中的镁条始终无明显变化,试管D中镁条第3天开始变黑,至第20天全部变黑。以实验现象为证据推理可以获得的结论是。镁条变黑后的生成物中一定含有元素。
(5)小林同学猜想镁条表面的黑色物质中含有碳酸盐,检验的方法是:取变黑后的镁条于试管内,。
-
10、物质的制备(1)、氢氧化锂(LiOH)在航天器中可用于吸收CO2。工业上用电解法制得的LiOH溶液中含有NaOH。在N2保护下将混合溶液蒸发结晶,可得到LiOH晶体。有关物质的溶解度如表:
电解法制得的1000g溶液中,LiOH的质量分数为10%、NaOH的质量分数为5%。
物质
溶解度/g
20℃
30℃
40℃
50℃
60℃
LiOH
12.8
12.9
13.0
13.3
13.8
NaOH
109
118
129
146
177
①该溶液中LiOH的质量为g。
②将该溶液蒸发溶剂并降低温度到20℃时,当剩余溶液中水的质量为100g时,有gLiOH析出。氢氧化钠能不能析出?理由是。
③结晶过程中,若没有N2保护,LiOH晶体中会混有Li2CO3。其原因是(用化学方程式表示)。
(2)、《天工开物》记载了锡的冶炼方法:入砂(指锡砂)数百斤,架木炭亦数百斤,鼓鞲(指鼓入空气)熔化,用铅少许,(锡)沛然流注。①高温下木炭还原锡砂(SnO2)的化学方程式为。
②炼锡时加入少许铅形成合金,产物更易熔化流出,原因是。
(3)、《周礼•考工记》中记载,古人利用贝壳和草木灰为原料制备物质洗涤丝帛。某兴趣小组的同学仿照古法,在老师的指导下按以下流程来制备去污液。
①上述流程中发生分解反应的化学方程式为。
②请你根据流程推测,该去污液中所含溶质的组成有哪几种可能?(用化学式表示)。
-
11、物质的组成结构与性质(1)、溴化氢(HBr)是一种易溶于水的气体,其溶液呈无色,被叫作氢溴酸。
①氢溴酸是由(填微观粒子符号)构成的,小林同学分析其构成后,认为它与盐酸有相似的性质。为探究其性质,进行如图实验:

②由上述实验可知,氢溴酸与盐酸有相似的性质,试分析④中产生红色喷泉的原因。
(2)、科学写作列举稀盐酸和稀硫酸的共性和差异性(各举一条即可),并分析该共性或差异性与其构成的关系,以此说明“物质的性质与其构成有关”。要求:语言简洁,逻辑性强,字数在150字以内。。
-
12、金属蚀刻(1)、精细化工中常对金属进行雕琢,化学蚀刻是常用的方法之一。其原理是通过溶液与金属的化学反应,从而形成凹凸。某车间以含盐酸的溶液为蚀刻液,生产金属雕花外墙装饰板的工艺流程如图所示。请分析流程,回答下列问题。

①胶膜应具有的性质是(写一种)。
②蚀刻步骤中发生反应的化学方程式为。
③喷漆可防止工艺品锈蚀,其防锈原理是。
(2)、化学兴趣小组的同学根据制作金属雕花外墙装饰板的工艺流程,制作一幅金属蚀刻画,两个小组的同学分别以铝板和银板为板材,涂胶后滴加蚀刻液进行蚀刻。
①为保证蚀刻成功,在蚀刻前需对铝板进行打磨,理由是。
②两组同学中不能成功得到蚀刻画的是 , 原因是。
能成功的小组中应用的蚀刻原理是(用化学方程式表示)。其基本反应类型为。
(3)、某加工厂进行金属蚀刻后得到的废液中含有Cu(NO3)2、Zn(NO3)2和AgNO3 , 取一定量废液,进行如图所示操作,并记录相关现象。
①滤液A中的金属阳离子有(写离子符号)。
②滤渣B中的金属有(写化学式)。
-
13、物质的性质与应用(1)、小林在学习氢氧化钙的性质与用途时进行了如图整理,并用化学用语表征相应用途中的反应原理或反应实质,请帮助他补充完整。① , ② , ③ , ④ , ⑤ , ⑥。
 (2)、某兴趣小组在完成了用石灰石和稀盐酸制取二氧化碳的实验后,欲运用数字化实验对反应后所得废液的组成进行定量探究,取一定量的废液,用图1装置进行实验:将80mL一定质量分数的碳酸钠溶液逐滴加入废液中,测得数据如图2。(CaCl2溶液呈中性)
(2)、某兴趣小组在完成了用石灰石和稀盐酸制取二氧化碳的实验后,欲运用数字化实验对反应后所得废液的组成进行定量探究,取一定量的废液,用图1装置进行实验:将80mL一定质量分数的碳酸钠溶液逐滴加入废液中,测得数据如图2。(CaCl2溶液呈中性)
①制取二氧化碳时发生反应的化学方程式为。
②分析图2数据可知废液中溶质的成分为(写化学式)。b点发生反应的化学方程式为。利用实验数据进行定量计算即可确定废液中溶质的含量。
③小林同学提出,不用数字化实验也可以定性检验废液中溶质的成分,请写出实验步骤、可能的现象及相关推理。
-
14、用下图所示浓硫酸配制100g质量分数为9.8%的稀硫酸,下列说法正确的是
 A、经过计算所需浓硫酸的体积为9.8mL,水为90.2mL B、实验所需的主要仪器有烧杯、温度计、托盘天平、量筒 C、稀释时把水倒入盛有浓硫酸的烧杯中,并不断搅拌 D、若少量浓硫酸沾到皮肤上,应立即用大量的水冲
A、经过计算所需浓硫酸的体积为9.8mL,水为90.2mL B、实验所需的主要仪器有烧杯、温度计、托盘天平、量筒 C、稀释时把水倒入盛有浓硫酸的烧杯中,并不断搅拌 D、若少量浓硫酸沾到皮肤上,应立即用大量的水冲 -
15、如表为某自热米饭的营养成分表,下列说法错误的是
营养成分
蛋白质
油脂
糖类
钠
钙
每份含量
29.6g
23.5g
104.7g
814mg
130mg
A、从均衡膳食的角度考虑,搭配苹果一起食用营养会更均衡 B、表中的“钠”“钙”都是人体必需的常量元素 C、该自热米饭配料表中共涉及到3种营养素 D、蛋白质、淀粉、油脂在人体内通过化学反应为生命活动提供物质和能量 -
16、下列物质的性质和用途对应关系不正确的是A、碳酸氢钠受热易分解,可用作治疗胃酸过多 B、铜具有良好的导电性,可用作导线 C、镁燃烧能发出耀眼白光,可用作照明弹 D、一氧化碳具有还原性,可用于冶炼金属
-
17、检查如图所示装置的气密性,其中漏气的装置是A、
 B、
B、 C、
C、 D、
D、
-
18、 某兴趣小组在实验室制取二氧化碳后,将装置内剩余废液进行过滤,然后对滤液中溶质的质量分数进行测定,实验如下:
取50g滤液,向其中逐滴加入溶质质量分数为10%的Na2CO3溶液,反应过程中加入Na2CO3溶液的质量与生成沉淀或气体的质量关系如图所示:

根据实验过程和图像提供的信息,请回答:
(1)、图中曲线a:表示的是随着Na2CO3溶液的滴加,生成(填“沉淀”或“气体”)质量的变化情况;(2)、M点对应溶液中的溶质为(写化学式);(3)、通过计算:x的数值为 , 滤液中HCl的质量分数为。 -
19、 水杨酸是一种天然的消炎药,可以祛除角质、杀菌消炎,非常适合治疗毛孔堵塞引起的青春痘,也可作为化妆品防腐剂原料。水杨酸的分子式为C7H6O3 , 结构简式如图。请回答:
 (1)、水杨酸的相对分子质量为;(2)、水杨酸中C、H、O三种元素的质量比为。
(1)、水杨酸的相对分子质量为;(2)、水杨酸中C、H、O三种元素的质量比为。 -
20、 “双吸剂”的成分为铁粉、生石灰,是一种常用的袋装食品保鲜剂。小明同学在破损的食品包装袋中发现一包久置的“双吸剂”,于是对该固体成分进行了探究:
【提出问题】
久置后固体的成分是什么?
【初步观察】
打开“双吸剂”包装,发现固体粉末黑白相间,还有少量红棕色。
作出猜想】
久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3中的几种。
【实验探究】
取少量固体样品研磨,置于烧杯中,用磁铁吸引,黑色粉末能被吸引,说明有铁粉存在,然后将黑色粉末完全吸引取走。用残留的固体继续进行了如图实验:

【实验分析】
(1)、温度计示数变大,说明该固体样品中一定含有;(2)、向滤液中滴加酚酞试液后溶液变 , 说明该固体样品中一定含有Ca(OH)2;(3)、向滤渣中滴加足量稀盐酸有气泡生成,最后溶液变成黄色,说明该固体样品中一定含有CaCO3和;(4)、【实验反思】学认真思考后,认为【实验分析】(2)中得到固体样品中含有Ca(OH)2的结论不合理,理由是。