-
1、下列实验现象的描述正确的是A、铁丝在氧气中燃烧生成四氧化三铁 B、红磷在空气中燃烧放出白雾 C、硫在氧气中燃烧产生蓝紫色火焰 D、木炭在氧气中燃烧发出红光
-
2、2024年一篇报道“月壤制氧,中国试验出第一口氧气”,震惊世界。下列说法正确的是A、鱼类能在水中生活,证明氧气易溶于水 B、氧气可作火箭发动机的燃烧剂 C、氧气可作焊接金属的保护气 D、可通过加压降温将氧气变成液氧储存在蓝色钢瓶中
-
3、2025春晚歌曲《山鹰和兰花花》传达了对自然环境的关注,下列有关空气的描述正确的是A、酸雨是因为大量排放二氧化硫、二氧化碳气体引起的 B、空气质量指数越大,空气质量状况越好 C、温室效应是大量排放二氧化碳引起的,因此二氧化碳是空气污染物 D、氮气化学性质稳定可作保护气
-
4、下列实验操作正确的是


A.倾倒液体
B.加固体粉末


C.点燃酒精灯
D.量取一定体积的水
A、A B、B C、C D、D -
5、下列有关化学史的说法不正确的是A、汤姆孙发现电子 B、卢瑟福提出原子的核式结构模型 C、拉瓦锡研究空气的组成 D、道尔顿编制元素周期表
-
6、保持氨气()的化学性质的最小粒子是A、氨分子 B、氢原子 C、氮原子 D、氢原子和氮原子
-
7、分子、原子、离子都是构成物质的基本粒子,下列物质由原子构成的是A、水 B、二氧化碳 C、铁 D、硫酸铜
-
8、李清照在《醉花阴》中写了“东篱把酒黄昏后,有暗香盈袖。”词人能闻到菊花清香的原因是A、分子之间有间隔 B、分子很小 C、分子在不断运动 D、分子不可分
-
9、我国科学家屠呦呦因发现青蒿素(化学式C15H22O5),荣获2015年诺贝尔生理学或医学奖,请计算:
(1)青蒿素中氢、氧元素的质量比为 。
(2)28.2g青蒿素中含碳元素的质量为 g。
-
10、下图所示为实验室中常见的气体制备和收集装置。

请回答下列问题:
(1)、写出①的仪器名称:;(2)、实验室用高锰酸钾制取氧气,应选用发生装置(填字母序号),反应的符号表达式为。若用装置D收集氧气,验满的方法是。(3)、实验室用过氧化氢溶液和二氧化锰制取氧气,若选用C作发生装置,你认为选用C的优点是。(4)、已知一氧化氮气体难溶于水,在空气中易与氧气发生反应,则收集一氧化氮气体时应选用图中装置(填字母序号)。 -
11、请回答下列问题。(1)、结合所学知识回答问题:X、Y、Z是中学化学常见的物质,且三种物质均含有同一种元素。X、Y的组成元素完全相同;Z为气体单质,能供给呼吸,也能使带火星的木条复燃。它们之间有如下图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。

①Z的化学式为;
②X转化为Y的化学表达式为;该反应基本反应类型是。
③从微观角度解释X、Y组成元素完全相同,但性质不同的原因。
(2)、①若用过氧化氢溶液制取氧气,发生装置应选用以下装置;若用装置戊收集氧气,气体应从口(“a”或“b”)进入。
②若用甲和丙装置制取并收集氧气,实验结束时的操作。
-
12、根据下列图示实验,回答有关问题:

(1)实验①中夹持铁丝的仪器名称是 , ①中的实验现象;
(2)实验②中试管b中产生的气体是 , 由该实验得出的结论是(写一条);
(3)三个实验中都用到水,水的作用各不相同,我能一一说出。①集气瓶中的水:;②水槽中的水:;③烧杯中的水:。
-
13、今年3月22-28日是第28届“中国水周”,其主题为“节约水资源,保障水安全。”
(1)下列关于水的说法中,不正确的有:(填序号)。
①水是由氢元素和氧元素组成的化合物
②清澈、透明的泉水是纯净物
③合理施用农药、化肥,以减少水体污染
④将活性炭放入硬水中可使其软化
⑤洗菜、洗衣后的水用来浇花、冲洗厕所
(2)自然界中的水一般要净化后才能使用。吸附、过滤、蒸馏等三种净化水的操作中,单一操作相对净化程度最高的是。
(3)下图表示自来水消毒过程中发生的一个反应的微观过程:

①写出上述物质中单质的化学式;
②物质D中氯元素的化合价为。
-
14、如图为六种原子的结构示意图。

请回答下列问题:
(1)图中六种元素之间的最本质区别是;
(2)镁原子在化学反应中容易失去2个电子形成镁离子,镁离子的化学式为;氧化钠由钠离子和氧离子构成,氧化钠的化学式为。
(3)从原子结构上分析,图中哪两组元素具有相似的化学性质(填元素符号)、。
(4)在上述碘的原子结构示意图中,x=。
-
15、用化学符号表示:(1)、空气中含量最高的物质;;(2)、两个铝原子;(3)、由60个碳原子构成的单质分子;(4)、氯化亚铁;(5)、标出五氧化二磷中磷元素的化合价;(6)、画出钠离子的结构示意图。
-
16、某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法错误的是( )
 A、该反应中共有三种元素 B、该反应是化合反应 C、该反应的本质是原子的重新组合 D、该反应前后分子的种类发生改变
A、该反应中共有三种元素 B、该反应是化合反应 C、该反应的本质是原子的重新组合 D、该反应前后分子的种类发生改变 -
17、月球原位资源利用将成为原位补给水和氧气等关键生存物资的核心技术。(1)、Ⅰ.矿石处理
月壤样品分析结果表明其成分较复杂,其中的钛铁矿是铁和钛的氧化物(主要成分可写成具有磁性,其余为非磁性矿物。据此科研人员用干式磁选法(如图11所示)分选富集出钛铁矿。
⑴图11中钛铁矿颗粒将进入斗。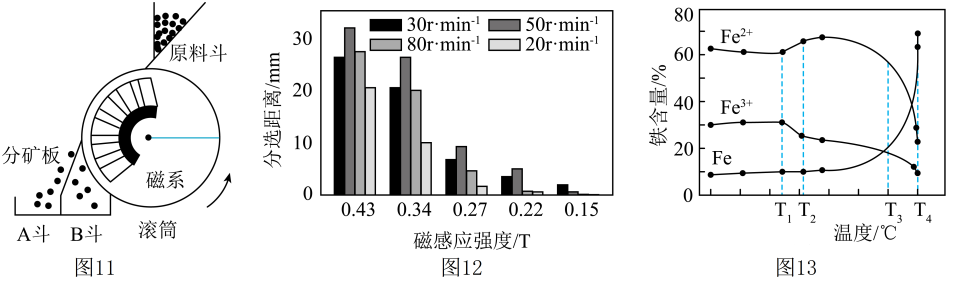
⑵科研人员对粒径为100μm的矿物在不同磁感应强度(单位:T)和转速(单位:条件下进行磁选实验,结果如图12所示,则该装置将月壤中磁性颗粒和非磁性颗粒分选开来的最佳条件为。(2)、Ⅱ.原位制水⑴水是保障人类生存的关键资源。科研人员还在月壤钛铁矿中发现储存有大量氢。在高温下钛铁矿中的氢与铁的氧化物能发生反应,其中氢与氧化亚铁反应生成单质铁和水,该反应方程式为.
⑵图13呈现了钛铁矿随着温度变化过程中所有价态的铁含量变化情况,由图可知最适合大量制水的反应温度为(选填“T2”、“T3”或“T4”)。同学甲发现 温度之间Fe2+的含量不降反升,他依据该温度范围Fe¹+的含量减少得出结论:该温度范围内 Fe3+转化成为了 Fe2+:同学乙认为该推理不严谨,还需参考同温度范围内.
⑶研究嫦娥五号采集的月壤,发现该样品可产水量约占月壤质量的7.5%。已知成人每天饮水量约为1500mL,据此可知每吨月壤可产生的水约能供位成人一天的饮水需求。(3)、Ⅲ.综合开发同学甲查阅资料获知月壤钛铁矿中还存在矿物ULM-1(含他提出一种利用太阳能原位开发月球资源的方案,流程如下:
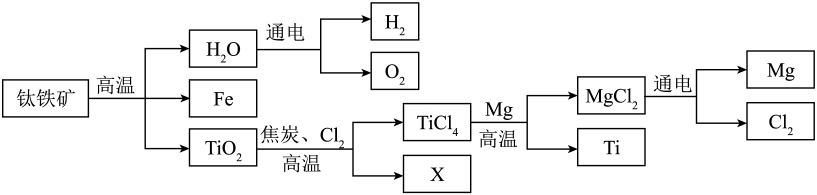
⑴上述流程中的X是一种含两种元素的可燃性气体,其化学式为。
⑵上述流程中可以循环利用的物质有。
⑶同学乙认为该方案暂时不可行,原因是还需要在月球上寻找到元素。 -
18、兴趣小组利用数字化实验探究建筑发生火灾时的逃生策略。
实验步骤:
①以直径25cm,高40cm的圆柱形耐高温密闭容器模拟一幢四层建筑,在密闭容器中放置高为10cm,20cm,30cm的蜡烛,分别模拟不同楼层同时着火的场景。在蜡烛火焰对应高度分别安装温度、传感器。
②启动数据采集,在50s 时同时点燃蜡烛,迅速盖紧圆柱形容器封盖。观察到蜡烛火焰由高到低依次熄灭,记录时间为:106秒、164秒、199秒。待采集数据稳定后停止实验,部分数据如下表:
时间/s
O2含量/%
CO2浓度
低
中
高
低
中
高
106
19.8
19.1
18.5
1940.2
2214.9
3056.5
164
18.9
17.7
17.1
1798.5
2002.3
2755.3
199
18.6
17.1
16.5
1771.9
1913.7
2666.7
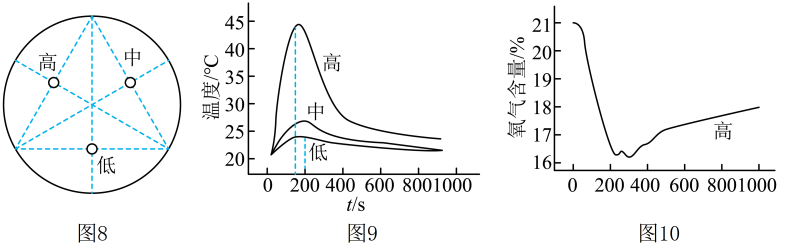 (1)、三支蜡烛的俯视位置如图8所示,目的是为了减小蜡烛间的相互影响,保证三支蜡烛到圆柱形容器壁的距离.(2)、蜡烛的成分之一为C23H48 , 其完全燃烧的化学反应方程式为.(3)、蜡烛由高到低熄灭,则高处蜡烛最先熄灭的原因是.(4)、结合表格中O2含量的变化,请你谈谈对燃烧条件的新认识:.(5)、实验过程中温度和高处O2含量变化曲线如图9和图10所示。
(1)、三支蜡烛的俯视位置如图8所示,目的是为了减小蜡烛间的相互影响,保证三支蜡烛到圆柱形容器壁的距离.(2)、蜡烛的成分之一为C23H48 , 其完全燃烧的化学反应方程式为.(3)、蜡烛由高到低熄灭,则高处蜡烛最先熄灭的原因是.(4)、结合表格中O2含量的变化,请你谈谈对燃烧条件的新认识:.(5)、实验过程中温度和高处O2含量变化曲线如图9和图10所示。①如图9所示,温度最高点出现时间低处晚于高处的原因可能是.
②如图10所示,高处O2含量下降后又明显升高的可能原因是.
(6)、①火灾时需要“往低处逃生”,其原因可能是低处(填序号).a.温度较低 b. CO2浓度较低 c. O2含量较高
②请再列举一种建筑发生火灾时的自救方法:.
-
19、传统美食松花蛋因胶冻状蛋体表面的松花状结晶而得名。(1)、腌制配料:生石灰、草木灰(含食盐、水等,生石灰的主要成分是.(2)、同学们收集松花状结晶并对其展开研究,经仪器分析发现其为富含的难溶物。
①提出假设:松花状结晶的主要成分为:a.MgCO3;b. ;c.两者都有.
②定性研究:
实验操作
实验现象
结论
取0.60g结晶,向其中滴加过量的稀盐酸。
固体溶解,
假设b成立
③定量测定:
将②实验后的混合液过滤,用蒸馏水洗涤滤渣2~3遍,将洗涤液与滤液合并,再向其中滴加NaOH溶液至产生大量白色沉淀,静置,向上层清液中继续滴加NaOH溶液,若 , 则所加NaOH溶液已足量。过滤,洗涤,低温烘干,得到固体0.58g,则晶体中的质量分数为。若没有将洗涤液合并入滤液,则测定结果(选填“偏大”、“偏小”或“无影响”)。
(3)、为探究松花状结晶形成过程中的来源,用原子吸收分光光度法测定腌制过程中鸭蛋不同部位的含量,结果如图7所示,形成结晶的来自于.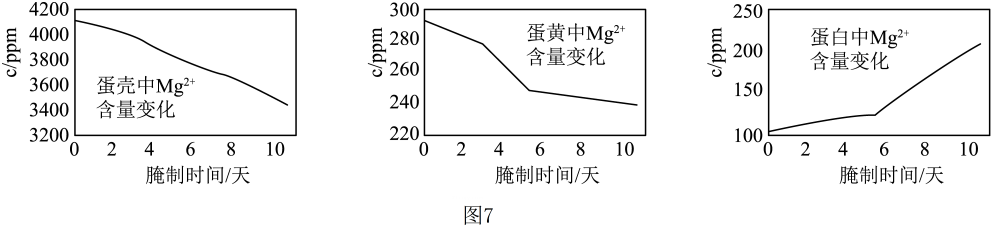 (4)、食用松花蛋时蘸取食醋口感更佳。松花状结晶会与食醋反应生成则该反应的化学方程式为.
(4)、食用松花蛋时蘸取食醋口感更佳。松花状结晶会与食醋反应生成则该反应的化学方程式为. -
20、同学们利用如图装置测定碳酸氢铵样品的纯度(杂质受热不分解)。
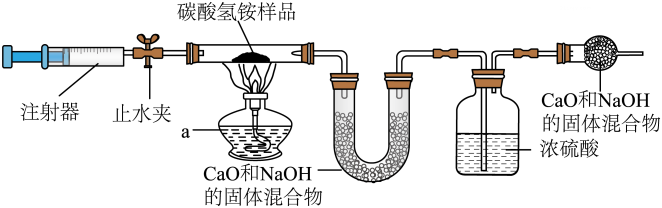 (1)、仪器a的名称: .(2)、气密性检查:在干燥管尾部连接瘪气球,打开止水夹,用注射器注入空气,关闭止水夹,若气球 , 则气密性良好。(3)、碳酸氢铵受热分解的化学反应方程式为.(4)、 U形管装置的作用: .(5)、实验过程中充分加热至固体不再减少后用注射器多次注入空气,其目的是.(6)、实验中取用10g样品进行实验,最后测得洗气瓶吸收氨气的质量为1.7g,求碳酸氢铵样品的纯度。
(1)、仪器a的名称: .(2)、气密性检查:在干燥管尾部连接瘪气球,打开止水夹,用注射器注入空气,关闭止水夹,若气球 , 则气密性良好。(3)、碳酸氢铵受热分解的化学反应方程式为.(4)、 U形管装置的作用: .(5)、实验过程中充分加热至固体不再减少后用注射器多次注入空气,其目的是.(6)、实验中取用10g样品进行实验,最后测得洗气瓶吸收氨气的质量为1.7g,求碳酸氢铵样品的纯度。