-
1、向一定质量的MgCl2、FeCl2和CuCl2混合溶液中加入Zn粉,过滤后,再向滤渣中加入稀硫酸,反应过程中部分生成物的质量与加入锌粉或稀硫酸的质量的关系如图所示。下列说法正确的是( )
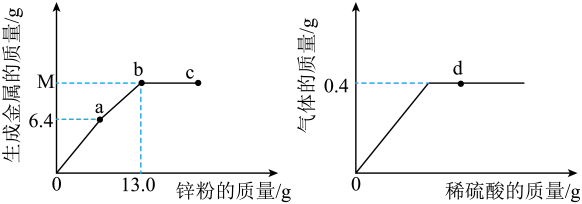 A、从0点到a点,溶液的质量不断增大 B、c点对应的溶液中只含一种溶质 C、与稀硫酸反应的锌粉的质量是5.6g D、b点固体与d点对应溶液中的固体组成不同
A、从0点到a点,溶液的质量不断增大 B、c点对应的溶液中只含一种溶质 C、与稀硫酸反应的锌粉的质量是5.6g D、b点固体与d点对应溶液中的固体组成不同 -
2、兴趣小组用如图所示装置测定木糖醇中碳、氢、氧元素的质量比。取1.52g木糖醇置于装置甲反应管中,充分反应后,测得丙装置增重1.08g,丁装置增重2.20g(实验前已排尽装置内空气,装置乙、丙、丁、戊内试剂均足量)。下列说法错误的是( )
 A、装置乙中氧化钢的作用是确保含碳物质全部转化为二氧化碳 B、实验结束,应先停止通入氧气再熄灭酒精灯 C、若缺少装置戊,将导致测得的木糖醇中氧元素含量偏大 D、木糖醇中碳、氢、氧三种元素的质量比为15:3:20
A、装置乙中氧化钢的作用是确保含碳物质全部转化为二氧化碳 B、实验结束,应先停止通入氧气再熄灭酒精灯 C、若缺少装置戊,将导致测得的木糖醇中氧元素含量偏大 D、木糖醇中碳、氢、氧三种元素的质量比为15:3:20 -
3、下列图像表示的反应过程与实际情况不相符合的是( )
 A、25℃时,向一定量的盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 B、向一定量的氢氧化钙饱和溶液中加入少量氧化钙固体 C、分别向等质量的镁和锌中滴加足量的溶质质量分数相等的稀盐酸 D、一定质量的铜粉在充满氧气的密闭容器中加热
A、25℃时,向一定量的盐酸和氯化钙的混合溶液中逐滴加入纯碱溶液至过量 B、向一定量的氢氧化钙饱和溶液中加入少量氧化钙固体 C、分别向等质量的镁和锌中滴加足量的溶质质量分数相等的稀盐酸 D、一定质量的铜粉在充满氧气的密闭容器中加热 -
4、碳酸锂(Li2CO3)是制造锂离子电池的重要原料。一种由锂辉石精矿(主要成分为LiAlSi2O6 , 还含有少量的MgO、CaO等)制取碳酸锂的工艺流程如下图所示。

【查阅资料】
①锂辉石焙烧时,LiAlSi2O6分解为LiAlO2和SiO2 , SiO2不溶于水也不与稀硫酸反应;
②LiAlO2能与硫酸反应生成Li2SO4和Al2(SO4)3;
③Li2CO3微溶于水,且溶解度随温度升高而减小。
下列说法错误的是( )
A、酸浸槽中溶液含四种金属阳离子 B、除杂池产生的滤渣只有碳酸钙 C、沉锂池中发生的化学反应是Li2SO4+Na2CO3=Li2CO3↓+Na2SO4 D、洗涤应控制在低温下进行 -
5、向密闭玻璃瓶中装入硝酸钾、氯化铵、蒸馏水、樟脑和乙醇溶液,可制成“天气瓶”。硝酸钾和氯化铵的溶解度曲线如图。
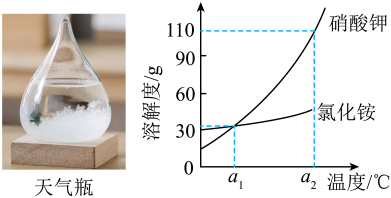
下列说法正确的是( )
A、a1℃时,硝酸钾和氯化铵溶液的溶质质量分数一定相等 B、a2℃时,向50g水中加入60g硝酸钾,充分溶解,可得到110g溶液 C、氯化铵溶液中混有少量的硝酸钾,可用降温结晶的方法提纯 D、a2℃时,等质量的硝酸钾和氯化铵饱和溶液降温至a1℃,析出晶体的质量:硝酸钾>氯化铵 -
6、鉴别、检验、除杂与分离是化学研究的重要方法。下列实验方案能达到实验目的的是( )
选项
实验目的
实验方案
A
鉴别分别盛有空气、氧气和二氧化碳的三瓶气体
各伸入一根燃着的木条,观察现象
B
检验氯化钠溶液中混有的氯化镁
取样,滴加氢氧化钠溶液,观察现象
C
除去NH4Cl溶液中混有的(NH4)2SO4
向溶液中加入过量的BaCl2溶液,过滤
D
分离氧化铜和铁粉
向混合物中加入足量盐酸,过滤
A、A B、B C、C D、D -
7、逻辑推理是学习化学常用的思维方法。下列逻辑推理正确的是( )A、金属能导电,则能导电的物质一定是金属 B、中和反应的产物是盐和水,则产物是盐和水的反应一定是中和反应 C、活泼金属与酸反应生成气体,则能与酸反应生成气体的物质一定是活泼金属 D、同种元素原子的质子数相同,则质子数相同的原子一定属于同种元素
-
8、科学工作者研发了一种SUNCAT系统,借助该系统利用如图所示的原理可持续合成氨。下列说法正确的是( )
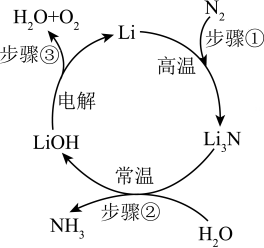 A、步骤①发生化合反应 B、步骤②参加反应的Li3~N和H2O的质量比为1:3 C、总反应的化学方程式是N2+H2O=NH3+O2 D、理论上反应过程中需要不断补充金属Li
A、步骤①发生化合反应 B、步骤②参加反应的Li3~N和H2O的质量比为1:3 C、总反应的化学方程式是N2+H2O=NH3+O2 D、理论上反应过程中需要不断补充金属Li -
9、芳纶纤维常用于国防领域高端装备的制造,间苯二胺(C6H8N2)是制取芳纶纤维的主要原料。下列说法错误的是( )A、1个间苯二胺分子由16个原子构成 B、间苯二胺由6个碳元素、8个氢元素、2个氮元素组成 C、间苯二胺中氢元素质量分数最低 D、可用燃烧法区分芳纶纤维和羊毛纤维
-
10、下列劳动实践中涉及的化学解释错误的是( )
选项
劳动实践
化学解释
A
用熟石灰处理酸性废水
酸与碱发生中和反应
B
炒菜时,油锅着火,用锅盖盖灭
降低可燃物的着火点
C
用活性炭净水
活性炭具有吸附性
D
用食醋除去水壶内的水垢
水垢与酸发生反应而溶解
A、A B、B C、C D、D -
11、钕是一种重要的稀土元素,在元素周期表中的部分信息及原子结构示意图如图所示。下列说法正确的是( )
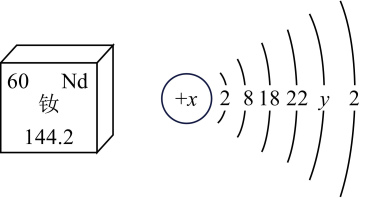 A、钕是非金属元素 B、钕的相对原子质量为144.2g C、y=10 D、钕原子的核电荷数为60
A、钕是非金属元素 B、钕的相对原子质量为144.2g C、y=10 D、钕原子的核电荷数为60 -
12、分类是学习化学的常用方法。下列物质分类正确的是( )A、混合物:液态氧、澄清石灰水 B、化合物:C70、乙醇 C、氧化物:五氧化二磷、干冰 D、盐:苛性钠、硝酸铵
-
13、某同学“测定草木灰的酸碱度及碳酸钾含量”的实验部分操作如下,其中正确的是( )A、
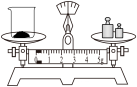 称量草木灰样品
B、
称量草木灰样品
B、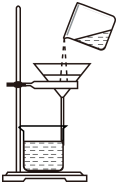 过滤浊液
C、
过滤浊液
C、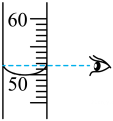 量取一定体积溶液
D、
量取一定体积溶液
D、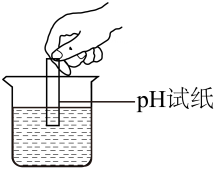 测定溶液pH
测定溶液pH
-
14、坚持绿色发展,促进人与自然和谐共生。下列做法与这一理念不相符合的是( )A、推广清洁能源,落实节能减排 B、大量施用化肥,提高粮食产量 C、垃圾分类回收,减少环境污染 D、积极植树造林,改善空气质量
-
15、实验室存放氢氧化钠的化学试剂柜应张贴的危险化学品标志是( )A、
 爆炸性物质
B、
爆炸性物质
B、 易燃固体
C、
易燃固体
C、 腐蚀性物质
D、
腐蚀性物质
D、 毒性物质
毒性物质
-
16、因青蒿素的研究获得诺贝尔生理学或医学奖的我国科学家是( )A、张青莲 B、屠呦呦 C、闵恩泽 D、徐光宪
-
17、中华民族的发明创造为人类文明进步作出了巨大贡献。我国的下列古代发明及应用不涉及化学变化的是( )A、烧制陶瓷 B、粮食酿酒 C、火法炼锌 D、晒制井盐
-
18、为测定某稀硫酸的溶质质量分数,化学小组取一定量合金于烧杯中,分五次加入等量的稀硫酸,测得相关数据如表:
实验次数
第一次
第二次
第三次
第四次
第五次
加入稀硫酸总质量/g
50
100
150
200
250
产生氢气总质量/g
0.1
m
0.3
0.4
0.4
(1)、表中m的值为。第五次实验后溶液中的溶质为(填化学式)(2)、计算该稀硫酸的溶质质量分数。 -
19、
下图是是配制50g质量分数为15%的氯化钠溶液的操作过程示意图,试回答:

(1)上述操作过程示意图中的错误有处,还缺少一个操作步骤是。B操作中实际称量氯化钠的质量是g。(说明:1g以下用游码)
(2)D操作应选用的量筒(从10mL、50mL、100mL中选择)
(3)若B的操作是正确的。下列的错误操作可能导致溶液溶质质量分数小于15%的是(填序号)
①C操作中有固体洒落 ②D操作中有少量水溅出 ③量取水时,仰视读数
(4)取20g质量分数为15%的氯化钠溶液配制成质量分数为6%的氯化钠溶液,需要加水g。
Ⅱ.某种手机电路板中含金属Fe、Cu、Ni、Ag,如图是某工厂回收部分金属的流程图:

【查阅资料】已知在一定条件下能发生 , 而Au、Ag不能反应。
(5)操作①后得到的滤渣中一定含有的金属是 , 实验室进行此操作时玻璃棒的作用是。
(6)写出滤液③和铁粉发生反应的化学方程式。
(7)Cu、Ag、Ni在溶液中的活动顺序由强到弱的顺序依次是。
-
20、
气体的制取与性质实验是初中化学实验的重要内容。
Ⅰ.气体的制取实验

(1)图1中仪器①的名称为________。
(2)实验室加热高锰酸钾制取氧气的化学方程式为________,选择并组装发生和收集装置,正确的连接顺序为________(填接口处字母)。
(3)装置B、C都可以作为实验室制取二氧化碳和氢气的发生装置,与装置C相比,装置B的优点是________。
Ⅱ.气体的性质实验

(4)木炭燃烧实验(如图2)。加热后的木炭在空气中红热,在氧气中剧烈燃烧,________(填实验现象),放出热量。燃烧现象不同的原因是________。
(5)二氧化碳性质实验(如图3)。当观察到短蜡烛熄灭时,关闭K,片刻后长蜡烛熄灭。从二氧化碳性质的角度分析原因:________。
(6)氢气性质实验(如图4)。用排水法收集到一瓶氢气,倒置于铁架台上,将一根点燃的蜡烛缓慢插入瓶中,瓶口有一团火焰,插入瓶中后蜡烛熄灭了。上述实验及操作能说明的是________(多选,填序号)。
A. 氢气能支持燃烧 B. 氢气具有可燃性 C. 氢气的密度比空气小 D. 氢气难溶于水