-
1、
某小组以“探究催化剂的奥秘”为题展开了项目式学习。将适量淀粉放入过氧化氢溶液中,过氧化氢溶液的分解速率加快。因此,该小组同学进行了如下探究:
【提出问题】淀粉能否作过氧化氢分解的催化剂?
【做出猜想】淀粉能作过氧化氢分解的催化剂。
【实验验证】
(1)完成下列实验探究:
实验步骤
实验现象
结论及解释
I.

A中无明显现象
B产生大量气泡,带火星木条复燃。
B中产生的气体是(填名称)。
Ⅱ.向B试管中重新加入的过氧化氢溶液,反应停止后过滤、洗涤、干燥、称量滤渣。
B中带火星木条又复燃,滤渣质量为
淀粉的和在反应前后均没有发生变化,能作过氧化氢分解的催化剂。
(2)B中过氧化氢反应的文字表达式:。
【实验拓展】同学们又设计了如图所示装置对比淀粉与二氧化锰的催化效果,实验均以生成气体为准,其他可能的影响因素忽略不计,相关数据见表:
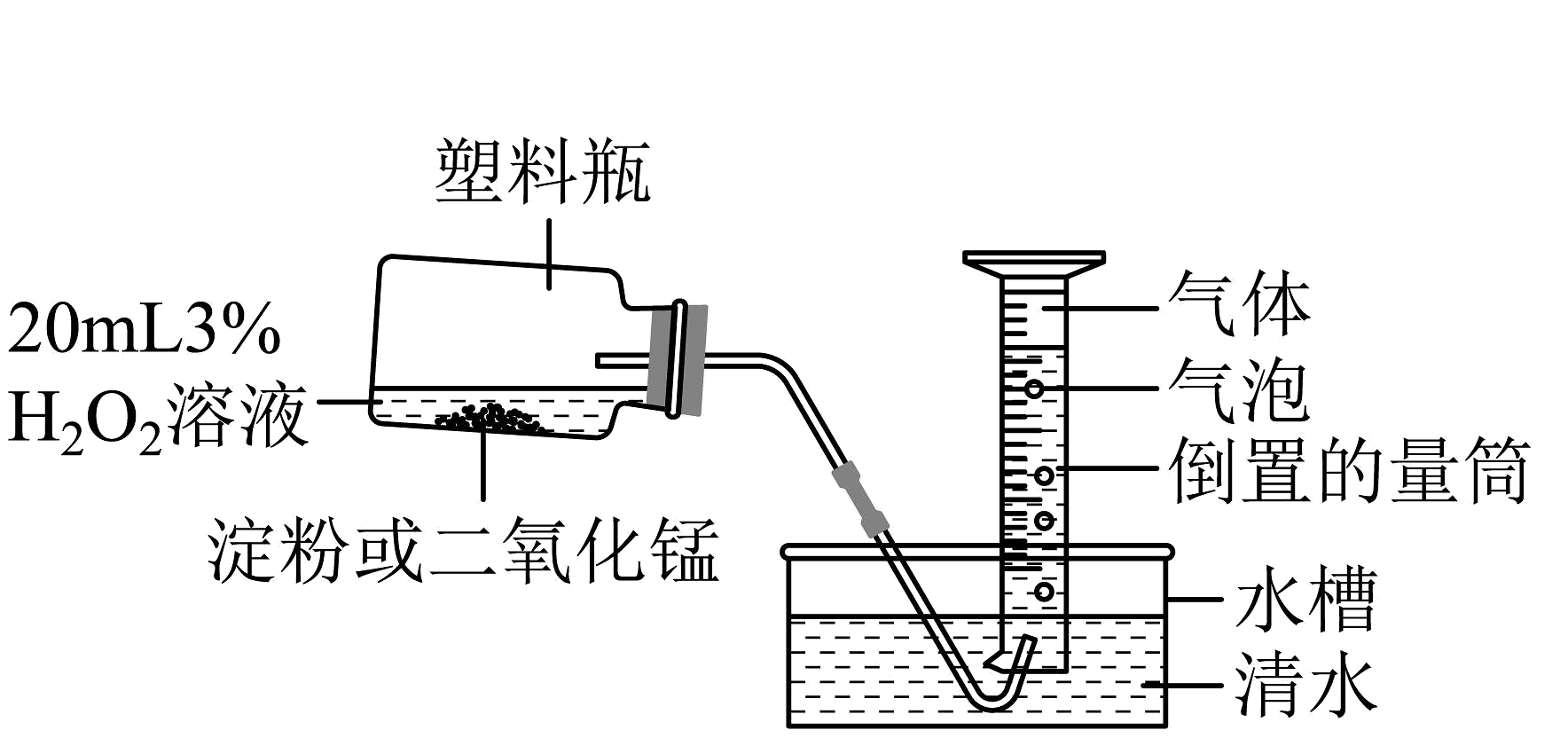
实验编号
过氧化氢溶液的体积
其他物质质量
待测数据
I
淀粉
Ⅱ
二氧化锰
(3)上述实验中“待测数据”是指;若 , 则可得出的结论是。
【拓展探究】
(4)催化剂在化工生产中起着重要作用,(选填“能”或“不能”)提高产物产量。
-
2、如图是实验室制取气体的部分装置。请回答有关问题:
 (1)、写出图中仪器的名称:① , ②。(2)、实验室用高锰酸钾制取氧气的装置有一个明显的错误是。其反应原理是(用文字表达式表示)。(3)、实验室用过氧化氢制取氧气,应选择的发生装置是(填字母序号)。(4)、甲烷气体难溶于水且密度比空气小。可用无水醋酸钠与碱石灰两种固体混合加热制取甲烷。你认为最适合用于实验室制取并收集一瓶较纯净的甲烷气体的装置是(填字母序号)。
(1)、写出图中仪器的名称:① , ②。(2)、实验室用高锰酸钾制取氧气的装置有一个明显的错误是。其反应原理是(用文字表达式表示)。(3)、实验室用过氧化氢制取氧气,应选择的发生装置是(填字母序号)。(4)、甲烷气体难溶于水且密度比空气小。可用无水醋酸钠与碱石灰两种固体混合加热制取甲烷。你认为最适合用于实验室制取并收集一瓶较纯净的甲烷气体的装置是(填字母序号)。 -
3、新型材料纳米级铁粉具有广泛的用途,它比普通铁粉更易与氧气反应,其制备流程如图所示:
 (1)、纳米级铁粉在物质分类中属于(填“纯净物”或“混合物”)。(2)、纳米级铁粉在氧气中能自发燃烧生成黑色固体,发生反应的文字表达式为。(3)、在制备纳米级铁粉的工艺流程中,氮气可以保护铁粉,利用了氮气的。(4)、上述流程中可以回收利用的物质是。(5)、写出氢气和氯化亚铁反应的文字表达式。
(1)、纳米级铁粉在物质分类中属于(填“纯净物”或“混合物”)。(2)、纳米级铁粉在氧气中能自发燃烧生成黑色固体,发生反应的文字表达式为。(3)、在制备纳米级铁粉的工艺流程中,氮气可以保护铁粉,利用了氮气的。(4)、上述流程中可以回收利用的物质是。(5)、写出氢气和氯化亚铁反应的文字表达式。 -
4、阅读下列短文:
氦气是一种无色无味、不易燃、不易爆的气体。充满氦气的气球能飘在空中,是因为氦气是除了氢气以外密度最小的气体。在标准大气压下,液氦的沸点是 , 与人类所说的绝对零度()只有一点点距离,所以氦气在低温领域有巨大的应用价值。氦气用途广泛,小到气球充气,大到医疗科研、国防军工和其他高科技产业,被称为“黄金气体”。氦气之所以被称为“黄金气体”,还有另一主要原因:氦气无法通过人工制备获得。一方面,从空气中提取氦气,成本可能比等体积的黄金还要贵,因此不具备工业提取价值。另一方面,由于氦气的化学性质不活泼,几乎没有固态或者液态化合物的存在形态,矿物中氦气的含量很低,且提取难度大,成本高。如图是全球氦气资源分布图:

依据文章内容,回答下列问题:
(1)、氦气能代替氢气填充飞艇,利用的氦气的物理性质是。庆典活动用氦气球比用氢气球更安全,原因是。(2)、氦气被称为“黄金气体”的原因:。(3)、氦气资源最丰富的国家是。(4)、从空气中提取氦气,不具备工业提取价值的主要原因是。 -
5、某中学化学兴趣小组同学收集一瓶河水,模拟自来水厂中水的净化过程进行实验。
 (1)、操作①是除去水中一些不溶物,该操作名称为。(2)、水是宝贵的自然资源,也是制取氢气的主要原料,如图是电解水的简易装置及微观变化图,请你根据图形回答问题。
(1)、操作①是除去水中一些不溶物,该操作名称为。(2)、水是宝贵的自然资源,也是制取氢气的主要原料,如图是电解水的简易装置及微观变化图,请你根据图形回答问题。
①写出a试管中收集到的气体是(填化学式)。
②写出电解水的反应文字表达式。
③为了使图2完整准确,请在丙图中补充相应的图形。
-
6、在①空气、②五氧化二磷、③氖气、④海水、⑤二氧化碳、⑥二氧化硫六种物质中,请回答下列问题(填序号)。(1)、不支持燃烧但能参与植物光合作用的是。(2)、有刺激性气味且会对空气造成污染的气体是。(3)、通常状况下,属于白色固体物质的是。(4)、用于制造电光源(如:霓虹灯等)的是。(5)、上述物质中属于混合物的是。
-
7、化学用语是学习和研究化学的工具,请用化学符号填空。(1)、氮元素:。(2)、三个钾原子:。(3)、氦气:。(4)、氢氧根离子:。(5)、标出氧化铝中铝元素的化合价。
-
8、逻辑推理是化学学习中常用的思维方法,下列推理正确的是A、氧化物中都含有氧元素,所以含有氧元素的化合物一定是氧化物 B、单质是由一种元素组成的纯净物,所以由一种元素组成的纯净物一定是单质 C、离子是带电的原子,所以带电的粒子一定是离子 D、金属元素原子的最外层电子数一般少于4个,所以最外层电子数少于4个的原子一定是金属元素
-
9、学习化学要构建好“宏观—微观—符号”的联系,下列说法正确的是A、分子大,原子小 B、“”可表示铜、铜元素、1个铜原子 C、钙原子和钙离子核电荷数不相同 D、原子和原子最外层电子数均为2,在化学反应中容易失去电子2
-
10、物质由微观粒子构成。下列由离子构成的物质是A、氯化钠 B、水 C、二氧化碳 D、铜
-
11、下列物质的性质中属于化学性质的是A、密度 B、溶解性 C、挥发性 D、可燃性
-
12、2023年世界环境日中国主题是“建设人与自然和谐共生的现代化”。下列做法有利于实现这一目标的是A、乘坐公共交通工具出行 B、将废气直接排入高空 C、大量燃放烟花爆竹 D、废弃塑料露天焚烧
-
13、钙是维持人体正常功能所必需的元素,如图是补钙剂“葡萄糖酸钙片”说明书的一部分。请根据图示中的相关信息计算回答下列问题:
葡萄糖酸钙片
成分:每片含葡萄糖酸钙
(化学式:)
用法:口服
用量:成人一日3次,每次4片
(1)、葡萄糖酸钙由种元素组成。(2)、葡萄糖酸钙中氢、氧元素的质量比为(填最简比)。(3)、按照说明书上用量服用,成人通过钙片每天摄入的钙元素的质量是多少?(写出计算过程,计算结果精确至0.01g) -
14、配制一定溶质质量分数的氯化钠溶液的过程如图1所示。
 (1)、写出图1中E仪器的名称: , 称量过程中仪器的指针偏左,应进行的操作是 , 溶解过程中玻璃棒的作用是。(2)、根据图2、图3可知,该小组同学配制的NaCl溶液溶质质量分数为。
(1)、写出图1中E仪器的名称: , 称量过程中仪器的指针偏左,应进行的操作是 , 溶解过程中玻璃棒的作用是。(2)、根据图2、图3可知,该小组同学配制的NaCl溶液溶质质量分数为。 (3)、若要把(2)所得溶液质量分数增加一倍,需要蒸发掉g的水。(4)、下列关于溶液的说法,正确的是________。A、只有固体可以作溶质 B、凡是均一的、稳定的液体一定是溶液 C、不饱和溶液转变为饱和溶液最简单有效的办法是加入溶质 D、物质在溶于水形成溶液的过程中,都会吸收热量
(3)、若要把(2)所得溶液质量分数增加一倍,需要蒸发掉g的水。(4)、下列关于溶液的说法,正确的是________。A、只有固体可以作溶质 B、凡是均一的、稳定的液体一定是溶液 C、不饱和溶液转变为饱和溶液最简单有效的办法是加入溶质 D、物质在溶于水形成溶液的过程中,都会吸收热量 -
15、“碳达峰、碳中和”被写入两会报告,体现了中国的大国担当。氢能是高热值清洁能源。目前,氢气的来源如图1所示。水煤气(主要成分是一氧化碳和水蒸气)在催化剂和加热条件下反应生成氢气和二氧化碳的反应是化石资源制氢过程中的重要反应之一,北京大学团队研究了在不同温度下,多种催化剂对水煤气变换反应中CO转化率的影响,结果如图2所示。

电解水制氢过程简便,但造价高昂,利用太阳能制氢是未来的发展方向,“人造太阳”的探索也就应运而生。我国“人造太阳”大科学装置“东方超环”利用的是核聚变,当氘、氚核聚变温度达到1亿摄氏度、持续时间超过1000秒,就能形成持续反应,为水分解提供能量。2020年4月,“东方超环”实现了1亿摄氏度运行近10秒,取得重大突破。除了氢气的生产,其运输、储存和利用等仍面临诸多挑战,需要人们不断探索。依据文章内容和所学知识回答下列问题。
(1)、根据图1目前氢气的主要来源是。(2)、点燃纯净的氢气,观察到火焰呈色。然后在火焰上方罩一个冷而干燥的小烧杯,过一会儿,观察到烧杯壁有且烧杯外壁发热,反应的符号表达式为。(3)、水煤气制氢最适宜的催化剂是___________。A、2%Au/α-MoC B、α-MoC C、2%Au/β-Mo2C(4)、图2中,催化剂为2%Au/α-MoC时,CO转化率和温度的关系是。(5)、根据下表信息可知氘、氚都属于氢元素,理由是。原子种类
质子数
中子数
核外电子数
氘
1
1
1
氚
1
2
1
(6)、下列说法正确的是___________(填序号)。A、α-MoC可使CO转化率接近100% B、水电解制氢的不足是造价高昂 C、利用太阳能制氢是未来发展方向 D、“东方超环”利用核裂变提供能量 -
16、如图为某同学进行电解水实验的装置图,试回答下列问题:
 (1)、图中A端为电源的(填“正”或“负”)极。(2)、在电解水实验中,将两极产生的气体的体积与时间的关系绘制成如图所示的图像。由图看出,a气体是 , b气体是。
(1)、图中A端为电源的(填“正”或“负”)极。(2)、在电解水实验中,将两极产生的气体的体积与时间的关系绘制成如图所示的图像。由图看出,a气体是 , b气体是。 (3)、如果管C中气体的体积为10mL,则管D中气体的体积约为。(4)、实验中用检验管C中气体,观察到的现象是。(5)、写出水在通电条件下反应的符号表达式 , 化学基本反应类型是。(6)、电解时,水分子分解示意图如下,补全横线上的模型图。
(3)、如果管C中气体的体积为10mL,则管D中气体的体积约为。(4)、实验中用检验管C中气体,观察到的现象是。(5)、写出水在通电条件下反应的符号表达式 , 化学基本反应类型是。(6)、电解时,水分子分解示意图如下,补全横线上的模型图。 (7)、此实验得出化学变化的实质是。(8)、水是一切生命体生存所必需的物质,我们必须爱护水资源,一方面要节约用水,另一方面要防治水体污染。请提出一条节约用水的措施。
(7)、此实验得出化学变化的实质是。(8)、水是一切生命体生存所必需的物质,我们必须爱护水资源,一方面要节约用水,另一方面要防治水体污染。请提出一条节约用水的措施。 -
17、科学界研究发现,血硒水平的高低与癌的发生息息相关:一个地区食物和土壤中硒含量高,癌症的发病率和死亡率就低,低硒或缺硒人群通过适量补硒,不但能够预防肿瘤、肝病等的发生,而且可以提高机体免疫能力,维护心、肝、肺、胃等重要器官正常功能。因此,硒被称为是人体微量元素的“防癌之王”。(1)、硒在元素周期表中方格信息和原子结构示意图如图所示。硒属于(填“金属”或“非金属”)元素,硒的相对原子质量为。硒原子的结构示意图中,X=。
 (2)、人们常摄入“富硒山药”、“富硒含胚芽油”来补充体内的“硒”,此处的“硒”指的是___________(填字母)。A、分子 B、原子 C、离子 D、元素 E、单质(3)、亚硒酸钠(Na2SeO3)中硒元素的化合价为。(4)、下图中与硒化学性质相似的原子是(填编号)
(2)、人们常摄入“富硒山药”、“富硒含胚芽油”来补充体内的“硒”,此处的“硒”指的是___________(填字母)。A、分子 B、原子 C、离子 D、元素 E、单质(3)、亚硒酸钠(Na2SeO3)中硒元素的化合价为。(4)、下图中与硒化学性质相似的原子是(填编号)
-
18、化学源于生活又服务于生活。座式酒精喷灯的火焰温度可达1000℃以上。使用时,向预热盘中注入酒精并点燃,待灯壶内酒精受热汽化从喷口喷出时,预热盘内燃着的火焰就会将喷出的酒精蒸气点燃。
 (1)、酒精喷灯火焰中(填“外焰”、“内焰”或“焰心”)部分温度最高。(2)、从材料中可得出酒精的一条化学性质是 , 一条物理性质是。(3)、铜质壶体中:铜是由(填“分子”、“原子”或“离子”)构成,铜的物质类别是(选填“化合物”、“混合物”或“单质”)。(4)、酒精完全燃烧生成二氧化碳和水,根据反应前后元素种类不变的原理,可确定酒精中一定含有元素,可能含有元素。
(1)、酒精喷灯火焰中(填“外焰”、“内焰”或“焰心”)部分温度最高。(2)、从材料中可得出酒精的一条化学性质是 , 一条物理性质是。(3)、铜质壶体中:铜是由(填“分子”、“原子”或“离子”)构成,铜的物质类别是(选填“化合物”、“混合物”或“单质”)。(4)、酒精完全燃烧生成二氧化碳和水,根据反应前后元素种类不变的原理,可确定酒精中一定含有元素,可能含有元素。 -
19、下列物质中属于纯净物的是A、洁净的空气 B、自来水 C、水银 D、豆浆
-
20、下列实验操作正确的是A、加热固体
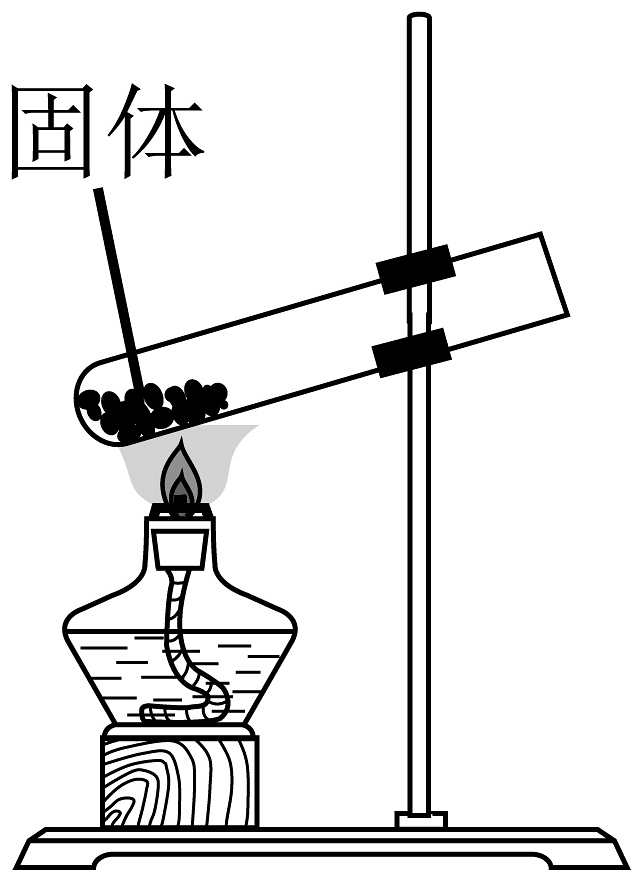 B、量取液体
B、量取液体 C、加热液体
C、加热液体 D、取粉末状固体
D、取粉末状固体