相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、我国稀土资源丰富,储量居世界第一位。铕是一种稀土元素,下列有关说法中正确的是
 A、铕属于非金属元素 B、铕原子核内中子数为63 C、铕原子核外有63个电子 D、铕的相对原子质量是152.0g
A、铕属于非金属元素 B、铕原子核内中子数为63 C、铕原子核外有63个电子 D、铕的相对原子质量是152.0g -
2、下列各选项中,解释与事实不符合的是
选项
事实
解释
A
过氧化氢和二氧化锰混合可制得氧气
化学变化中分子本身发生了变化
B
热水能使压瘪的乒乓球复原
分子受热,体积变大
C
蜡烛在空气中燃烧生成水
蜡烛中一定含有氢元素
D
湿衣服在夏天比在冬天干得快
温度升高,分子运动速率加快
A、A B、B C、C D、D -
3、下列实验操作正确的是A、液体读数
 B、滴加液体
B、滴加液体 C、液体取用
C、液体取用 D、液体加热
D、液体加热
-
4、下列有关实验现象的描述正确的是A、硫在空气中燃烧,发出明亮的蓝紫色火焰 B、红磷在空气中燃烧,产生大量白烟 C、木炭在氧气中燃烧、发出白光,生成黑色固体 D、氢气在空气中燃烧,发出淡蓝色火焰,生成水
-
5、下列前者属于混合物,后者属于氧化物的是A、稀有气体 水 B、锰酸钾 二氧化锰 C、氧气 二氧化硫 D、空气 高锰酸钾
-
6、关于铁的描述中,属于化学性质的是A、铁块是银白色的 B、铁在潮湿的空气中生锈 C、铁具有良好的导热性 D、铁能在氧气中剧烈燃烧
-
7、已知106g的质量分数为10%的碳酸钠溶液与73g盐酸恰好完全反应。求:(1)、盐酸中溶质质量分数。(2)、反应后所得溶液中溶质质量分数。
-
8、蛋白质由甘氨酸()等多种氨基酸构成。计算:(1)、“”中数字“5”的含义是。(2)、甘氨酸中氮、氧元素的质量比是。(3)、甘氨酸中碳元素的质量分数是。(4)、150g甘氨酸中含有氧元素的质量为g。(5)、氮元素质量相等的甘氨酸和硝酸铵的质量比是。(6)、某甘氨酸溶液中溶质与溶剂中所含氢元素质量相等,则该溶液溶质质量分数是。
-
9、根据下列仪器及装置,请你回答有关问题。
 (1)、写出仪器名称:① , ②。(2)、用高锰酸钾制氧气写出方程式 , 发生装置是 , 还需改进的地方是。(3)、可以用C装置收集氧气,①原因是。
(1)、写出仪器名称:① , ②。(2)、用高锰酸钾制氧气写出方程式 , 发生装置是 , 还需改进的地方是。(3)、可以用C装置收集氧气,①原因是。②收集氧气的最佳时刻是。
③实验结束时应先 , 目的是。
(4)、实验室制氢气化学方程式为 , 上述收集装置中不能用于收集氢气的是。(5)、①写出实验室制取的反应方程式 , 选择的发生和收集装置是。②验满的方法是。
-
10、写出下列反应的化学方程式。(1)、铁丝在氧气中燃烧的反应方程式。(2)、检验二氧化碳的反应方程式。(3)、铁与硫酸铜溶液反应的化学方程式为。
-
11、为验证质量守恒定律,某兴趣小组做了以下实验进行探究。
 (1)、图1用酒精灯给a端铜丝加热2分钟冷却后,观察到铜丝变黑、玻璃棒(填“a”或“b”)端下沉,写出反应方程式。(2)、在进行实验2时,发现托盘天平指针.写出反应方程式 , 二氧化锰的作用是。(3)、图3中先称量镁条和陶土网的质量为 , 然后点燃镁条,观察到 , 反应结束后称量总质量为。根据质量守恒定律可知:生成的氧化镁质量应大于参加反应的镁条质量,而实验事实是 , 原因是。(4)、根据以上实验可知,验证质量守恒定律时,对于有气体参加的反应,应在容器中进行实验。(5)、化学反应遵循质量守恒的根本原因是。
(1)、图1用酒精灯给a端铜丝加热2分钟冷却后,观察到铜丝变黑、玻璃棒(填“a”或“b”)端下沉,写出反应方程式。(2)、在进行实验2时,发现托盘天平指针.写出反应方程式 , 二氧化锰的作用是。(3)、图3中先称量镁条和陶土网的质量为 , 然后点燃镁条,观察到 , 反应结束后称量总质量为。根据质量守恒定律可知:生成的氧化镁质量应大于参加反应的镁条质量,而实验事实是 , 原因是。(4)、根据以上实验可知,验证质量守恒定律时,对于有气体参加的反应,应在容器中进行实验。(5)、化学反应遵循质量守恒的根本原因是。 -
12、溶液与人类的生活息息相关。(1)、下列少量物质分别放入水中,充分搅拌,能得到溶液的是________(填序号)。A、食盐 B、面粉 C、醋酸 D、花生油(2)、如图所示将少量液体X加到烧瓶中固体Y上,观察到气球逐渐膨胀,符合题意的组是。

A
B
C
D
X
稀盐酸
水
水
水
Y
碳酸钠
氯化钠
氢氧化钠
硝酸铵
(3)、在实验室中配制100g质量分数为16%的氯化钠溶液,需要水的质量为g。(4)、向50g质量分数为12%的硝酸钾溶液中加入5g硝酸钾固体完全溶解,所得溶液中溶质质量分数为。 -
13、根据以下与水有关的示意图回答问题(1)、小明用浑浊的河水制备纯净水,实验过程如左图:
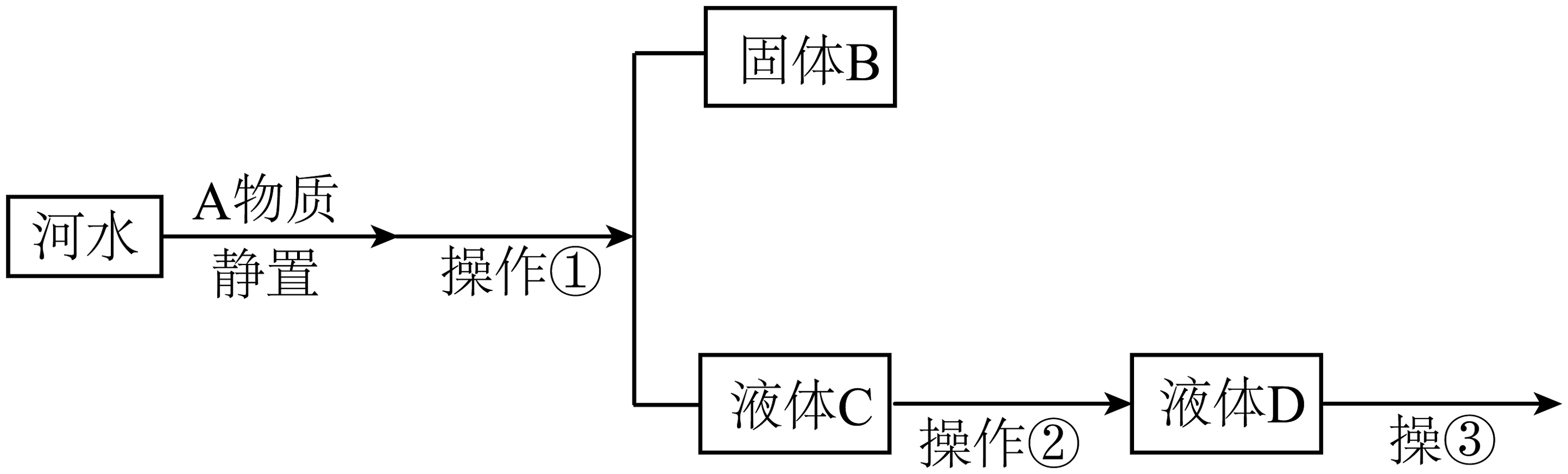
加入的A物质是 , 其作用是。操作①的名称是 , 该操作中玻璃棒的作用是。操作②常用做吸附剂除去液体C中的色素和异味。操作③的名称是。
(2)、如图为电解水的实验示意图。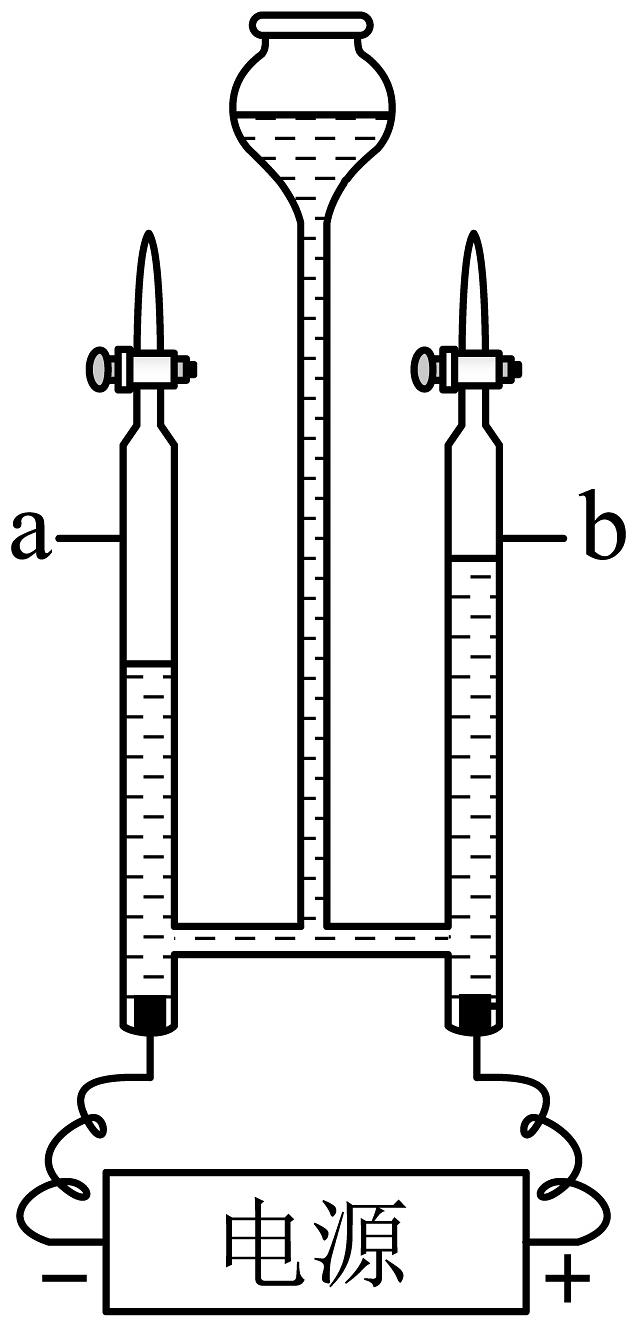
①在电解器玻璃管中加满水。通电,观察到玻璃管中有气泡冒出,a、b管内气体体积比约为。
②用燃着的木条分别检验两个玻璃管中的气体,观察到(填“a”或“b”)中气体使木条燃烧更旺。
③写出电解水的化学方程式 , 该实验得出的结论是。
-
14、在宏观、微观和符号之间建立联系是学习化学的重要思维方式。(1)、氮气是由组成的,是由构成的.(填“氮元素”或“氮原子”或“氮分子”或“氨离子”)。(2)、元素周期表中原子序数为101的元素被命名为“钔”,是纪念门捷列夫编制元素周期表所作出巨大贡献。已知钔的相对原子质量为258,则钔原子的核外电子数为。(3)、图1为氟元素在元素周期表中信息和氟原子及镁原子的结构示意图。
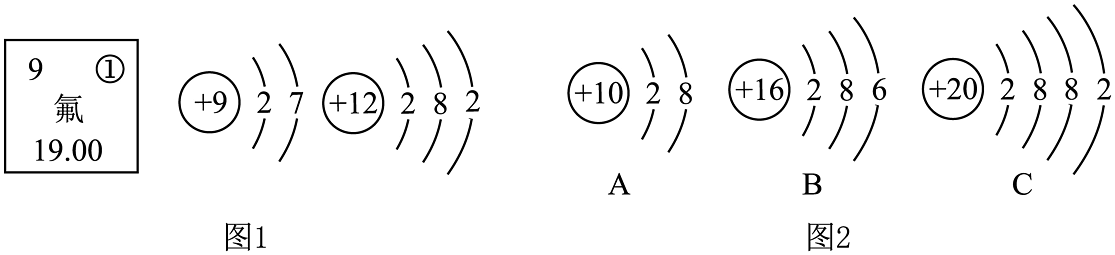
写出图中①代表的元素符号 , 写出氟化镁的化学式为。
(4)、图2中与镁原子化学性质相似的是(填序号),原因是。(5)、图2中A与B属于不同种元素,是因为它们。(6)、汽车尾气中的有害气体甲和乙在催化剂作用下反应生成丙和丁,能减轻空气污染。甲、乙、丙、丁的分子示意图如图,写出该反应的化学方程式为。甲
乙
丙
丁





-
15、化合物W在9.6g氧气中恰好完全燃烧,生成和 , 下列判断正确的是A、W的质量是5.6g B、二氧化碳与水的分子个数比为 C、W中碳元素质量分数是52.2%. D、W一定含有碳和氢元素.可能含有氧元素
-
16、如图所示的四个图象,能正确反映对应变化关系的是
 A、等量的两份过氧化氢溶液,一份中加入二氧化锰 B、水通电产生氢气和氧气的质量关系 C、将一定质量的硝酸铵固体与一定体积的水混合 D、向一定质量分数的氯化钠溶液中不断加水
A、等量的两份过氧化氢溶液,一份中加入二氧化锰 B、水通电产生氢气和氧气的质量关系 C、将一定质量的硝酸铵固体与一定体积的水混合 D、向一定质量分数的氯化钠溶液中不断加水 -
17、我国古代炼锌主要反应:① , ② , 下列说法正确的是A、X的化学式为 B、反应①是分解反应,反应②是置换反应 C、①②反应前后固体总质量一定不变 D、①②反应前后碳元素的化合价均发生改变
-
18、下列实验方案不能达到实验目的的是
选项
实验目的
实验方案
A
鉴别氢氧化钠和氯化钠固体
分别滴加等量的蒸馏水观察
B
鉴别水和5%的过氧化氢溶液
分别加入少量二氧化锰粉末,观察
C
除去碳酸钙中的泥沙
溶于水后,过滤
D
鉴别氮气和二氧化碳两种气体
将燃着的木条分别伸入气体中,观察
A、A B、B C、C D、D -
19、逻辑推理是一种重要的化学思维方法,下列推理正确的是A、质子数决定元素的种类,则质子数相同的微粒一定属于同种元素 B、和的组成元素都相同,则它们的化学性质相同 C、单质都是同种元素组成的,则由一种元素组成的纯净物一定是单质 D、溶液是均一、稳定的混合物,则均一、稳定的液体一定是溶液
-
20、制备尿素的化学方程式为。下列说法正确的是A、中N的化合价为+3价 B、尿素中氮元素的质量分数为23.3% C、参加反应的和质量比为 D、尿素中碳元素与氮元素的质量比为