-
1、下列有关实验现象的描述正确的是A、氢气和硫在空气中燃烧,火焰都呈淡蓝色 B、磷在氧气中燃烧,产生大量白色烟雾 C、铁丝在氧气中燃烧时火星四射,有四氧化三铁固体生成 D、木炭在氧气中燃烧,发出红光,生成能使澄清石灰水变浑浊的气体
-
2、下列说法错误的是A、二百多年前,用定量的方法研究空气成分的科学家是拉瓦锡 B、能形成酸雨的空气污染物主要是二氧化硫和二氧化氮 C、空气中氮气的质量分数约为78% D、工业上用分离液态空气的方法制氧气利用了液氮和液氧的沸点不同
-
3、下列物质的用途中,主要利用了其化学性质的是A、稀有气体制霓虹灯 B、氮气作保护气 C、铜丝作导线 D、活性炭净水
-
4、某同学的下列生活行为不符合环保理念的是A、骑自行车上学 B、将废弃易拉罐丢入“可回收垃圾”桶 C、用洗菜的水冲厕所 D、为预防疾病,尽量使用一次性餐具
-
5、如图是测定空气中氧气含量的实验,瓶底预留少量水吸收白烟。
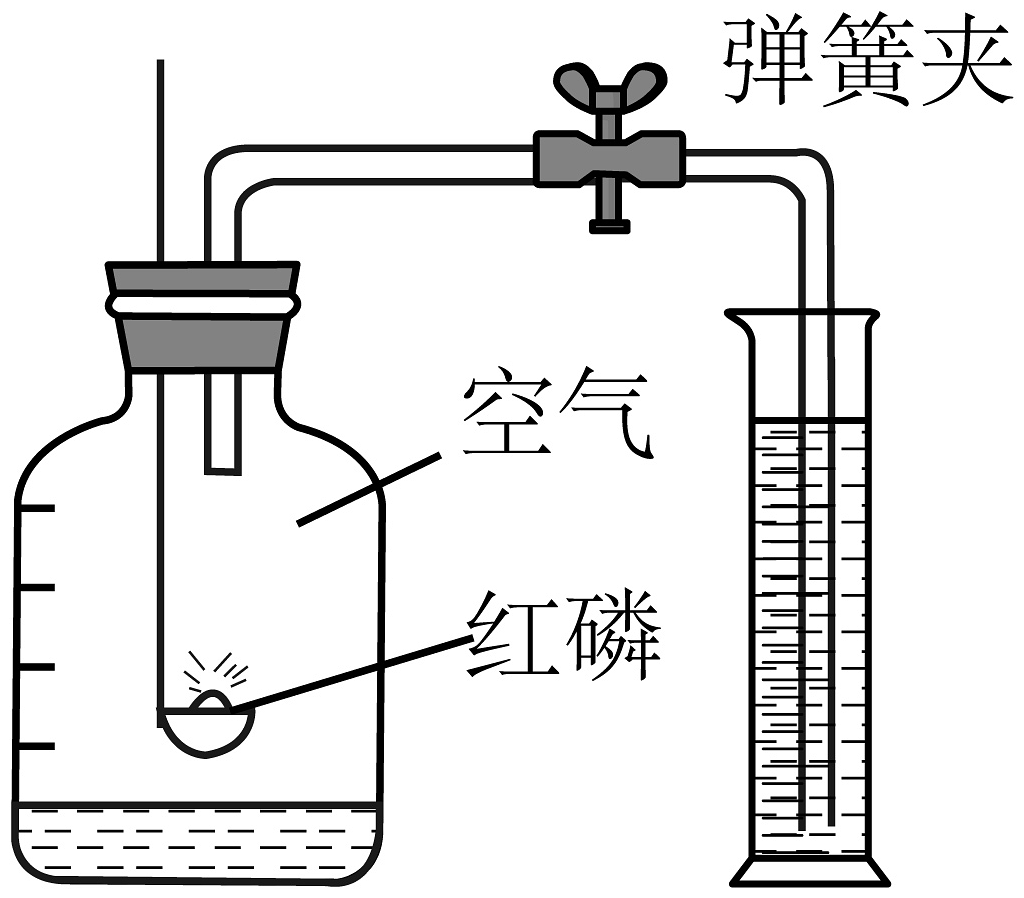 (1)、待装置冷却后打开止水夹,会看到量筒中的水;写出反应的符号表达式。(2)、已知实验前量筒中水的体积为100mL,实验后剩余水的体积为20mL,则原集气瓶内空气的体积大约是 , 原集气瓶内空气的质量是多少?(写出计算过程并保留一位小数)(标准状况下空气的密度为1.293g/L)
(1)、待装置冷却后打开止水夹,会看到量筒中的水;写出反应的符号表达式。(2)、已知实验前量筒中水的体积为100mL,实验后剩余水的体积为20mL,则原集气瓶内空气的体积大约是 , 原集气瓶内空气的质量是多少?(写出计算过程并保留一位小数)(标准状况下空气的密度为1.293g/L) -
6、
某化学兴趣小组的同学为了比较氧化铜和二氧化锰对过氧化氢分解的催化效果,用如图1所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的3mL5%的过氧化氢溶液注入试管中,利用注射器收集氧气,收集到氧气的体积和时间的关系如图2所示。
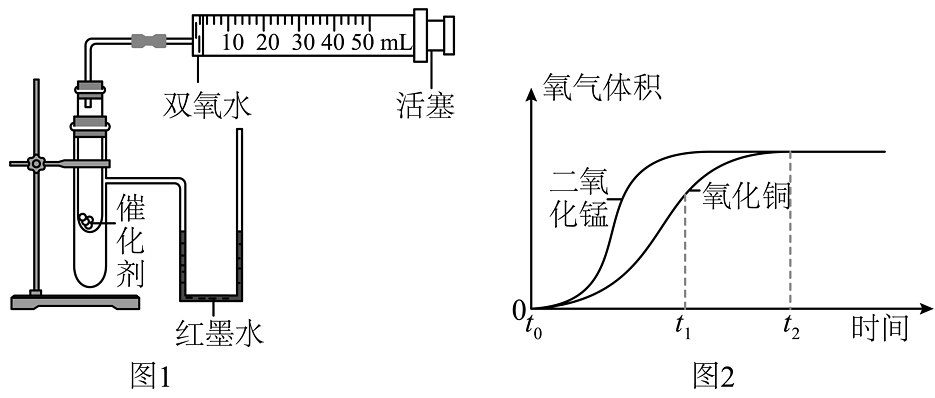
(1)催化剂是能其他物质的化学反应速率,而本身的质量和在化学反应前后都不变的物质。该反应时放热反应,反应了一段时间后,发现装有红墨水的U型管水位左边(填“下降”或“上升”)。
(2)根据相同时间注射器内氧气的体积不同,可比较两种催化剂的催化效果,通过图像得出的结论是:催化效果(填“二氧化锰”或“氧化铜”)比较好;该图像t2时间之前两条线重合在一起了,因为。
【拓展延伸】
(3)同学们在老师的指导下设计实验继续探究。向两支试管中分别加入等质量的不同浓度的过氧化氢溶液,再加上等质量、等浓度的FeCl3溶液,分别用气压传感器测定两试管中气体压力变化曲线。如图3、4所示。

①为保证实验准确性,向两支试管中加入FeCl3溶液的质量和浓度必须相等,因为。
②请你从曲线中找出FeCl3溶液对双氧水分解速率影响的一条规律性结论: , 写出该反应的符号表达式。
-
7、如图是氧气的实验室制取与性质的有关实验示意图。
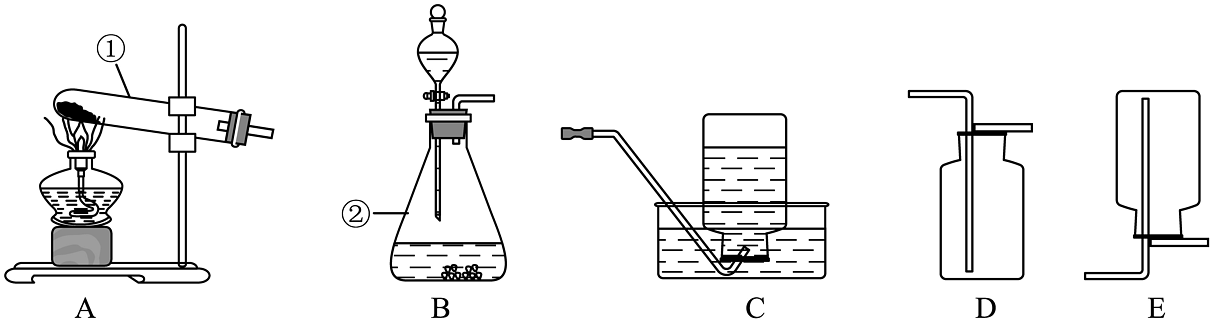 (1)、图中仪器①的名称是 , ②的名称是。(2)、实验室用装置A制取氧气的符号表达式为。(3)、欲收集一瓶干燥的氧气,可从图中选择的收集装置是(填序号),验满的方法是。如图C收集好一瓶氧气,应先再。(4)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体。已知甲烷难溶于水,密度比空气小。从图一中选择发生装置为(填序号,下同),收集装置应选。
(1)、图中仪器①的名称是 , ②的名称是。(2)、实验室用装置A制取氧气的符号表达式为。(3)、欲收集一瓶干燥的氧气,可从图中选择的收集装置是(填序号),验满的方法是。如图C收集好一瓶氧气,应先再。(4)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体。已知甲烷难溶于水,密度比空气小。从图一中选择发生装置为(填序号,下同),收集装置应选。 -
8、请你细心阅读下列物质之间的相互关系,然后回答下列问题:
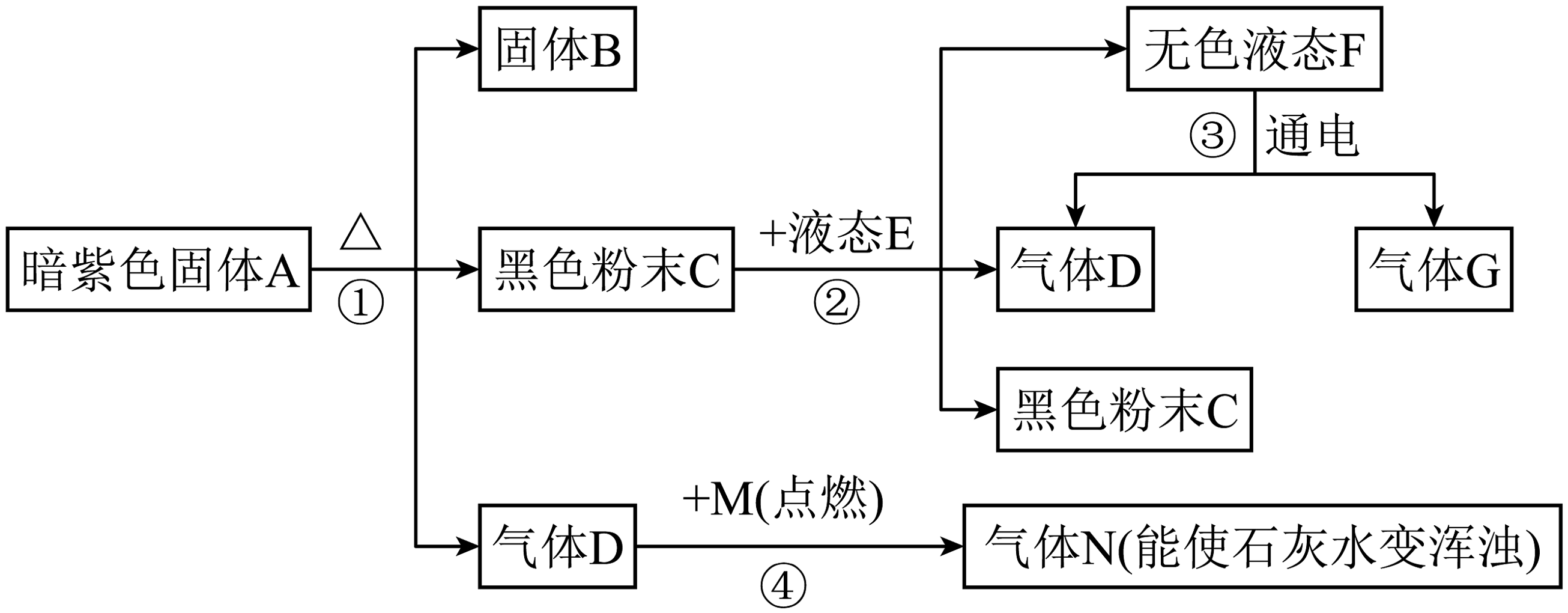 (1)、请你根据上述关系图写出下列物质的化学符号:A , C , N。(2)、写出上述关系图中①、④两步所发生反应的符号表达式:
(1)、请你根据上述关系图写出下列物质的化学符号:A , C , N。(2)、写出上述关系图中①、④两步所发生反应的符号表达式:①;
④。
-
9、2023年5月30日,我国“神舟十六号”载人航天飞船成功发射。为保证宇航员正常的生命活动,空间站内的空气需与我们周围的空气组成相近,主要采用如图循环系统:
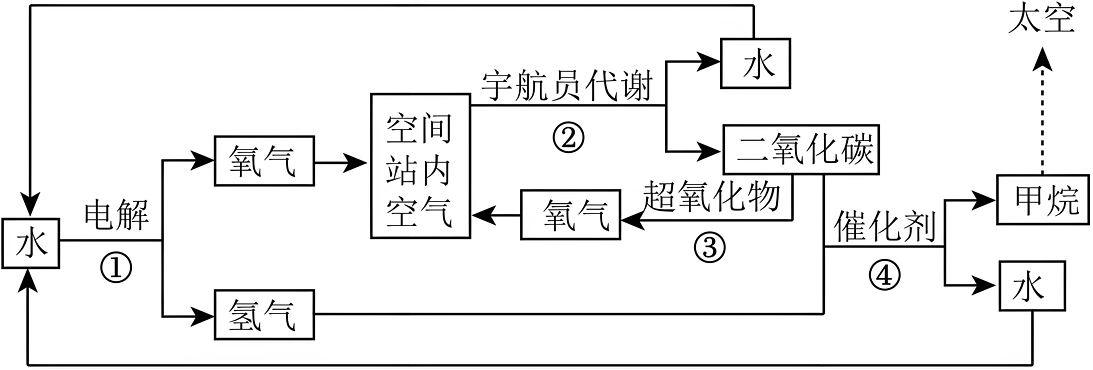 (1)、空间站内空气中含量最多且不会被宇航员消耗的气体是(填化学式),补充氧气的化学反应有(填序号,下同)。消耗氧气的化学反应有。(2)、反应④的文字表达式是;此系统中循环利用的物质有(写一种)。
(1)、空间站内空气中含量最多且不会被宇航员消耗的气体是(填化学式),补充氧气的化学反应有(填序号,下同)。消耗氧气的化学反应有。(2)、反应④的文字表达式是;此系统中循环利用的物质有(写一种)。 -
10、臭氧O3是地球大气中的一种微量气体。O3通常状况下是淡蓝色气体,有鱼腥味。O3比O2活泼得多,是一种强氧化性气体,具有较强杀菌能力,在一定条件下,O2可以转化为O3。研究人员用臭氧分析仪监测紫外灯照射产生的臭氧浓度随时间的变化,实验结果如图1。还通过实验研究了臭氧浓度与其杀菌效果的关系,结果如图2。
 (1)、O3的物理性质是(写出一点即可)。(2)、从微观的视角说明O3与O2化学性质不同的原因是。(3)、O2在一定条件下转化成O3的过程(填“是”或“不是”)化学变化。(4)、由图1可知,紫外线照射时间相同时,氧气产生的臭氧量比空气。由图2可知,臭氧浓度与其杀菌效果的关系是。
(1)、O3的物理性质是(写出一点即可)。(2)、从微观的视角说明O3与O2化学性质不同的原因是。(3)、O2在一定条件下转化成O3的过程(填“是”或“不是”)化学变化。(4)、由图1可知,紫外线照射时间相同时,氧气产生的臭氧量比空气。由图2可知,臭氧浓度与其杀菌效果的关系是。 -
11、完成如表。(1)、
元素名称
氢
硫
钾
元素符号
(2)、以下物质A.氮气;B.一氧化碳;C.二氧化碳;D.铁;E.五氧化二磷;F.氦气(填字母)。
①化学性质比较不活泼,液态情况下可用于制造低温环境的气体是;
②生活中最常用的金属是;
③可用于填充探空气球的是;
④空气中的三大污染气体之一的气体是。
-
12、下列实验方案的设计中,不能达到实验目的的是A、比较二氧化碳的含量
 B、探究二氧化锰加快反应速率
B、探究二氧化锰加快反应速率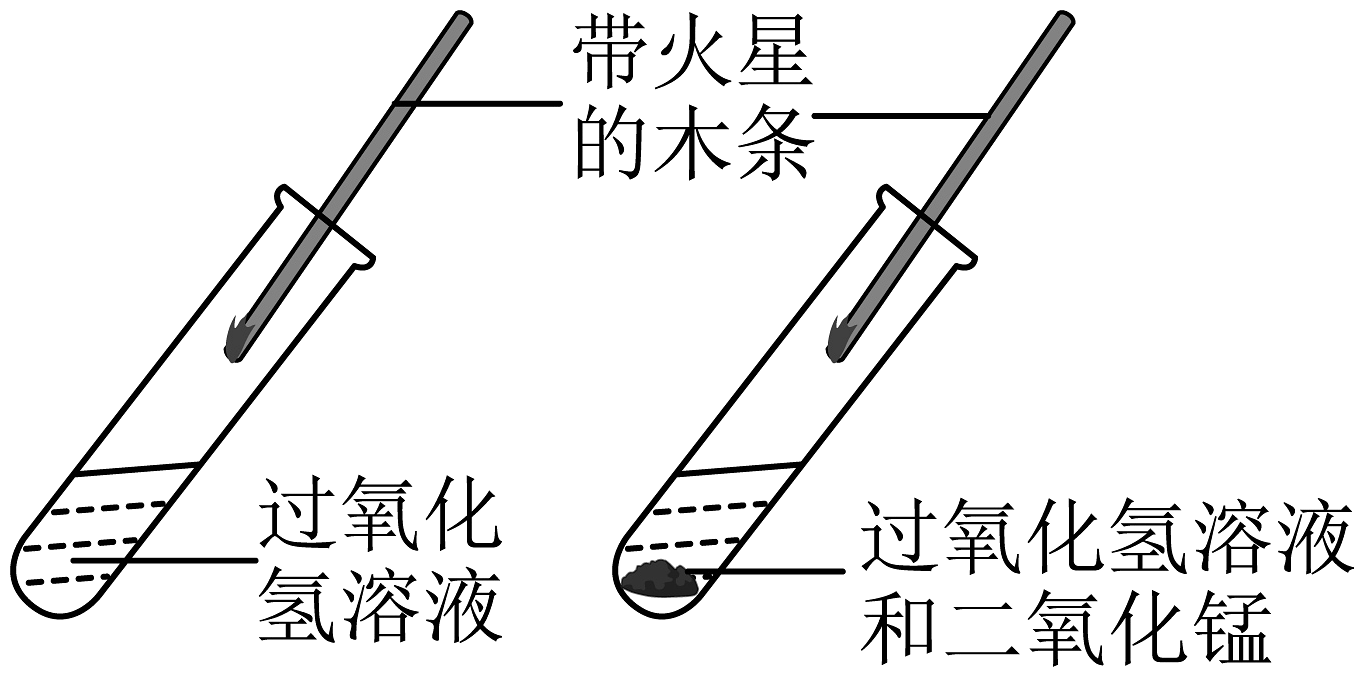 C、探究温度对微粒运动速率的影响
C、探究温度对微粒运动速率的影响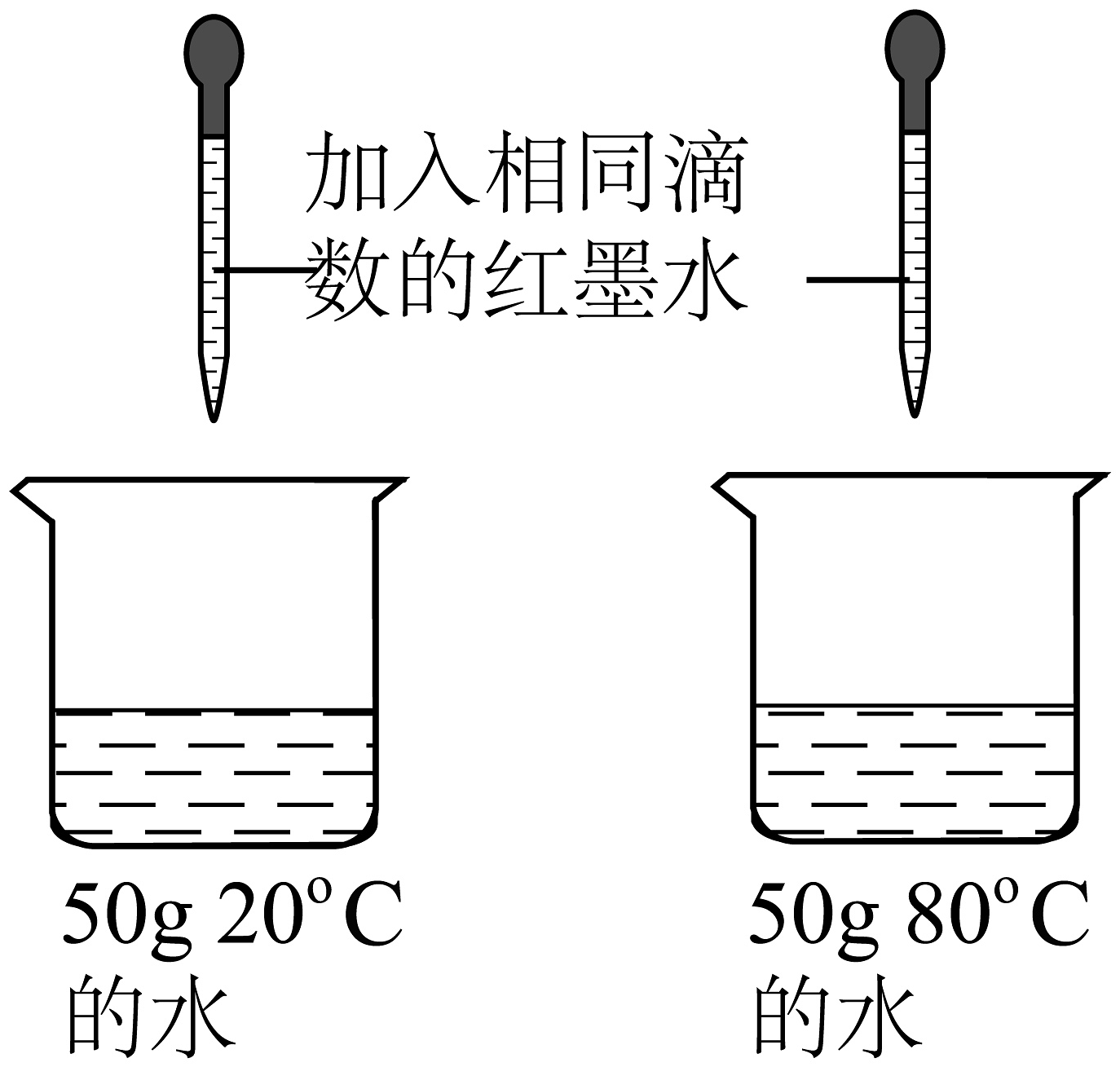 D、用排水法收集O2
D、用排水法收集O2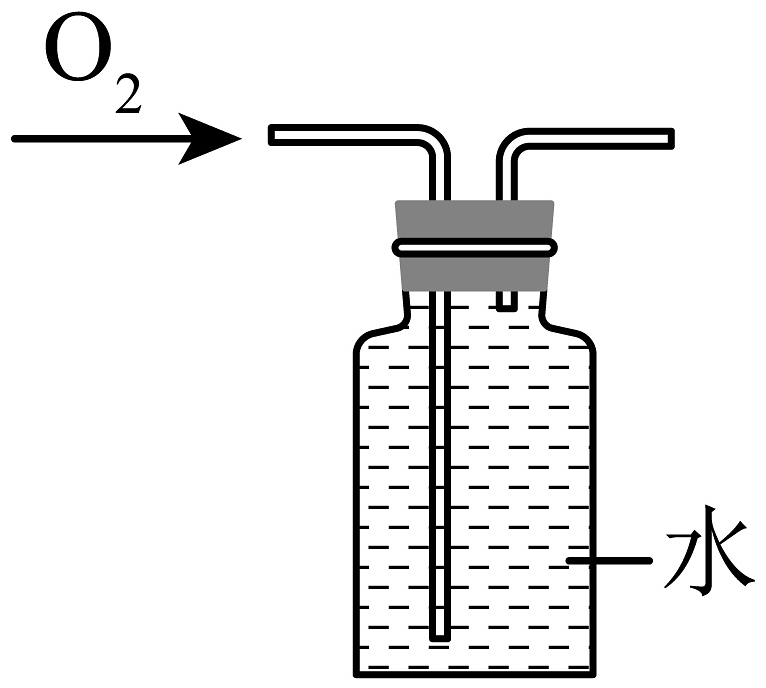
-
13、化学反应有多种类别。化合反应、分解反应、氧化反应的关系可用如图表示,其中b处表示的反应既属于化合反应,又属于氧化反应。现有反应:甲烷+氧气二氧化碳+水,则此反应应该填充到
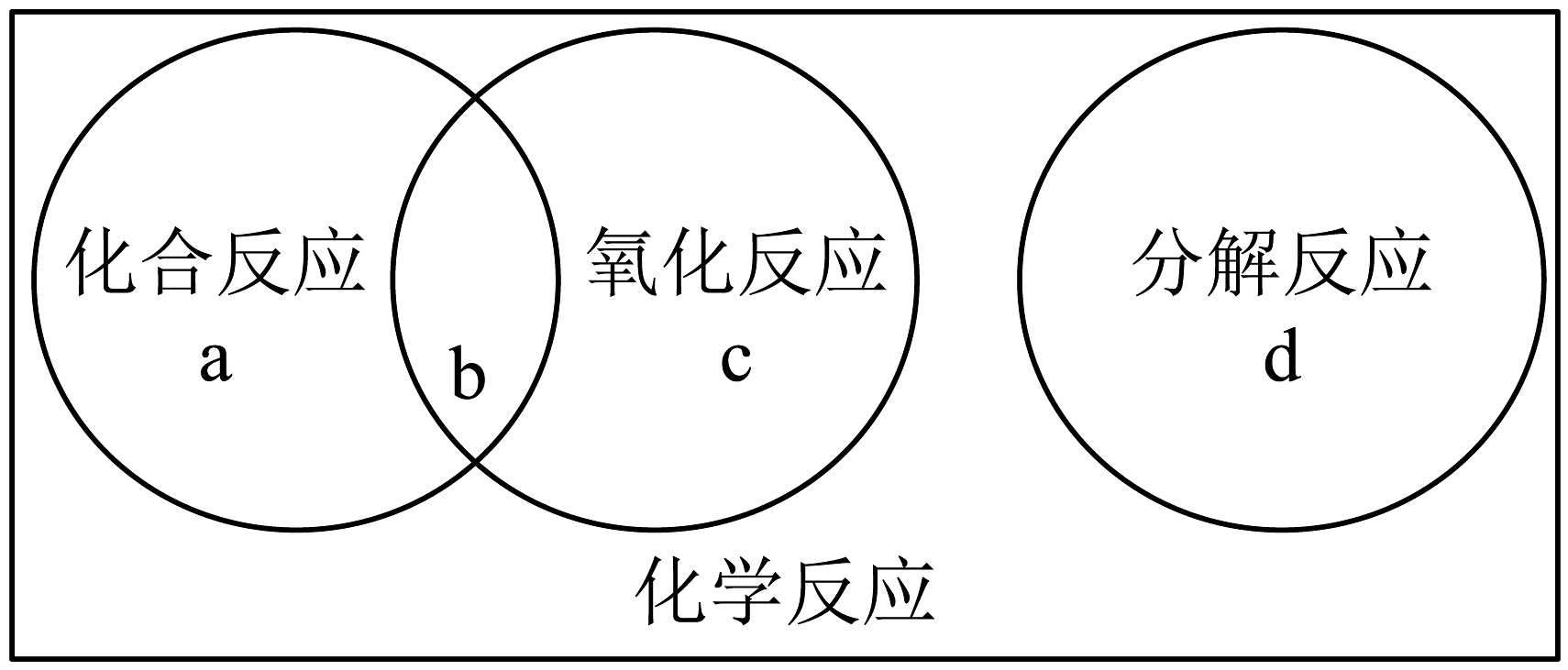 A、a处 B、b处 C、c处 D、d处
A、a处 B、b处 C、c处 D、d处 -
14、下图是氧化汞分解的微观示意图。下列根据图示的有关叙述中,正确的是
 A、反应中,发生变化的是汞原子和氧原子 B、反应中,氧化汞分子可以再分,汞原子、氧原子不能再分 C、氧化汞是由汞和氧气组成的 D、氧化汞分子是由汞分子和氧分子构成的
A、反应中,发生变化的是汞原子和氧原子 B、反应中,氧化汞分子可以再分,汞原子、氧原子不能再分 C、氧化汞是由汞和氧气组成的 D、氧化汞分子是由汞分子和氧分子构成的 -
15、拉瓦锡用定量的方法研究了空气的成分。某兴趣小组利用氧气传感器来检测足量红磷燃烧过程中氧气的含量,如图所示,下列判断正确的是
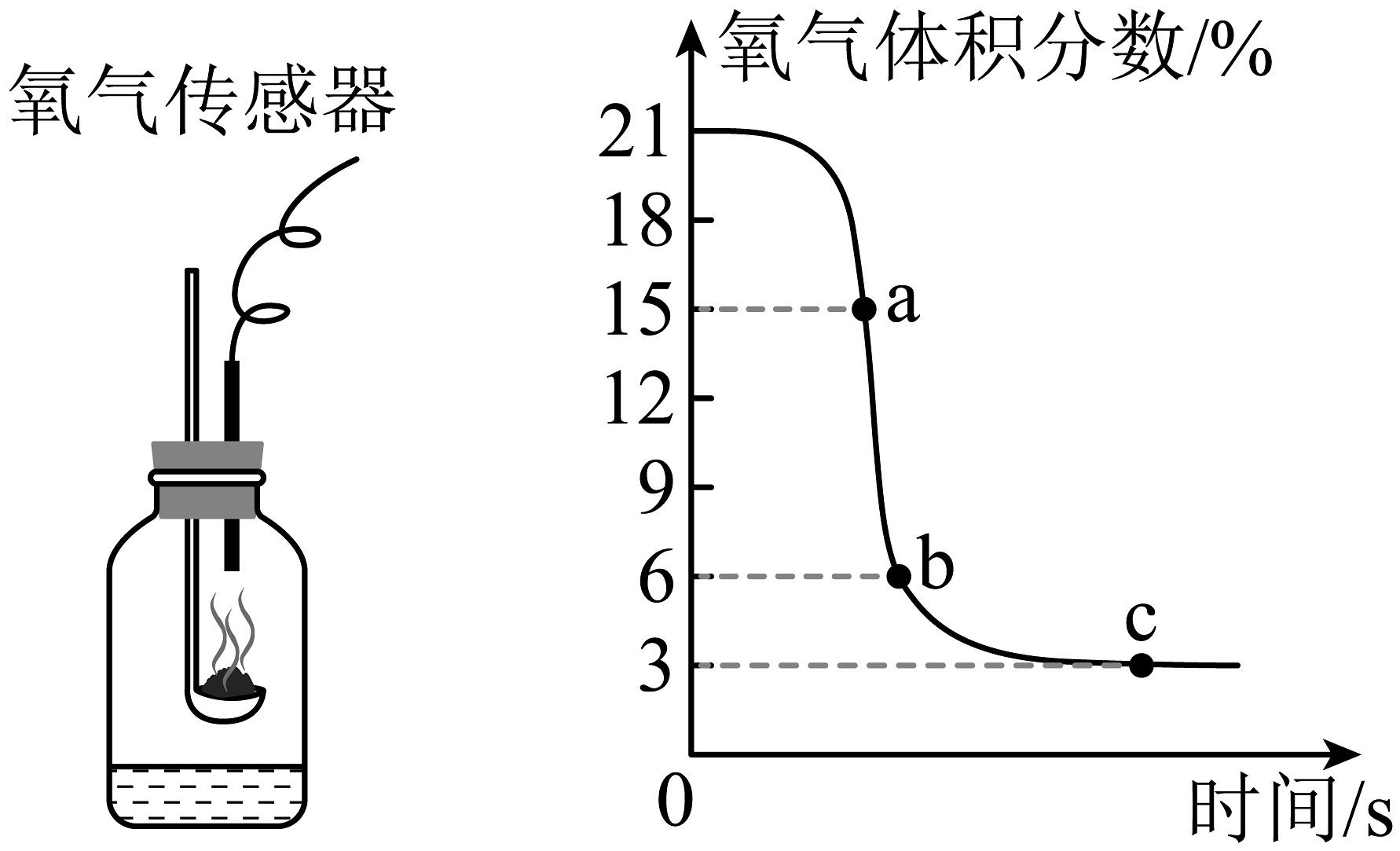 A、a点时,容器内氮气体积分数为85% B、将红磷换成木炭也能得到相似的实验数据 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、此实验测得空气中氧气的质量分数为18%
A、a点时,容器内氮气体积分数为85% B、将红磷换成木炭也能得到相似的实验数据 C、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 D、此实验测得空气中氧气的质量分数为18% -
16、下列物质燃烧的实验现象描述正确的是A、蜡烛燃烧产生黄色火焰,冒白烟 B、硫在氧气中燃烧后生成有刺激性气味的气体 C、铁丝在空气中燃烧时,火星四射,生成黑色固体 D、木炭在氧气中剧烈燃烧,发出白光,生成二氧化碳
-
17、
某实践活动小组在老师带领下,对空气质量检测等开展了一系列项目式学习活动。
活动一:了解空气质量指数所表示的含义
【思考分析】

(1)图1是该小组所在地区某日的空气质量情况,其空气质量状况为(填“优”“良”或“轻度污染”)。
活动二:认识微型空气质量“检测站”
【查询网络】微型空气质量检测系统可实时、准确地检测室外空气污染物、其结构如图2所示。
(2)太阳能板工作时发生的能量转化是。
活动三:调查微型空气质量“检测站”
观察并记录某段时间显示的数据如下表
二氧化氮
臭氧
一氧化碳
22
158
1.3
(3)除显示器显示的内容外,还需要检测的空气污染物有(写一种)。
活动四:进行实践
同学们对工厂附近的空气质量感到好奇,调研发现该工厂为了获得充足的能量。长期采用燃煤技术。于是同学们猜测该工厂排放的废气中含有二氧化硫。
【查阅资料】二氧化硫是有刺激性气味的气体,能使澄清石灰水变浑浊,也能使品红溶液褪色。
(4)设计并进行实验
实验操作
实验现象
实验结论
收集一瓶该工厂的废气,加入 , 振荡。
废气中含有二氧化硫
活动五:提出空气质量改进方案
(5)为了保护人类赖以生存的环境,我们在校园中能做什么?(写一条)。
-
18、甲醛(CH2O)是空气污染物,石墨负载MnO2催化甲醛氧化原理如图1所示:
 (1)、甲醛中碳、氧元素质量比为。图1中含氧元素质量分数最高的化合物是(填化学式)。(2)、抽取某室内空气样品2m3 , 所含甲醛充分氧化(),产生的CO2质量为0.44mg,求1m3该空气样品中甲醛的质量是多少(写出计算过程)?是否超标(最大限值为0.08mg/m3)?(3)、不同催化剂、温度对甲醛催化转化的影响如图2所示,效果最好的是(填对应曲线字母)。以单位时间内甲醛转化为CO2的百分数衡量催化转化速率,100℃时,γ-MnO2与β-MnO2催化的速率比为。
(1)、甲醛中碳、氧元素质量比为。图1中含氧元素质量分数最高的化合物是(填化学式)。(2)、抽取某室内空气样品2m3 , 所含甲醛充分氧化(),产生的CO2质量为0.44mg,求1m3该空气样品中甲醛的质量是多少(写出计算过程)?是否超标(最大限值为0.08mg/m3)?(3)、不同催化剂、温度对甲醛催化转化的影响如图2所示,效果最好的是(填对应曲线字母)。以单位时间内甲醛转化为CO2的百分数衡量催化转化速率,100℃时,γ-MnO2与β-MnO2催化的速率比为。
-
19、
兴趣小组发现实验室一片久置的铜片表面附着了一层绿色固体,通过查阅资料得知该绿色固体是铜绿[Cu2(OH)2CO3]。
(1)甲同学刮下一些铜绿进行如下探究,请完成下表:
实验装置
实验现象
实验结论

试管内壁有水雾
铜绿受热后生成
铜绿受热后生成氧化铜
气球胀大
乙同学对气球胀大的原因产生了兴趣,于是进行如下探究。
【作出猜想】
猜想Ⅰ:试管内的空气受热膨胀;
猜想Ⅱ:铜绿受热后生成二氧化碳;
猜想Ⅲ:铜绿受热后生成一氧化碳:
猜想Ⅳ:铜绿受热后生成一氧化碳和二氧化碳。
【实验与分析】
(2)熄灭酒精灯并冷却至室温后,气球仍比加热前大,证明猜想(填序号)不成立。
(3)乙同学用下图装置进行实验,发现A中 , 反应的化学方程式为 , 说明铜绿受热后生成二氧化碳;B处玻璃管内无明显现象,说明猜想(填序号,下同)不成立。
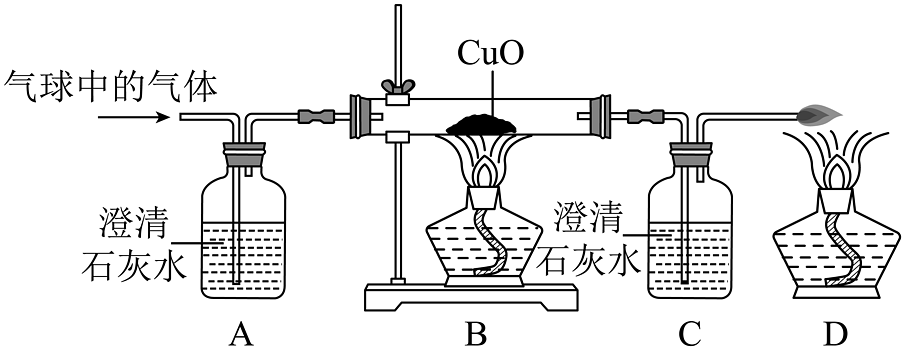
【实验结论】
(4)猜想成立。
【反思】
(5)根据铜绿的化学式可知,铜绿是铜与空气中的氧气、水和(填物质名称)共同作用形成的。
(6)丙同学认为乙同学的实验中省略A处集气瓶也能得到相同的结论,请描述与结论相对应的实验现象:。
-
20、
Ⅰ.氧气、二氧化碳制取与性质实验
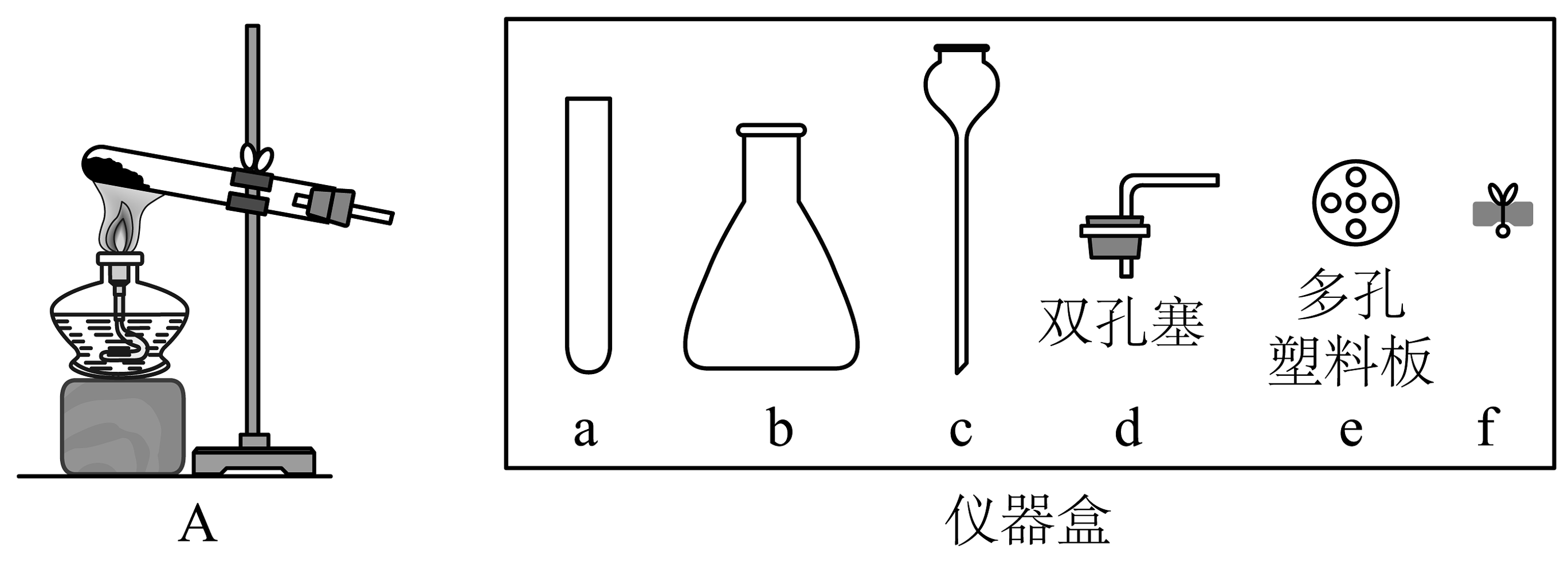
(1)用装置A(试管里装有少量高锰酸钾)制取O2的反应化学方程式是 , 试管口略向下倾斜的原因是 , 组装随开随用,随关随停制取CO2的发生装置,需选择仪器盒中的d、e和。
(2)氧气的性质实验:将装在燃烧匙的硫粉点燃,伸入集满氧气的集气瓶中,观察到硫粉燃烧,放出热量,发出火焰。硫粉燃烧生成了(填物质化学式),其中集气瓶中装有水,水的作用是。
Ⅱ.自制简易CO2吸收及供氧器
(3)利用回收材料制备一次性CO2吸收器(如下图)。O2发生器内先放入红砖粉末催化剂,倒入过氧化氢溶液,反应的化学方程式为 , 可作为CO2吸收剂的固体是。
a.CaCO3 b.Ca(OH)2 c.MnO2 d.CuO
