相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、将含有不溶性物质的硝酸钾固体的混合物放入一定量的水中充分搅拌,得到的实验数据如下:
表1:
温度/℃
20
40
60
剩余固体质量/g
136.8
72.2
20
表2:
温度/℃
20
30
40
50
60
70
80
溶解度/g
31.6
45.8
63.9
85.5
110
138
169
试计算:
(1)、原固体混合物中硝酸钾的质量是g。(2)、加入水的质量是g。 -
2、小乐查阅资料发现氯化铁可作过氧化氢溶液制取氧气的催化剂,为了验证这一说法并比较氯化铁和二氧化锰的催化能力强弱,小乐利用如图所示装置和下述实验步骤进行实验

步骤1:正确连接装置,并检查装置气密性;
步骤2:按表所示实验药品及用量进行实验
组别
5%的过氧化氢溶液/mL
催化剂种类及质量/g
60s内收集到氧气的体积/mL
1
20
无
2
20
二氧化锰m
3
20
氯化铁m
步骤3:待第3组实验完全反应后,进行如下处理
 (1)、装置连接的正确顺序是(用小写字母表示)。(2)、为了比较氯化铁和二氧化锰的催化能力强弱,在此实验中可依据的现象是。(3)、若氯化铁是过氧化氢溶液制取氧气的催化剂,则m、m1、m2符合的等式是。
(1)、装置连接的正确顺序是(用小写字母表示)。(2)、为了比较氯化铁和二氧化锰的催化能力强弱,在此实验中可依据的现象是。(3)、若氯化铁是过氧化氢溶液制取氧气的催化剂,则m、m1、m2符合的等式是。 -
3、将某无色混合气体依次进行如下实验(假设每步实验均作用完全):①通过氢氧化钠固体后,气体体积变小;②通过灼热的氧化铜粉末,粉末变为红色;③通过白色硫酸铜粉末,粉末变为蓝色:④通过澄清石灰水,溶液变浑浊。试推断原混合气体的组成可能是A、H2、CO B、CO、CO2、H2O(气) C、H2、CO2 D、H2、CO、H2O(气)
-
4、研究生石灰(CaO)露置于空气中变质的情况设计实验如下
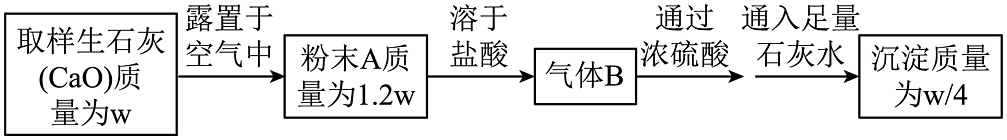
则下列结论错误的是
A、粉末A中CaO的质量为0.62w B、粉末A中钙元素的质量与生石灰样品中钙元素的质量相等 C、粉末A中CaO的吸收H2O的质量为0.09w D、由气体B可确定粉末A中含有 CaCO3由沉淀的质量可确定其质量为w/4 -
5、取 1.6g某物质在足量氧气中完全燃烧,生成4.4g二氧化碳和3.6g水,关于该物质的组成有下列论断:①一定含 C、H;②一定不含 О;③可能含 О; ④一定含O;⑤分子中 C、H 的原子个数比为 1:2;⑥分子中C、H的原子个数比为 1:4.其中正确的是A、①②③ B、①②⑤ C、①③⑥ D、①④⑤
-
6、容器内有 A、B、C、D 四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表,下列说法正确的是
物质
A
B
C
D
反应前质量/g
19.7
8.7
31.6
0.4
反应后质量/g
待测
17.4
0
3.6
A、反应后密闭容器中A的质量为19.7克 B、物质C一定是化合物,物质D可能是单质 C、反应过程中,物质B与D变化的质量比为87:36 D、A与C的相对分子质量之比为197:316 -
7、注射器是一种常见的医疗器械,它在初中科学实验中的巧妙使用可使实验操作更简洁、现象更明显。以下对注射器在实验中的使用及实验分析正确的是
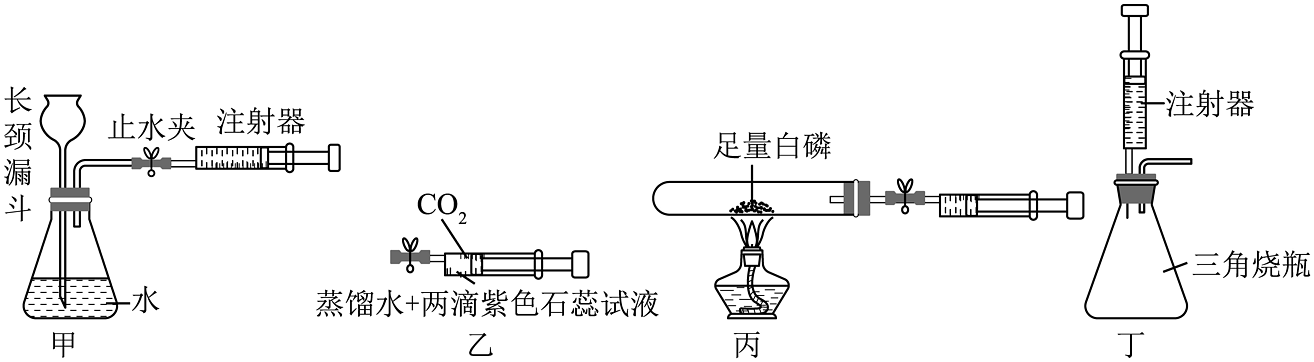 A、甲中注射器用于气密性检査,打开止水夹,快速向外拉活塞,若长颈漏斗口有气泡产生,则气密性一定良好 B、乙中注射器作反应容器,夹紧弹簧夹振荡,紫色石变红,则 CO2是酸 C、丙中的注射器可用于气体体积的测量,该装置测量的是红磷燃烧后试管中剩余气体的体积 D、丁中的注射器代替了长颈漏斗,优点之一为可节约试剂用量
A、甲中注射器用于气密性检査,打开止水夹,快速向外拉活塞,若长颈漏斗口有气泡产生,则气密性一定良好 B、乙中注射器作反应容器,夹紧弹簧夹振荡,紫色石变红,则 CO2是酸 C、丙中的注射器可用于气体体积的测量,该装置测量的是红磷燃烧后试管中剩余气体的体积 D、丁中的注射器代替了长颈漏斗,优点之一为可节约试剂用量 -
8、当汽车尾气产生的NO2在日光照射下分解成为NO和氧原子时,即开始光化学烟雾的循环,不断地产生O2 , 这个循环包括下列3个化学方程式:(1)NO2=NO+O;(2)___________;(3)O+O2=O3 , 则(2)中的化学方程式是A、NO+O=NO B、2NO+O2=2NO2 C、O3=O+O2 D、2N2+2O3=4NO+O2
-
9、下列实验方案能达到实验目的的是
选项
实验目的
实验方案
A
鉴别羊毛和棉线
灼烧后闻气味
B
验证质量守恒定律
50g水和 50g酒精混合后为100g
C
检验氧气已收集满
将带火星的木条伸入集气瓶
D
稀释浓硫酸
将水倒入浓硫酸中并用玻璃棒搅拌
A、A B、B C、C D、D -
10、遵守实验室规则是安全进行实验并获得成功的重要保证。下列同学做法中,值得肯定的是A、小枚同学乐于助人,把小娟实验用完的废液直接倒入下水道 B、进入实验室后,小萍看到实验桌上有白糖,尝了一小口 C、小毛看了某电视剧中炸喷泉的情节,于是偷偷地去化学实验室把某种药品拿了出来 D、小君想知道某气体的气味,用手在瓶口轻轻扇动,使少量气体飘入鼻孔
-
11、在牙膏中,常用轻质碳酸钙粉末等作摩擦剂。已知某品牌牙膏中的摩擦剂是CaCO3和SiO2(SiO2既不溶于水也不与稀盐酸反应),化学兴趣小组为测量该牙膏中CaCO3的含量,通过实验测得下图数据:(假设产生气体全部逸出)
 (1)、生成CO2的质量为g。(2)、求牙膏中碳酸钙的质量分数。(写出计算过程)
(1)、生成CO2的质量为g。(2)、求牙膏中碳酸钙的质量分数。(写出计算过程) -
12、如图所示是自然界存在的三大重要循环——“水循环”“氧循环”和“碳循环”。用学科观点分析碳循环和氧循环,其中正确的是
 A、变化观:每个人都在参与碳、氧循环,碳循环中的“碳”是指二氧化碳 B、守恒观:碳、氧循环过程中各元素守恒 C、平衡观:碳、氧循环使得大气中氧气增加和二氧化碳减少 D、微粒观:绿色植物的光合作用会使自然界中的氧原子总数增加
A、变化观:每个人都在参与碳、氧循环,碳循环中的“碳”是指二氧化碳 B、守恒观:碳、氧循环过程中各元素守恒 C、平衡观:碳、氧循环使得大气中氧气增加和二氧化碳减少 D、微粒观:绿色植物的光合作用会使自然界中的氧原子总数增加 -
13、农业上常用氯化钠溶液来选种。化学兴趣小组从农科站取来36g氯化钠溶液测定其溶质的质量分数。向36g氯化钠溶液中逐滴滴入硝酸银溶液至不再产生白色沉淀,共消耗硝酸银溶液100g,过滤,测得滤液质量为121.65g。计算:
(温馨提示:NaCl+AgNO3=AgCl↓+NaNO3)
(1)、产生沉淀的质量为g。(2)、该氯化钠溶液中溶质的质量分数。 -
14、
盐酸作为一种在化学实验中频繁使用的试剂,具有极为广泛的用途。
(1)请写出盐酸的一种用途:。
【问题】浓盐酸敞口放置在空气中溶质质量分数会减小,那么稀盐酸散口放置在空气中溶质质量分数是否减小?对此问题,某兴趣小组进行了下列实验探究:

【提出猜想】
(2)猜想一:溶质质量分数减小;猜想二:溶质质量分数增大;猜想三:溶质质量分数。
【查阅资料】pH计可较精确地测定溶液的pH;能与稀盐酸反应生成。
【进行实验】取适量稀盐酸分为两等份(如图1),一份密封保存(下称甲),另一份敞口放置15天(下称乙)实验Ⅰ:用pH计测两份稀盐酸的pH(结果如下表)。
试样
甲
乙
pH
0.6
0.5
(3)上表数据说明敞口放置的稀盐酸酸性较(填“强”或“弱”),也说明猜想成立。
实验Ⅱ:用图2装置和药品分别测定两份稀盐酸与粉末反应产生的体积(结果如表)。
试样
甲
乙
V()
V(甲)
V(乙)
(4)测得V(甲)V(乙)(选填“>”、“<”或“=”),也得出了与实验1相同的结论。
【反思交流】
从微观角度分析,为什么稀盐酸加热后溶质质量分数会出现上述变化?
【实验再探】
(5)加热稀盐酸,在试管口放置紫色石蕊试液浸泡后干燥的纸花。纸花变红,说明稀盐酸中的HCl和不断扩散。那么导致上述实验中结果的原因是逸出HCl和的组分之比(选填“>”、“<”或“=”)原溶液中组分之比。
-
15、某同学配制50g溶质质量分数为16%的氯化钠溶液,整个操作过程如图所示。
 (1)、配制溶液的正确操作顺序为_____(填字母)。A、①②③④⑤ B、②①⑤③④ C、②①③④⑤(2)、配制溶液需要氯化钠固体的质量为g;(3)、该实验操作中错误的是(填序号)。(4)、经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是_____(填字母)。A、氯化钠固体不纯 B、加水时有水洒落到烧杯外 C、量筒取水时仰视读数 D、溶解时烧杯内壁有水珠
(1)、配制溶液的正确操作顺序为_____(填字母)。A、①②③④⑤ B、②①⑤③④ C、②①③④⑤(2)、配制溶液需要氯化钠固体的质量为g;(3)、该实验操作中错误的是(填序号)。(4)、经检测,该同学配制的溶液溶质质量分数偏大,可能的原因是_____(填字母)。A、氯化钠固体不纯 B、加水时有水洒落到烧杯外 C、量筒取水时仰视读数 D、溶解时烧杯内壁有水珠 -
16、燃煤电厂所排放的脱硫废水中含氯化钙、氯化镁、硫酸镁等物质,由于水中含有钙离子和镁离子,导致其水的硬度较高。以下是除去这些离子(即钙离子和镁离子)的一种工艺流程。
 (1)、“沉淀”时需要不断搅拌,目的是。(2)、加入稀盐酸后,和稀盐酸发生中和反应的物质是。(3)、上述流程中须先加熟石灰后加碳酸钠,添加顺序不能颠倒,原因是。
(1)、“沉淀”时需要不断搅拌,目的是。(2)、加入稀盐酸后,和稀盐酸发生中和反应的物质是。(3)、上述流程中须先加熟石灰后加碳酸钠,添加顺序不能颠倒,原因是。 -
17、认真阅读下列科普短文。
关于什么是酸和碱,其理论的形成有如下发展历程。
观点1:17世纪前,人们对酸碱的认识较模糊,只凭感觉器官的感受来判定。
观点2:17世起末,朴素的酸碱理论,凡物质的水溶液能使石蕊试液变红的物质叫酸:使石蕊试液变蓝的物质叫碱。
观点3:19世纪末,酸碱电离理论:电离(解离)时生成的阳离子全都是的化合物叫酸,电离(解离)时生成的阴离子全都是的化合物叫碱。
观点4:20世纪初,酸碱质子理论,任何能给出质子的物质(分子、原子或离子)都是酸,任何能接受质子的物质(分子、原子或离子)都是碱,且酸和碱有如下关系:酸→+碱,两者彼此联系在一起叫做共轭酸碱对。酸失去一个质子后形成的物质叫做该酸的共轭碱,碱结合一个质子后形成的物质叫做该碱的共轭酸。
依据短文内容,回答下列问题。
(1)、根据观点1的判断,人们常吃的柠檬中含有(选填“酸”或“碱”)。(2)、往碳酸氢钠溶液中滴加紫色石蕊溶液,溶液变蓝色,根据观点2,得到的结论是。(3)、硫酸氢钠溶液中含氢离子,钠离子和硫酸根离子,根据观点3,硫酸氢钠(填“是”或“不是”)酸。(4)、已知稀盐酸的解离方程式为 , 根据观点4,盐酸的共轭碱是(填化学符号)。 -
18、下图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
 (1)、A点的含义是。(2)、若甲中混有少量乙,最好采用的方法提纯甲(填“降温结晶”或“蒸发结晶”)。(3)、将30℃时50g固体甲加入到50g水中充分搅拌溶解,得到的溶液质量为g。
(1)、A点的含义是。(2)、若甲中混有少量乙,最好采用的方法提纯甲(填“降温结晶”或“蒸发结晶”)。(3)、将30℃时50g固体甲加入到50g水中充分搅拌溶解,得到的溶液质量为g。 -
19、请参加“氯化钠欢乐之旅”的实践活动。(1)、活动一:参观盐场
利用风吹和日晒使海水不断蒸发至有晶体析出,此过程溶液中NaCl的质量分数逐渐(选填“增大”或“减小”)。
(2)、活动二:同学们查阅资料发现氯化钠是一种重要的化工原料,氯化钠溶液通电能产生火碱、氯气()和另一种可燃性气体。请写出电解氯化钠溶液发生的化学反应方程式。 -
20、氢氧化钙是白色粉末状物质,微溶于水,其水溶液俗称石灰水。氢氧化钙可由生石灰(CaO)与水反应得到。农业上可用氢氧化钙与硫酸铜等配制具有杀菌作用的波尔多液作为农药使用。(1)、氢氧化钙俗称消石灰或;(2)、请写出生石灰与水反应的化学方程式:。