相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、写出下列反应的化学反应方程式。(1)、镁带在空气中燃烧。(2)、铜在空气中加热。(3)、红磷在空气中燃烧。(4)、硫在氧气中燃烧。
-
2、水是人及切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识。请你回答:(1)、天然水中含有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的方法是。(2)、下列关于水的说法中,不正确的有(填序号)。
①冰水混合物属于纯净物
②清澈、透明的泉水是纯净物
③合理使用农药、化肥,以减少水体污染
④将明矾放入硬水中可使其软化
⑤洗菜、洗衣后的水可以用来浇花、冲洗厕所
(3)、如图所示,电解水的实验中试管a、b中产生气体的体积比约为。写出该反应的化学方程式 , 该实验证明水是由组成的。
-
3、化学是在原子、分子水平上研究物质及其变化的科学。
(1)用数字和化学符号填空
①1个氢分子;
②2个氧原子;
③3个二氧化氮分子;
④4个硫酸根离子。
(2)构成物质的粒子之间的关系如图所示。回答下列问题:

①甲是;
②在氧气、汞、氯化钠三种物质中,由原子直接构成的物质是;
③保持氧气化学性质的最小粒子是。
(3)下表列出了部分元素的原子结构示意图,请回答下列问题:
O
Na
Mg
Cl




①氧原子的核电荷数为;
②钠原子在化学反应中易(填“得到”或“失去”)电子。
③由镁元素和氯元素组成化合物的化学式为。
-
4、化学就在我们身边。现有①氧气②氢气③氖气④氮气。选择适当物质填空(填序号)。
(1)焊接金属时常用作保护气的是;
(2)可充入霓虹灯且通电时会发出有色光的是;
(3)密度最小的气体是;
(4)炼钢、气焊、航天、医疗等行业均需要用到的是。
-
5、甲、乙、丙、丁四种物质在密闭容器中发生化学反应,反应前后各物质的质量变化情况如表所示,则下列说法正确的是
物质名称
甲
乙
丙
丁
反应前质量/g
20
10
20
0
反应后质量/g
6
x
8
26
A、甲可能是单质 B、乙、丙、丁是生成物 C、乙可能是该反应的催化剂 D、该反应为分解反应 -
6、酒精灯中的燃料的主要成分是乙醇(C2H5OH),下列有关乙醇的说法正确A、乙醇的相对分子质量为46克 B、1个乙醇分子由8个原子构成 C、乙醇中碳元素的质量分数约为52.2% D、乙醇中H、O两种元素的质量比为5:16
-
7、建立宏观与微观联系是化学常用的思维方式。下列对宏观事实的微观解释,不正确的是A、湿衣服在阳光下比在阴凉处干得快——温度越高,分子运动速率越快 B、夏季在校园里闻到阵阵花香——分子在不断地运动 C、氧气和臭氧(O3)性质不完全相同——构成物质的分子不同 D、气体可压缩储存于钢瓶中——压强增大,气体分子变小
-
8、稀土元素是一类有重要用途的资源。铈(Ce)是一种常见的稀土元素,下列有关说法错误的是( )
 A、铈原子的原子序数是58 B、铈属于非金属元素 C、铈原子中的核外电子数是58 D、铈的相对原子质量是140.1
A、铈原子的原子序数是58 B、铈属于非金属元素 C、铈原子中的核外电子数是58 D、铈的相对原子质量是140.1 -
9、下列图示实验操作中,正确的是A、点燃酒精灯
 B、检查装置气密性
B、检查装置气密性 C、滴加液体
C、滴加液体 D、读取体积数据
D、读取体积数据
-
10、
关于催化剂的研究是一项重要的课题,某化学兴趣小组以“探究催化剂的奥秘”为题展开了项目式学习。
【任务一】认识催化剂
(1)催化剂在化工生产中起着重要作用,下列说法正确的是______。
A. 不加入催化剂化学反应就不能发生 B. 在化学反应前后催化剂的性质不发生改变 C. 用作催化剂的物质不可能是其他反应的反应物或生成物 D. 同一反应可能有多种催化剂 【任务二】探究催化制
查阅资料发现氧化铜(CuO)也可以作为过氧化氢分解的催化剂,于是进行相应探究。称量0.2g氧化铜,取5mL5%的过氧化氢溶液于试管中,进行如图所示实验。

(2)填写表格:
步骤①现象
步骤⑥现象
步骤⑦现象
实验结论
试管中有极少量气泡产生,带火星的木条没有复燃
称得氧化铜的质量为________
溶液中有气泡冒出
氧化铜是过氧化氢分解反应的催化剂
(3)步骤①③对比可以说明________。
(4)步骤⑦的目的是________。
【任务三】
(5)该小组探究MnO2、CuO对过氧化氢分解的催化效果。设计的方案和记录的数据如表所示:
实验序号
过氧化氢溶液
催化剂
收集50mLO2所用时间
实验1
30mL2%
粉末状MnO20.2g
21s
实验2
30mL2%
粉末状CuO0.2g
47s
①结论:MnO2与CuO哪种物质对过氧化氢分解的催化效果更好?________(填物质化学式)
②要比较MnO2、CuO对过氧化氢分解的催化效果,还可以测量________。
③如图装置可用来测量生成氧气的体积,C框内应选用的仪器为________。

-
11、如图是实验室常见的制取气体的装置:
 (1)、写出图中标有①的仪器名称:。(2)、用高锰酸钾加热制取氧气时,选用的发生装置A,反应的符号表达式。(3)、实验室如果选用装置E收集氧气,当集气瓶里的水排完后,在水下用玻璃片盖住集气瓶口,将集气瓶移出水面,(填“正”或“倒”)放在桌面上。(4)、实验室选用装置BF组合制取并收集氧气,加液体时液面高度至少应该在(填“a”或“b”)处以上,原因是;O2应从F装置导管口(选填“c”或“d”)端通入。(5)、甲烷难溶于水,且密度比空气小,实验室常用加热固体醋酸钠和固体碱石灰的混合物来制取甲烷,发生装置应用(填序号,下同),欲收集干燥的甲烷最好用装置。
(1)、写出图中标有①的仪器名称:。(2)、用高锰酸钾加热制取氧气时,选用的发生装置A,反应的符号表达式。(3)、实验室如果选用装置E收集氧气,当集气瓶里的水排完后,在水下用玻璃片盖住集气瓶口,将集气瓶移出水面,(填“正”或“倒”)放在桌面上。(4)、实验室选用装置BF组合制取并收集氧气,加液体时液面高度至少应该在(填“a”或“b”)处以上,原因是;O2应从F装置导管口(选填“c”或“d”)端通入。(5)、甲烷难溶于水,且密度比空气小,实验室常用加热固体醋酸钠和固体碱石灰的混合物来制取甲烷,发生装置应用(填序号,下同),欲收集干燥的甲烷最好用装置。 -
12、元素周期表是学习和研究化学的重要工具。完成下列问题。
 (1)、不同种元素的最本质区别是不同。(2)、氮和磷为同族元素,其化学性质相似,是因为两种原子相同。(3)、写出元素X的离子符号 , Y单质的化学式为。(4)、氧原子核外电子是。(5)、原子序数分别为1、8、11的三种元素组成的化合物是(填化学式)。
(1)、不同种元素的最本质区别是不同。(2)、氮和磷为同族元素,其化学性质相似,是因为两种原子相同。(3)、写出元素X的离子符号 , Y单质的化学式为。(4)、氧原子核外电子是。(5)、原子序数分别为1、8、11的三种元素组成的化合物是(填化学式)。 -
13、水是一种重要的资源,爱护水资源,人人有责。(1)、如图所示,电解水的实验中,通电一段时间后,玻璃管a中收集到的气体是(填化学式),该反应的文字(或符号)表达式是。通过实验可以得出水是由组成的。
 (2)、下列做法会造成水体污染的是(填序号)。
(2)、下列做法会造成水体污染的是(填序号)。①工业废水处理达标后排放
②随意丢弃废旧电池
③提倡使用无磷洗衣粉
④合理使用化肥和农药
(3)、生活中,同学们发现烧水壶内壁经常出现水垢,则该自来水为(填“硬水”或“软水”)。 -
14、用化学用语填空。(1)、氨气。(2)、5个铁原子。(3)、2个铝离子。(4)、保持过氧化氢化学性质的微粒。
-
15、如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,下列说法中不正确的是
 A、红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹 B、实验时红磷一定要过量 C、实验前一定要检验装置的气密性 D、该实验证明空气中氧气的含量约占总体积的
A、红磷燃烧产生大量的白雾,火焰熄灭后立刻打开弹簧夹 B、实验时红磷一定要过量 C、实验前一定要检验装置的气密性 D、该实验证明空气中氧气的含量约占总体积的 -
16、下列有关催化剂的说法正确的是A、二氧化锰是所有化学反应的催化剂 B、加入二氧化锰催化剂,双氧水生成的氧气增加 C、催化剂在反应前后化学性质和质量不变 D、双氧水中不加二氧化锰,化学反应不能发生
-
17、建设环境友好型社会是全社会共同的责任。下列物质中不属于空气污染物的是A、二氧化硫 B、二氧化碳 C、二氧化氮 D、一氧化碳
-
18、如图是实验室制备、收集、验满、验证性质的操作,其中不正确的是A、
 B、
B、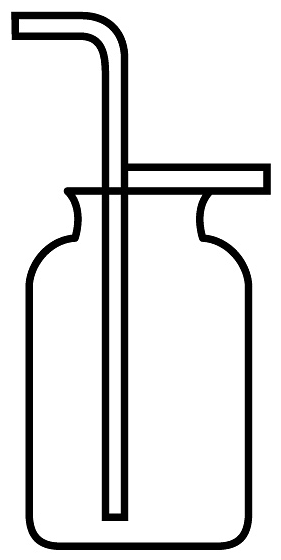 C、
C、 D、
D、
-
19、为测定某稀硫酸中溶质的质量分数,向盛有该稀硫酸的烧杯中,分三次加入一定质量的锌粉,生成气体的质量与加入锌粉质量的关系如图所示。请计算:
 (1)、m的值为。(2)、该稀硫酸中溶质的质量分数。
(1)、m的值为。(2)、该稀硫酸中溶质的质量分数。 -
20、
某化学兴趣小组在进行用过氧化氢制取氧气的实验时,误将失去标签的氧化铜当作二氧化锰使用,结果发现加入氧化铜后,过氧化氢溶液迅速出现了气泡。小组同学对氧化铜在过氧化氢溶液中的作用及效果进行了实验探究。
[查阅资料]氧化铜(CuO)为黑色固体,不溶于水。
[提出问题]氧化铜在过氧化氢溶液分解过程中是否具有催化作用,其效果是否比二氧化锰更好?
[设计实验]以生成等体积的氧气为标准,设计了下列三组实验(其他可能影响实验的因素均忽略)。
实验序号
过氧化氢溶液质量/g
其他物质质量/g
待测数据
①
10
0
a
②
10
氧化铜0.3
b
③
10
二氧化锰0.3
c
(1)上述实验应测量的“待测数据”是收集等体积氧气所需的。对比实验①、②,若ab(填“>”或“<”),说明氧化铜能加快过氧化氢的分解速率。(2)从实验②反应后的剩余物通过过滤、洗涤、干燥的方法分离出氧化铜,若称得其质量为0.3g,说明氧化铜的在化学反应前后保持不变。[实验结论]
(3)小明同学根据上述实验得出结论:氧化铜是过氧化氢溶液分解的催化剂,小娅同学认为该说法不合理,还需补充一个实验,请你帮助小娅设计实验方案(写出实验步骤,现象及结论) , 实验②反应的文字表达式为。(4)设计实验②和③是为了比较。