相关试卷
- 湖南省长沙市2016-2017学年九年级化学一模考试试卷
- 广东省东莞市中堂星晨学校2016-2017学年九年级化学一模考试试卷
- 广东省茂名高州市东岸中学2016-2017学年九年级化学一模考试试卷
- 广东省广州市花都区2016-2017学年九年级化学一模考试试卷
- 广西柳州市柳南区2014-2015学年九年级化学一模考试试卷
- 北京市西城区2017—2018学年九年级上学期化学期末考试试卷
- 北京市海淀区2017-2018学年九年级上学期化学期末考试试卷
- 北京市朝阳区2017-2018学年九年级上学期化学期末考试试卷
- 北京市丰台2017-2018学年九年级上学期化学期末考试试卷
- 广东省深圳市罗湖区2017-2018学年九年级上学期化学期末考试试卷
-
1、千金藤素的化学式为C37H38N2O6 , 下列关于千金藤素的说法正确的是A、千金藤素由83个原子构成 B、分子中含1个N2分子 C、千金藤素属于氧化物 D、由碳、氢、氮、氧四种元素组成
-
2、水是生命之源。城市生活用水经自来水厂净化处理的过程如图。下列说法错误的是
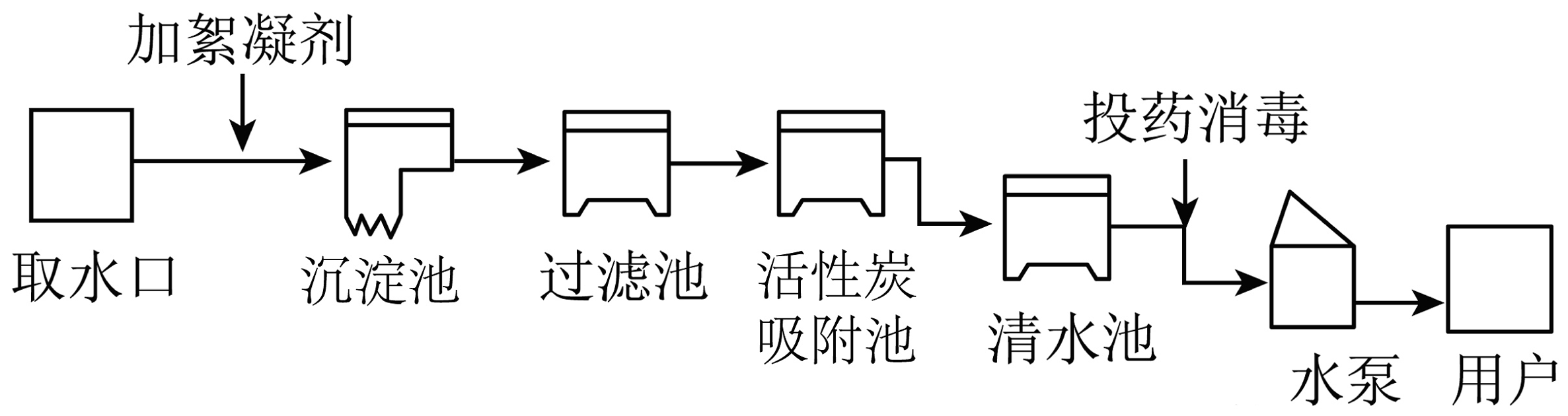 A、通过沉淀池、过滤池除去水中不溶性杂质 B、活性炭吸附池内常用来吸附色素和异味 C、自来水厂投入明矾进行消毒 D、投药消毒过程包含化学变化
A、通过沉淀池、过滤池除去水中不溶性杂质 B、活性炭吸附池内常用来吸附色素和异味 C、自来水厂投入明矾进行消毒 D、投药消毒过程包含化学变化 -
3、下列化学用语中,既能表示一种物质,还能表示一种元素的是A、 B、H C、 D、
-
4、如图为四种气体的微观示意图,图中“
 ”“
”“ ”分别表示两种不同的原子,下列表示单质的是 A、
”分别表示两种不同的原子,下列表示单质的是 A、 B、
B、 C、
C、 D、
D、
-
5、下列对实验指定容器中的水的解释没有体现水的主要作用的是
选项
A
B
C
D
实验装置




解释
吸收放出的热量
通过量筒中水体积的变化得出空气中氧气的体积
冷却溅落的高温熔融物,防止集气瓶炸裂
排净集气瓶内的空气,便于氧气收集
A、A B、B C、C D、D -
6、空气是我们熟悉的气体。下列关于空气及其成分的说法正确的是A、空气中氮气的质量分数约为78% B、氧气能支持燃烧,可以作燃料 C、稀有气体用于制造霓虹灯,利用了其物理性质 D、常见的空气污染物有氮气、二氧化硫、二氧化氮等
-
7、空气质量关系到人们的生活品质和身体健康,《室内空气质量标准》自2023年2月1日起实施。下列做法不利于保护空气的是A、大力发展植树造林 B、在田野里焚烧秸秆 C、使用清洁能源 D、提倡绿色出行
-
8、
某同学设计了如图所示的实验装置,探究“分子的基本性质”,请回答下列问题:

【查阅资料】碱性溶液能使酚酞试液变红,而氨水呈碱性。
【实验方案一】如图Ⅰ。
(1)①观察到的实验现象是;
②该方案的不足之处是(任写一点)。
【实验改进】老师对图Ⅰ所示的装置进行了改进(如图Ⅱ所示),并进行了以下操作:
①取一条滤纸,在滤纸条上等距离滴加无色酚酞试液;
②将滴加了无色酚酞试液的滤纸条放入一洁净的试管中,并在试管口塞一团脱脂棉;
③在脱脂棉上滴加几滴浓氨水。
【分析讨论】
(2)实验过程中若发现滤纸条没有变红而脱脂棉变红,导致这种现象产生的错误操作可能是:。
【拓展延伸】同学们经过讨论后认为,图Ⅰ、图Ⅱ所示装置虽能证明分子的基本性质,但不能证明影响分子基本性质的因素,于是又设计了如图Ⅲ所示的装置。
【实验改进】
(3)在A、D两试管中分别加入等量的少许浓氨水,B、C两试管中加入等量的少许无色酚酞溶液,立即用带导管的橡皮塞按图Ⅲ连接好,并将D试管放置在盛有热水的烧杯中,观察。分析讨论:按照图Ⅲ所示的装置进行操作,观察到的现象是 , 该现象得出的结论是。
【实验反思】
(4)在图Ⅰ、图Ⅱ的实验中均闻到了刺激性气味的气体,因此实验室应保存氨水。
-
9、元素周期表是学习和研究化学的重要工具。请回答下列问题:(1)、元素周期表中不同元素间最本质的区别是________(填字母)。A、质子数不同 B、中子数不同 C、相对原子质量不同(2)、下图图1是元素周期表的部分内容,图2是这三种元素的原子结构示意图。

①硒元素的相对原子质量为 , 它属于(填“金属”,或“非金属”)元素。
②图2中硫原子的结构示意图是(填字母)。
③氧、硫、硒三种元素化学性质相似的原因是。
④画出的结构示意图是。
-
10、“见著知微,见微知著”是化学思维方法。根据下列粒子的结构示意图回答问题。
 (1)、上图A—F六种粒子共有种元素。(2)、与D化学性质相似的原子是(填字母)。(3)、若G粒子是带三个单位正电荷的微粒,G粒子的化学符号为。若G粒子是带两个单位负电荷的微粒,G粒子的化学符号为。
(1)、上图A—F六种粒子共有种元素。(2)、与D化学性质相似的原子是(填字母)。(3)、若G粒子是带三个单位正电荷的微粒,G粒子的化学符号为。若G粒子是带两个单位负电荷的微粒,G粒子的化学符号为。 -
11、北斗卫星导航系统是我国自行研制的全球卫星导航系统,如原子钟被称为北斗卫星的“心脏”,用来计算时间,铷元素在周期表中的信息如图所示。
 (1)、从元素分类角度,铷元素属于(填“金属”或“非金属”) 元素。(2)、铷元素的原子序数是。(3)、铷元素的相对原子质量为。
(1)、从元素分类角度,铷元素属于(填“金属”或“非金属”) 元素。(2)、铷元素的原子序数是。(3)、铷元素的相对原子质量为。 -
12、A~F 是我们学过的常见物质。A、D是无色液体,B是黑色固体,F是无色刺激性气味气体。它们之间有如图所示转化关系:
 (1)、物质D的名称为:。(2)、反应①的符号表达式 , 反应②的符号表达式。(3)、B在反应①中起作用,在反应前后不变。(4)、反应①的基本反应类型为 , 反应②的基本反应类型为。
(1)、物质D的名称为:。(2)、反应①的符号表达式 , 反应②的符号表达式。(3)、B在反应①中起作用,在反应前后不变。(4)、反应①的基本反应类型为 , 反应②的基本反应类型为。 -
13、实验室制取氧气中,可供选择的实验装置如图所示。
 (1)、写出仪器的名称:①;②。(2)、若用高锰酸钾氧气,发生装置可选用装置。反应的化学符号表达式为。若用B装置来制取氧气,反应的符号表达式为(3)、若用B或C装置制取氧气,B装置的优点是 , C装置的优点是。;若用图G装置收集氧气,则气体应从(填“a”或“b”)口进入。(4)、实验室选择AD装置制取氧气,收集完氧气后,应进行的操作是先 , 再。(5)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体,已知甲烷难溶于水,比空气的密度小,制备甲烷选择(填字母)发生装置,要收集甲烷气体,可以用装置(填字母)。
(1)、写出仪器的名称:①;②。(2)、若用高锰酸钾氧气,发生装置可选用装置。反应的化学符号表达式为。若用B装置来制取氧气,反应的符号表达式为(3)、若用B或C装置制取氧气,B装置的优点是 , C装置的优点是。;若用图G装置收集氧气,则气体应从(填“a”或“b”)口进入。(4)、实验室选择AD装置制取氧气,收集完氧气后,应进行的操作是先 , 再。(5)、实验室常用加热无水醋酸钠和碱石灰固体的方法制取甲烷气体,已知甲烷难溶于水,比空气的密度小,制备甲烷选择(填字母)发生装置,要收集甲烷气体,可以用装置(填字母)。 -
14、
已知空气的主要成分是氮气和氧气,某课外活动小组设计测定空气中氧气含量的实验,实验装置如图所示:

(1)红磷在集气瓶中发生反应的文字表达式为。该实验中红磷稍过量,目的是。
(2)待燃烧停止,并冷却至后,打开止水夹,观察到烧杯中的水进入集气瓶,瓶内水量约是集气瓶体积的 , 由本实验还可以推知氮气的哪些物理性质?。
(3)某学生用上述实验装置测定的结果是:空气中氧气含量与正常值有较明显的偏小,其原因可能是(只要求答出一种)。
(创新实验)
(4)如图是小东设计的探究空气中氧气含量的装置。与课本实验相比,该实验的一个优点是。活塞最终停留在刻度附近。

-
15、根据下图提供的信息,下列说法不正确的是
 A、钠的原子序数为11 B、钠原子核外有11个电子 C、钠的相对原子质量是 D、钠属于金属元素
A、钠的原子序数为11 B、钠原子核外有11个电子 C、钠的相对原子质量是 D、钠属于金属元素 -
16、拉瓦锡用定量的方法研究了空气的成分。在密闭装置中,某兴趣小组利用凸透镜聚光来引燃白磷,再借助氧气传感器来检测足量白磷燃烧过程中氧气的含量,如图所示。下列判断正确的是
 A、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 B、将白磷换成木炭可得到同样的实验结论 C、观察到的现象是白磷燃烧,产生大量白色烟雾 D、a点时容器内氮气体积分数为85%
A、氧气有剩余,说明物质燃烧时氧气必须达到一定浓度 B、将白磷换成木炭可得到同样的实验结论 C、观察到的现象是白磷燃烧,产生大量白色烟雾 D、a点时容器内氮气体积分数为85% -
17、下列有关空气的说法不正确的是A、通常状况下,无色、无味的气体一定是空气 B、饼干在空气中变软是因为空气中含有水蒸气 C、稀有气体通电时能发出不同颜色的光,可制作航标灯 D、空气质量级别为Ⅲ级时,属于轻微或轻度污染
-
18、生活中的加铁酱油的中的“铁”指的是A、原子 B、分子 C、单质 D、元素
-
19、下列变化中,属于化学变化的是A、水挥发 B、鸡蛋变臭 C、轮胎爆炸 D、干冰升华
-
20、
“Zn有灵犀”化学兴趣小组同学无意中发现过氧化氢溶液和“84”消毒液以及氧化铜混合后均产生了大量气泡,有同学对此产生了疑惑——“84”消毒液能否作过氧化氢分解的催化剂呢?催化过氧化氢分解除了二氧化锰外是否有更好的催化剂呢?同学们在老师的指导下对这两个问题展开了探究。
【资料】①“84”消毒液的有效成分是次氯酸钠。
②“84”消毒液和过氧化氢溶液混合能产生氧气。
③氧化铜是过氧化氢分解的催化剂。
探究一:探究次氯酸钠能否作过氧化氢分解的催化剂。
【设计实验】同学们设计了如图所示实验装置进行探究。(实验前导气管中已充满了水)

【进行实验】
(1)步骤Ⅰ:连接好装置,并________(填操作)。
步骤Ⅱ:向锥形瓶中加入30mL“84”消毒液,然后用注射器吸取25mL过氧化氢溶液,塞紧橡胶塞;
步骤Ⅲ:将注射器中的过氧化氢溶液平均分5次(每次5mL)推入锥形瓶中;每次推入过氧化氢溶液,待不再产生气泡后,读出量筒中水的总体积如表所示。
第1次
第2次
第3次
第4次
第5次
量筒中水的总体积/mL
140
280
365
370
x
【讨论与分析】
(2)下列有关该实验的数据分析中,正确的是______。
A. 第1次实验产生的气体为140mL B. 前两次实验产生气体的总体积为270mL C. 表格中x的值是370 D. 第4、5次加入液体后几乎没有气体产生 (3)小组同学根据表中数据分析得出结论:在次氯酸钠中加入过氧化氢,次氯酸钠作________(填“反应物”或“催化剂”)。
探究二:氧化铜与二氧化锰的催化效果比较。
图1所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的等体积、等浓度的过氧化氢溶液快速注入试管中,利用注射器收集氧气,收集到氧气的体积和时间的关系如图2所示。

(4)开始实验时要快速注入过氧化氢溶液的原因可能是________。
(5)实验中造成U型管内红墨水液面左低右高的可能原因是________。
(6)通过图2除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是________。
(7)请写出氧化铜催化过氧化氢溶液分解制氧气的符号表达式________。