-
1、槲皮素(C15H10O7)具有抗氧化作用,有助于预防多种慢性疾病。下列有关其说法正确的是A、由碳原子、氢原子和氧原子构成 B、氧元素的质量分数最大 C、含有5个氢分子 D、碳、氢原子的个数比为3∶2
-
2、手机快充电源适配器中含有的氮化镓可以提高充电的效率。镓元素在元素周期表中的信息如图所示,下列说法错误的是
 A、镓原子核内有31个质子 B、镓的原子质量是69.72 C、镓属于金属元素 D、镓的元素符号为Ga
A、镓原子核内有31个质子 B、镓的原子质量是69.72 C、镓属于金属元素 D、镓的元素符号为Ga -
3、化学用语是学习化学的重要工具。下列化学用语表示正确的是A、两个氢分子:2H B、三个氮原子:3N C、镁离子:Mg+2 D、氦气:He2
-
4、《化学鉴原》中许多元素的中文名称沿用至今,参与这部著作合译的是我国近代化学家A、张青莲 B、闵恩泽 C、徐寿 D、侯德榜
-
5、硫酸钙(CaSO4)能使豆浆形成凝胶状的豆腐。硫酸钙属于A、氧化物 B、酸 C、碱 D、盐
-
6、高钙片是一种人体补钙药,其有效成分是碳酸钙,工业上从石灰石(主要成分为CaCO3)获得高纯度CaCO3的流程如图:
查阅资料:石灰石高温煅烧,它的主要成分碳酸钙就会生成生石灰(主要成分:氧化钙)和二氧化碳,其中所含的杂质不会反应。
 (1)、上述生产过程中石灰石高温煅烧的化学方程式是 , 该反应的基本类型是反应,石灰石的主要成分碳酸钙中钙、氧元素质量比为。(2)、试剂①是一种常见的氧化物,是人类的生命之源。固体A与试剂①发生化合反应生成Ca(OH)2 , 请写出该反应的化学方程是。(3)、试剂②的名称是;气体B的用途是(写出一种即可)。(4)、使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一。上述流程中有的物质可以再利用,流程图上还可循环利用的物质是、(填化学式)。
(1)、上述生产过程中石灰石高温煅烧的化学方程式是 , 该反应的基本类型是反应,石灰石的主要成分碳酸钙中钙、氧元素质量比为。(2)、试剂①是一种常见的氧化物,是人类的生命之源。固体A与试剂①发生化合反应生成Ca(OH)2 , 请写出该反应的化学方程是。(3)、试剂②的名称是;气体B的用途是(写出一种即可)。(4)、使原料中各原子的利用率尽可能达到100%是“绿色化学”的核心理念之一。上述流程中有的物质可以再利用,流程图上还可循环利用的物质是、(填化学式)。 -
7、
水是生命之源,可中实践小组学生在老师的指导下开展了有关“水的净化”的项目式学习活动。
【活动一】了解水的净化
波波同学参加东江环保实践活动,取一瓶东江水带回实验室,在老师的指导下,按下列流程进行实验,制取蒸馏水。请回答下列问题:

(1)取水后加入明矾的作用是________。
(2)进行过滤时,下列做法错误的是_________。
A. 玻璃棒要靠在三层滤纸的一边 B. 漏斗下端口不能接触烧杯的内壁 C. 滤纸的边缘要低于漏斗口 D. 液面不要低于滤纸边缘 (3)向滤液中加入活性炭,利用其________性,除去水样中的色素和异味。
(4)消毒剂高铁酸钠(Na2FeO4)集氧化、吸附、凝聚、杀菌等功能于一体,目前被广泛应用于自来水净化,高铁酸钠中铁元素的化合价为________。
(5)在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是________。
【活动二】了解航天员在太空中氧气和水的相互转化
航天员在太空生活需要氧气和水。氧气和水的相互转化,体现了“合”与“分”的思想。
“合”的思想
液氢和液氧反应产生的能量可为返回舱返回提供动力,实验室进行氢气燃烧的实验如图1所示,该反应的微观示意图如图2所示:

(6)点燃纯净的氢气,可观察到的现象是产生________色火焰。
“分”的思想
(7)航天员在空间站生活所需氧气主要通过电解水获得,该反应的文字或符号表达式是________。
(8)如图3是电解水的实验装置,其中负极产物为 ________。

(9)“合”与“分”的思想通过以上事实,证明了水是由 ________组成。
-
8、
I.实验室制取氧气与二氧化碳的性质。
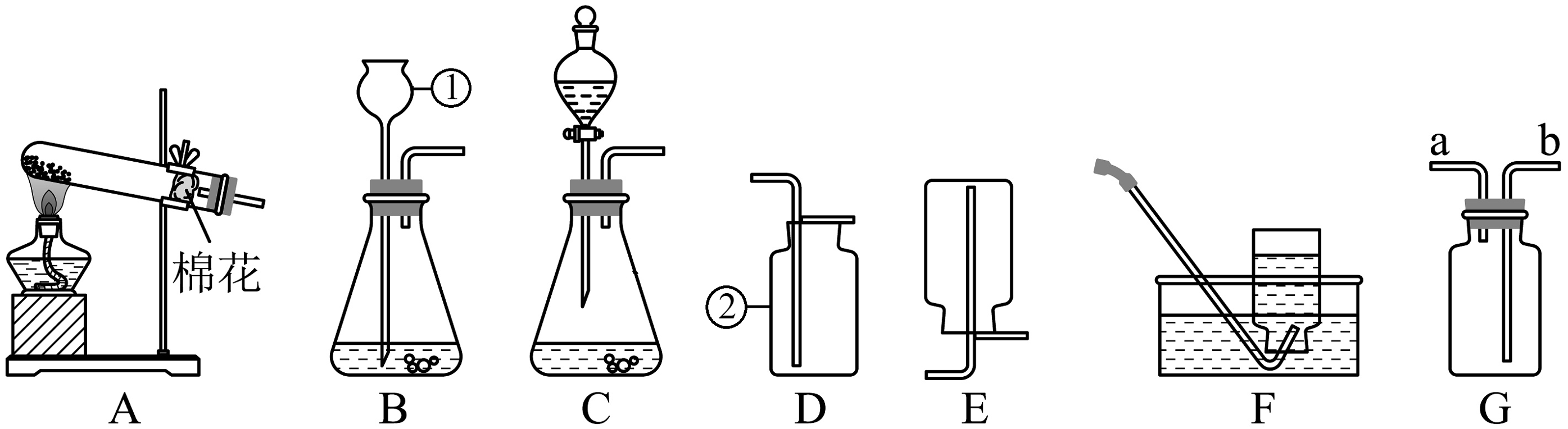
(1)写出装置中标号的仪器名称:①________,②________。
(2)装置A可用于高锰酸钾制取氧气反应的化学方程式是________,选用装置A作为发生装置的依据是________。
(3)若用过氧化氢溶液制取氧气,为了控制反应的速率,则应选择的发生装置为________(填序号)。
(4)G是一种可用于集气、洗气等的多功能装置。氢气是一种密度比空气小、难溶于水且与水不反应的气体,若用G装置收集氢气,氢气应从________(填“a”或“b”)进入G中;若将G装置内装满水,再连接量筒,就可以用于测定氢气的体积,则量筒与G装置________(填“a”或“b”)连接。
II.自制简易制氧机

(5)原料选择,用过氧化氢溶液比高锰酸钾更合适的原因是________(写一条)。
(6)组装仪器:化学小组利用塑料瓶、注射器、吸管输液管等设计并制作如图简易制氧机。下列说法错误的是_______(填序号)。
A. 甲瓶是气体发生装置 B. 试剂B只能是二氧化锰 C. 注射器可以控制滴加液体的速率 D. 乙瓶可以使氧气湿润 -
9、广袤的自然界是一个碳的世界,以下是四种碳单质的微观结构。
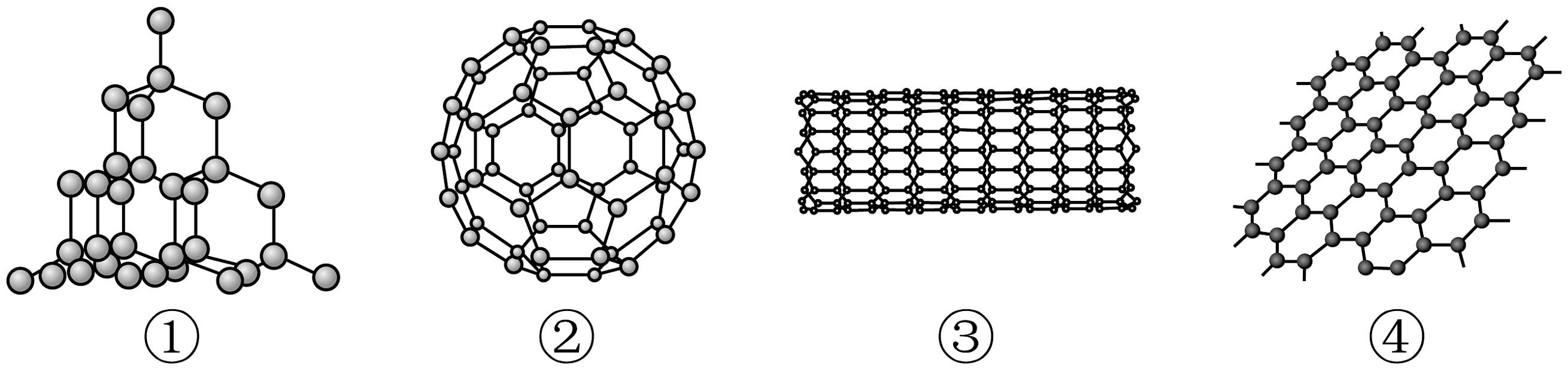 (1)、四种碳单质的物理性质存在较大差异的原因是。(2)、碳化硅(SiC)的结构与①金刚石类似,则下列推测合理的是______(填序号)。A、碳化硅的结构形似足球 B、碳化硅能导电,可作电极 C、碳化硅硬度大,可作砂轮切割石料(3)、物质②为C60 , C60由(填“原子”或“分子”或“离子”)构成,C60不充分燃烧的产物是。(4)、科学家发现可将③碳纳米管打开制备④石墨烯,该过程属于(填“物理”或“化学”)。
(1)、四种碳单质的物理性质存在较大差异的原因是。(2)、碳化硅(SiC)的结构与①金刚石类似,则下列推测合理的是______(填序号)。A、碳化硅的结构形似足球 B、碳化硅能导电,可作电极 C、碳化硅硬度大,可作砂轮切割石料(3)、物质②为C60 , C60由(填“原子”或“分子”或“离子”)构成,C60不充分燃烧的产物是。(4)、科学家发现可将③碳纳米管打开制备④石墨烯,该过程属于(填“物理”或“化学”)。变化。将酞菁-钴酞菁-三氯化铝复合嵌接在碳纳米管上,制得一种高效催化剂,其反应之一的微观过程如图:(注:
 表示CH4)
表示CH4)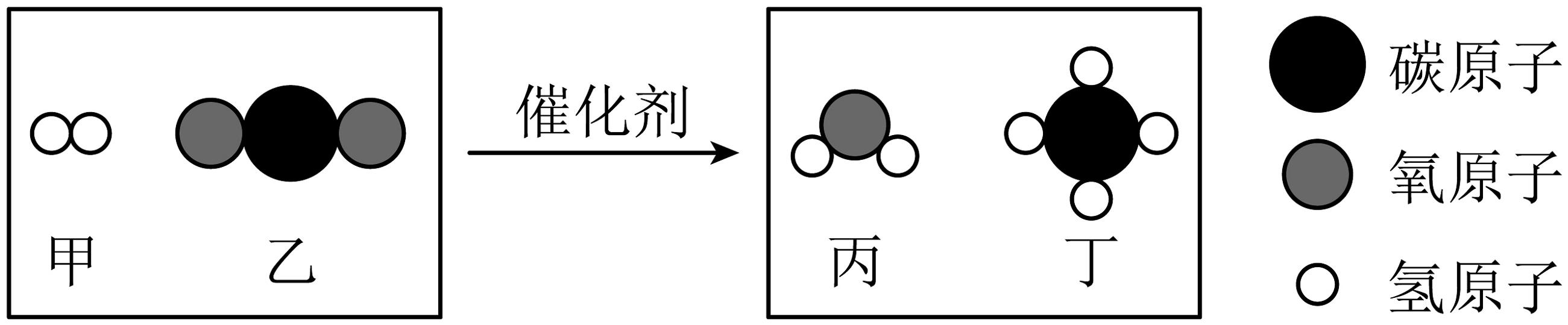
①参加反应的甲、乙两种分子的个数比为。
②写出该反应的化学方程式。
-
10、2024年5月3日,嫦娥六号探测器成功发射,开启月球背面采样之旅。(1)、月球背面的水有固态和气态两种存在方式。
①气态水的分子间隔比固态水更(填“大”或“小”)。
②水由固态变为气态的过程中,没有发生变化的是(填“物理”或“化学”)性质。
(2)、科研人员曾用嫦娥五号带回的月壤证实:在一定条件下,月壤中的FeO(铁橄榄石的主要成分)分解生成Fe3O4(磁铁矿的主要成分)以及单质铁。①写出该反应的化学方程式。
②下列关于含铁物质的说法中,正确的是 (填序号)。
A.磁铁矿是工业炼铁的重要原料
B.铁锈的主要成分是
C.铁合金比纯铁应用更为广泛
-
11、下列实验设计不能达到实验目的的是
实验设计
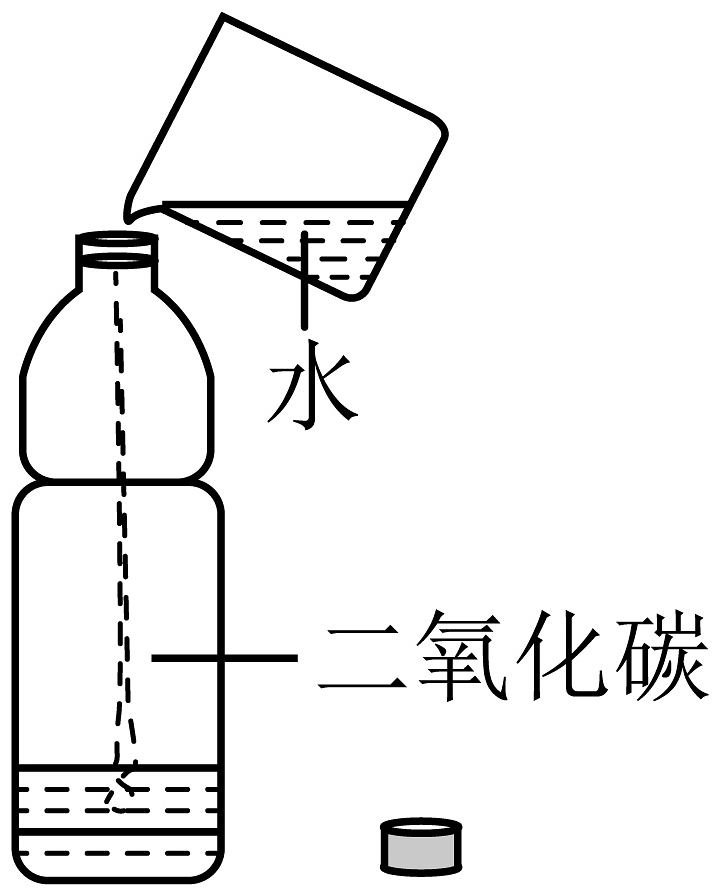
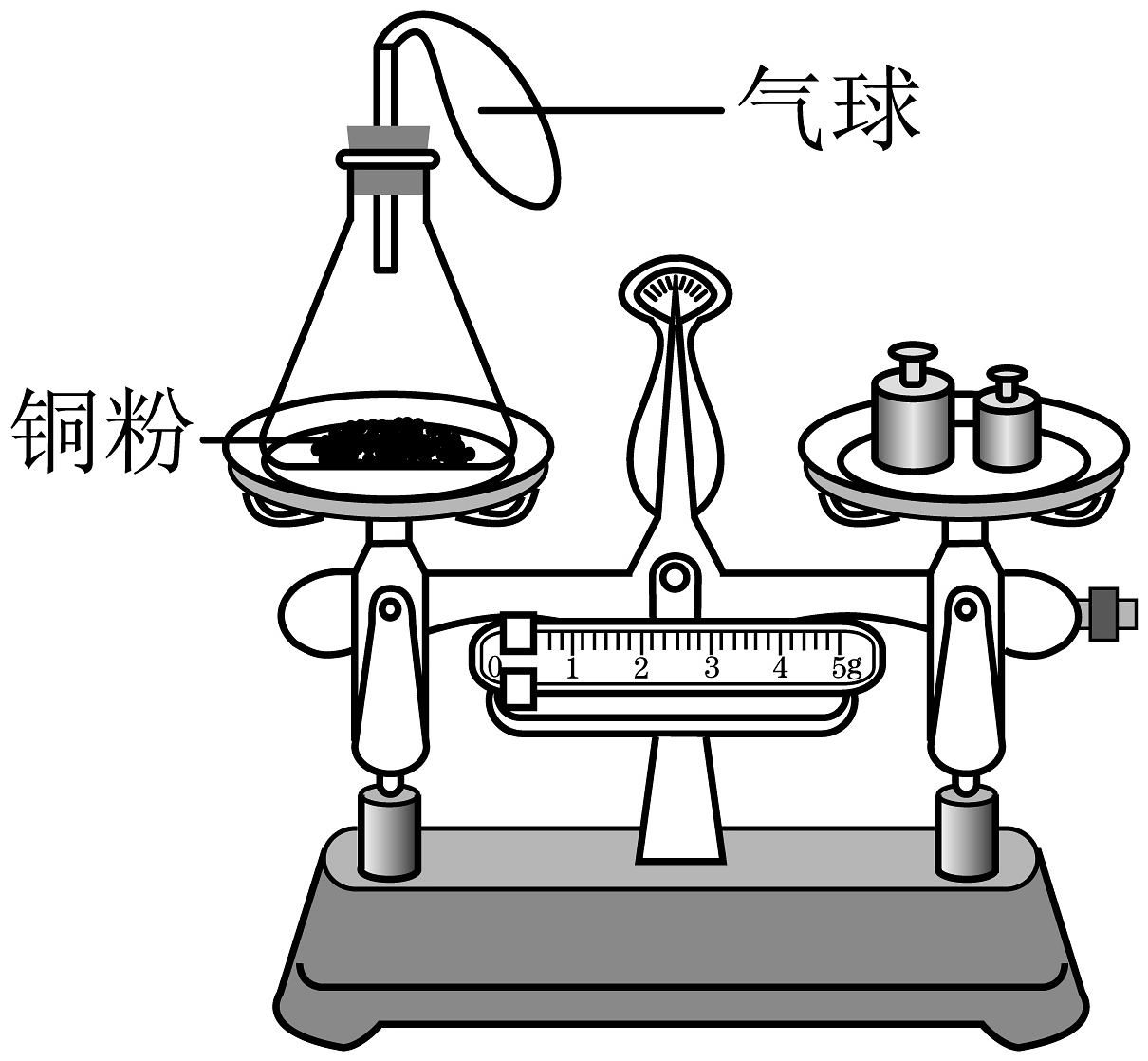

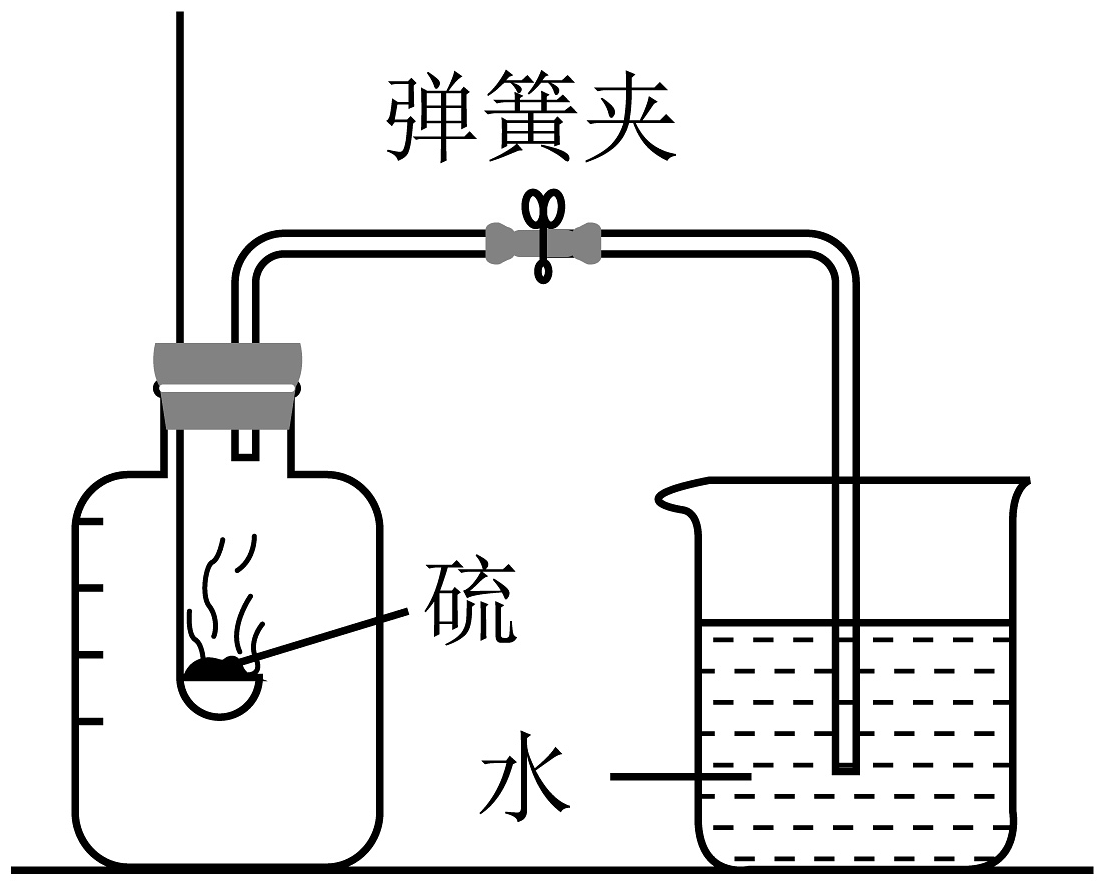
实验目的
A.探究CO2是否溶于水
B.验证质量守恒定律
C.检验氢气的纯度
D.测定空气中氧气的含量
A、A B、B C、C D、D -
12、钉在元素周期表中的相关信息如图所示。下列说法正确的是
 A、钌属于非金属元素 B、钌的相对原子质量为101.1g C、钌原子的核外电子数为44 D、二氧化钌的化学式为O2Ru
A、钌属于非金属元素 B、钌的相对原子质量为101.1g C、钌原子的核外电子数为44 D、二氧化钌的化学式为O2Ru -
13、化学核心素养展现了化学课程对学生发展的重要价值,下列说法错误的是
A
化学观念
和的分子构成不同,所以化学性质存在明显差异
B
科学思维
水、干冰、澄清石灰水都属于氧化物
C
科学探究与实践
在燃着的蜡烛上方罩一个干燥的烧杯,探究燃烧产物是否有水
D
科学态度与责任
实验后的废液集中回收处理,符合绿色化学理念
A、A B、B C、C D、D -
14、交警检测司机是否酒后驾车用的检测仪里装有重铬酸钾(K2Cr2O7) ,K2Cr2O7中 Cr元素的化合价为A、-2 B、+1 C、+6 D、+7
-
15、下图所示实验操作不正确的是A、
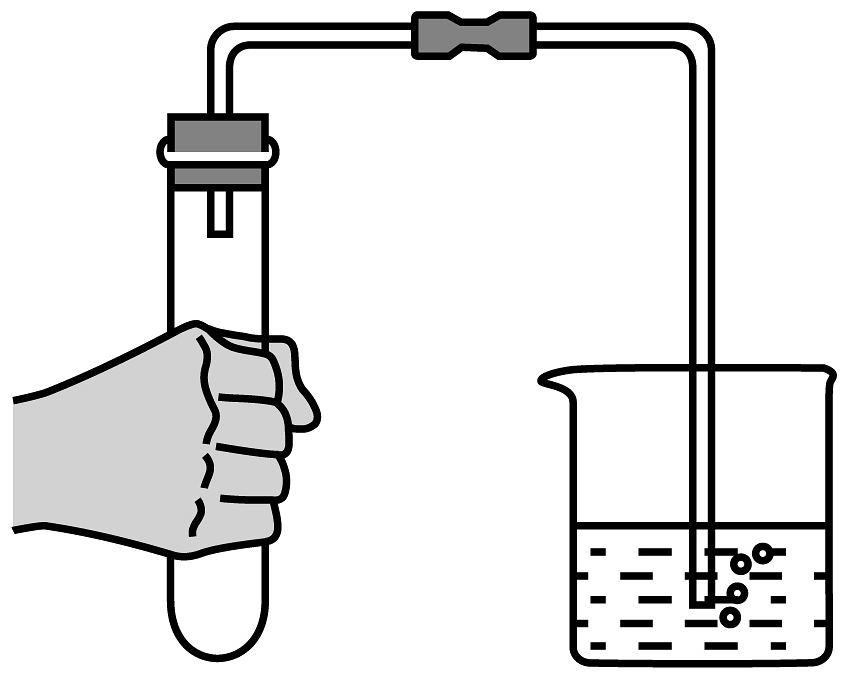 检查气密性
B、
检查气密性
B、 点燃酒精灯
C、
点燃酒精灯
C、 滴加液体
D、
滴加液体
D、 取液体药品
取液体药品
-
16、贫血的人可以多吃菠菜,每100g菠菜中含铁2.9mg。这里的“铁”是指A、铁原子 B、铁元素 C、铁单质 D、铁离子
-
17、新情境 我国历史悠久,有丰富的历史文化遗产。下列文物所用的材料属于金属材料的是A、西汉素纱襌衣 B、三星堆青铜面具 C、唐三彩陶器 D、名画《关山密雪图》
-
18、下列标识中,一般张贴在洗手台上的是A、
 B、
B、 C、
C、 D、
D、
-
19、我国航天事业发展迅猛。若你是航天科技人员,请试着解决空间站二氧化碳和水再利用的问题。(1)、空间站里的二氧化碳主要产生于人的呼吸,请补充完成下列产生的化学方程式:。(2)、空间站中科学家采用水气整合系统实现的清除和的再生,流程如下图所示。

反应器1发生的反应:;反应器2发生的反应:。若消耗0.22吨二氧化碳,则会产生的质量是多少吨?(请写出解题过程)
(3)、此流程中的反应(填“能”或“不能”)完全实现水的循环,理由是。 -
20、某学习小组利用锈蚀严重的废铜屑为原料回收铜,铜锈的主要成分是碱式碳酸铜,其化学式为。分别采用题图的两种方案。请回答下列问题:
资料1:
资料2:回收铜的两种实验方案。
 (1)、方案一中黑色固体C的名称为 , 步骤II是利用了CO的性(填“氧化”或“还原”),生成的二氧化碳不直接排放到空气中,需要将其回收后再与碳粉在高温下反应,又可以生成CO,写出该反应的化学反应方程式。(2)、方案二中步骤Ⅲ、Ⅳ、Ⅴ都涉及到的操作名称是 , 该操作中使用玻璃棒的作用是。(3)、方案二中步骤Ⅳ加入过量铁粉的主要目的是 , 步骤Ⅳ中生成铜的反应方程式为 , 该反应的基本反应类型是。
(1)、方案一中黑色固体C的名称为 , 步骤II是利用了CO的性(填“氧化”或“还原”),生成的二氧化碳不直接排放到空气中,需要将其回收后再与碳粉在高温下反应,又可以生成CO,写出该反应的化学反应方程式。(2)、方案二中步骤Ⅲ、Ⅳ、Ⅴ都涉及到的操作名称是 , 该操作中使用玻璃棒的作用是。(3)、方案二中步骤Ⅳ加入过量铁粉的主要目的是 , 步骤Ⅳ中生成铜的反应方程式为 , 该反应的基本反应类型是。