版本:
相关试卷
- (浙教版)科学 七年级下册 第五章 制造技术与工程 单元卷(提高)
- (浙教版)科学 七年级下册 第五章 制造技术与工程 单元卷(基础)
- (浙教版)科学 八年级下册 第五章 控制系统与工程 单元卷(提高)
- (浙教版)科学 八年级下册 第五章 控制系统与工程 单元卷(基础)
- 浙江省金华市新东方双语学校2025-2026学年第二学期八年级期中检测·科学试题卷
- 浙江省温州市绣山中学2025-2026学年第二学期八年级期中检测 科学试卷( 1-2章)
- 浙江省浙共体2025-2026学年下学期七年级科学学科期中学能诊断卷(1-2章)
- 浙江省宁波市北仑区四校联考2025-2026学年第二学期八年级期中试卷 科学卷
- 浙江省金华市义乌市丹溪中学2025-2026学年第二学期九年级期中测试 科学试题卷
- 浙江省海山教育联盟2025-2026学年第二学期八年级期中评估 科学试题卷
-
1、氢氧化钠是实验室一种常见的碱,在研究氢氧化钠性质实验中的部分实验及现象记录如下,其中现象不合理的选项是( )
选项
实 验
现 象
A
将 NaOH固体放在表面皿上,放置一会儿
固体受潮,逐渐溶解
B
向盛有NaOH 溶液的试管中滴入无色酚酞试液
溶液变红
C
向盛有 NaOH 溶液的试管中滴加稀HCl
有NaCl生成
D
向盛有NaOH溶液的试管中滴加 CuSO4溶液
产生蓝色(絮状)沉淀
A、A B、B C、C D、D -
2、下列选项中,物质的俗称,化学式和物质类别不一致的是( )A、水银———— Hg————单质 B、生石灰——CaO——氧化物 C、消石灰———— Ca(OH):————碱 D、小苏打————Na2CO3————盐
-
3、规范操作是科学实验成功的关键。下列实验操作规范的是( )A、溶解物质
 B、测液体 pH
B、测液体 pH C、取化学药品
C、取化学药品 D、稀释浓硫酸
D、稀释浓硫酸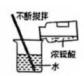
-
4、小柯想测定实验室制二氧化碳的石灰石中碳酸钙的质量分数,采用了如下方法:称取该石灰石样品20g,把100g稀盐酸分五次加入,测量过程所得数据见下表(已知石灰石样品中的杂质不溶于水,不与稀盐酸反应)。请计算:
序号
1
2
3
4
5
加入稀盐酸的质量/g
20
20
20
20
20
剩余固体的质量/g
15
a
5
2.8
2.8
(1)、上表中a的数值为。(2)、样品中碳酸钙的质量分数。(3)、第3次实验结束时所得溶液溶质质量分数。(计算结果精确到0.1%) -
5、航母舰体需要定期除锈维护,为实现对除锈废液(溶质主要成分为HCl、FeCl3 , 其他杂质忽略)的综合利用,需测定废液中HCl的质量分数。取200g废液样品,依次加入100g溶质质量分数相同的NaOH 溶液,过滤,称重,相关数据如图。回答下列问题。
 (1)、第③次过滤后,滤液中溶质的成分为 (用化学式表示)。(2)、所用NaOH 溶液溶质的质量分数(写出计算过程)。(3)、废液样品中 HCl的质量。
(1)、第③次过滤后,滤液中溶质的成分为 (用化学式表示)。(2)、所用NaOH 溶液溶质的质量分数(写出计算过程)。(3)、废液样品中 HCl的质量。 -
6、已知某测电笔内部电阻为5×105欧,人体电阻为4000欧。如图所示家庭照明电路中,闭合开关S,电灯L发光。
 (1)、此时人拿到测电笔测试A 点时,测电笔的氖管(填“发”或“不发”)光。(2)、如此时将零线保险盒盖拔掉(断路),人拿测电笔测试A点时(A点在灯泡右边),测电笔的氖管(填“发”或“不发”)光。通过他的电流是毫安?(写出计算过程)
(1)、此时人拿到测电笔测试A 点时,测电笔的氖管(填“发”或“不发”)光。(2)、如此时将零线保险盒盖拔掉(断路),人拿测电笔测试A点时(A点在灯泡右边),测电笔的氖管(填“发”或“不发”)光。通过他的电流是毫安?(写出计算过程) -
7、小强利用压力传感器、电磁继电器、阻值可调的电阻R等元件,设计了一个汽车超载自动报警电路,如图甲所示。他了解到这种压力传感器所受压力越大时,输出的电压U就越大,二者的关系如图乙所示。闭合开关S,当继电器线圈中电流大于或等于20mA时,衔铁被吸合。已知传感器的输出电压U即为继电器控制电路的电源电压,线圈的电阻为20Ω。
 (1)、车辆不超载时,工作电路中绿灯亮;当传感器所受压力增大到一定程度时,红灯亮,说明汽车超载。请你判断灯(选填“L1”或“L2”)是红灯。(2)、某水平公路桥禁止质量大于或等于20t的车辆通行,要用小强设计的装置为此桥报警,R的阻值应调节为多少?(3分)(g取10N/kg)(3)、若要减小公路桥禁止通行车辆的质量,应(选填“增大”或“减小”)电阻R 的阻值。
(1)、车辆不超载时,工作电路中绿灯亮;当传感器所受压力增大到一定程度时,红灯亮,说明汽车超载。请你判断灯(选填“L1”或“L2”)是红灯。(2)、某水平公路桥禁止质量大于或等于20t的车辆通行,要用小强设计的装置为此桥报警,R的阻值应调节为多少?(3分)(g取10N/kg)(3)、若要减小公路桥禁止通行车辆的质量,应(选填“增大”或“减小”)电阻R 的阻值。 -
8、某化学实验小组在实验室将68.1g的二氧化锰和过氧化氢溶液的混合物放入锥形瓶中制备氧气,充分反应后,锥形瓶中剩余物的总质量为66.5g。求:(1)、制得氧气的质量为 g。(2)、计算参加反应的过氧化氢的质量是多少?
-
9、2011年我国女科学家屠呦呦发现青蒿素(青蒿素的化学式: 它是一种用于治疗疟疾的药物,获美国拉斯克奖。(1)、青蒿素分子由种原子构成的。(2)、一个青蒿素分子含有个原子。(3)、青蒿素中C、H、O三种元素的质量比为。
-
10、某兴趣小组利用如图装置进行了“可燃物燃烧的条件”的探究实验。

①将所需仪器按照装置图连接起来;
②打开K1和K2 , 向上拉动任意一支注射器的活塞;
③将实验所需药品加入对应的仪器;
④将装有适量白磷的具支试管放入冷水中;
⑤打开K1 , 关闭K2 , 往装置甲中加入适量的双氧水,氧气进入具支试管中;
⑥关闭K1 , 打开K2 , 往装置乙中加入适量的盐酸,二氧化碳进入具支试管中;
⑦将装有适量白磷的具支试管放入80℃的热水中;
⑧…,生成气体进入具支试管中;
⑨关闭K1 , 打开K2 , 往装置乙中加入适量的盐酸。
(1)、实验步骤②的目的是;(2)、在实验步骤⑥中,具支试管中氧气已经排尽的实验现象是;(3)、步骤⑧中…处应进行的操作是 , 才能看到白磷燃烧起来的实验现象;(4)、已知白磷的化学式为P,写出白磷燃烧的化学方程式。结论:可燃物燃烧必须与氧气接触,温度达到其着火点。 -
11、2025年,第四批052D 驱逐舰的飞行甲板上,全新涂装的Z·20F 舰载反潜直升机揭开面纱。如图甲,这款代号“黑旋风”的国产机型,其机尾有根“棍子”,叫做舰载磁异探测器,它能将潜艇经过海域引起的磁场强弱变化转为相应的变化电流,从而发现潜艇的存在。那么,感应电流是如何产生的呢?下面是小明的探究过程,如图乙所示。请帮他解答相应问题。
 (1)、小明进行了如图丙中的1-5五次操作,在1-5主次操作中电流表指针能发生偏转的是1、3、4;小明分析实验现象,得出了产生感应电流的条件:闭合电路中的一部分导体在磁场中做 时,导体中就会产生感应电流。在此装置中,相当于电源;(2)、在探究实验中,小明发现每次电流表指针摆动的角度不同,猜想可能与导体切割磁感线运动速度有关。小明为了验证自己的猜想,再次利用如图乙装置进行多次实验(导体运动区域的磁场强弱相同)。如表所示是实验测得的数据,分析数据可得出结论:在磁场强弱相同时,;
(1)、小明进行了如图丙中的1-5五次操作,在1-5主次操作中电流表指针能发生偏转的是1、3、4;小明分析实验现象,得出了产生感应电流的条件:闭合电路中的一部分导体在磁场中做 时,导体中就会产生感应电流。在此装置中,相当于电源;(2)、在探究实验中,小明发现每次电流表指针摆动的角度不同,猜想可能与导体切割磁感线运动速度有关。小明为了验证自己的猜想,再次利用如图乙装置进行多次实验(导体运动区域的磁场强弱相同)。如表所示是实验测得的数据,分析数据可得出结论:在磁场强弱相同时,;实验次数
1
2
3
4
5
速度v/ cm/s
1
2
3
4
5
电流 I/mA
2.0
4.0
5.9
8.1
10.2
(3)、图中实验现象与 (选填“动圈式话筒”或“扬声器”)的工作原理相同。 -
12、如图是实验室制取气体的有关仪器和装置,据图回答下列问题。
 (1)、请写出图中标有序号②的仪器名称:(2)、加热氯酸钾和二氧化锰混合物的方法制取氧气,选择BEF 组合装置时,实验完毕,为防止水槽中的水倒流入试管使试管炸裂,停止实验的正确操作是。(3)、某同学用排水法收集了一瓶氧气,测得氧气的纯度偏低,原因可能是(填字母)。
(1)、请写出图中标有序号②的仪器名称:(2)、加热氯酸钾和二氧化锰混合物的方法制取氧气,选择BEF 组合装置时,实验完毕,为防止水槽中的水倒流入试管使试管炸裂,停止实验的正确操作是。(3)、某同学用排水法收集了一瓶氧气,测得氧气的纯度偏低,原因可能是(填字母)。a.收集气体前,集气瓶没有注满水
b.导管口开始有气泡冒出,立刻收集
c.收集气体后,集气瓶中仍有少量水
(4)、如图为上述反应过程中某变量y随时间的变化趋势,纵坐标表示的是( )。 A、固体中氧元素的质量 B、生成O2的质量 C、固体中 MnO2的质量分数 D、固体中钾元素的质量
A、固体中氧元素的质量 B、生成O2的质量 C、固体中 MnO2的质量分数 D、固体中钾元素的质量 -
13、为探究原子的内部结构,1911年英国科学家卢瑟福进行了α粒子(含有2个质子)轰击金箔散射实验。
 (1)、如图甲,α粒子碰到荧光屏会引起闪光。卢瑟福将荧光屏设计成360°环绕,基于的假设是α粒子可能穿过金箔,也可能。(2)、根据α粒子散射实验数据,统计不同偏转角度的α粒子数量,并绘制成如图乙所示曲线。则图中能说明原子核的体积小但质量大的是段曲线。(选填“AB”“AC”或“BC”)
(1)、如图甲,α粒子碰到荧光屏会引起闪光。卢瑟福将荧光屏设计成360°环绕,基于的假设是α粒子可能穿过金箔,也可能。(2)、根据α粒子散射实验数据,统计不同偏转角度的α粒子数量,并绘制成如图乙所示曲线。则图中能说明原子核的体积小但质量大的是段曲线。(选填“AB”“AC”或“BC”) -
14、如图所示是老师设计的一个实验装置,用来探究“影响电磁铁磁性强弱因素”,它是由电源、滑动变阻器、开关、带铁芯的螺线管(线圈电阻忽略不计)和自制的针式刻度板组成,通过观察指针偏转角度的大小,来判断电磁铁磁性的强弱。用竹片削制的指针下方加装固定一物体E,导线a与接线柱2相连。
【制定计划与设计实验】
 (1)、.按如图所示连接好电路,闭合开关,调节滑动变阻器滑片 P到某一位置,记下此时指针偏转的角度,保持滑片P位置不变,导线a改为与接线柱1相连,可以探究电磁铁磁性强弱与的关系;保持接线方式不变,移动变阻器滑片 P,可以探究电磁铁磁性强弱与另外一个因素的关系。(2)、【进行实验与收集证据】
(1)、.按如图所示连接好电路,闭合开关,调节滑动变阻器滑片 P到某一位置,记下此时指针偏转的角度,保持滑片P位置不变,导线a改为与接线柱1相连,可以探究电磁铁磁性强弱与的关系;保持接线方式不变,移动变阻器滑片 P,可以探究电磁铁磁性强弱与另外一个因素的关系。(2)、【进行实验与收集证据】.当滑动变阻器的滑片P向左滑动时,指针偏转的角度将会(选填“增大”或“减小”)。
(3)、.【评估交流】在实验过程中该自制装置的指针均向右偏转,只是偏转角度不同,若要让指针向左偏转,需要将一块小磁铁换装在如图E处,且让磁铁的右端为极。
-
15、已知某溶液由硝酸、盐酸、硫酸、硫酸钠、碳酸钠、硝酸铜等稀溶液中的两种组成。向该溶液逐滴滴加 Ba(OH)2溶液的体积与生成沉淀的关系如右图所示。则该溶液肯定存在 ;肯定不存在。

-
16、如图甲所示,水平桌面上,两块相同的条形磁铁在水平推力F1的作用下,做匀速直线运动。
 (1)、取走其中一块后,磁铁在水平推力F2的作用下仍做匀速直线运动,如图乙,则F2F1(选填“>、=或<”)。(2)、如图丙,磁铁在F2作用下,匀速直线运动过程中,若闭合开关S,则磁铁速度将(选填“变大”“不变”或“变小”),此时,将滑动变阻器的滑片向左移动,欲保持磁铁匀速直线运动,F2应(选填“变大”“不变”或“变小”)。
(1)、取走其中一块后,磁铁在水平推力F2的作用下仍做匀速直线运动,如图乙,则F2F1(选填“>、=或<”)。(2)、如图丙,磁铁在F2作用下,匀速直线运动过程中,若闭合开关S,则磁铁速度将(选填“变大”“不变”或“变小”),此时,将滑动变阻器的滑片向左移动,欲保持磁铁匀速直线运动,F2应(选填“变大”“不变”或“变小”)。 -
17、植物的光合作用和呼吸作用强度可以用单位时间内吸收或释放二氧化碳的量来表示。如图是某植物在恒温30℃时,处于不同光照下在单位时间内对二氧化碳的吸收或释放量。
 (1)、植物吸收或释放二氧化碳的主要通道是叶表皮的。(2)、已知该植物光合作用和呼吸作用最适温度分别为25℃和30℃。那么在其它条件不变的情况下,将温度调节到25℃时,图中曲线上的A 点将向移动(填“上”或“下”)。
(1)、植物吸收或释放二氧化碳的主要通道是叶表皮的。(2)、已知该植物光合作用和呼吸作用最适温度分别为25℃和30℃。那么在其它条件不变的情况下,将温度调节到25℃时,图中曲线上的A 点将向移动(填“上”或“下”)。 -
18、如图为实验室制取和收集常见气体的装置示意图。
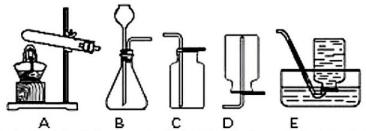 (1)、实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式(2)、实验室制取和收集二氧化碳应选用的装置组合是(填字母代号)
(1)、实验室用过氧化氢和二氧化锰制取氧气,反应的化学方程式(2)、实验室制取和收集二氧化碳应选用的装置组合是(填字母代号) -
19、用化学符号填空:
n个钠离子; 3个硫酸根离子; 2个氮原子;
地壳中含量最多的金属元素与最多的非金属元素组成化合物的化学式;
-
20、某无色气体X可能含有氢气、一氧化碳、二氧化碳和甲烷四种气体中的一种或两种。为确认其组成,某同学取一定量该气体按如图所示装置进行实验(假设每步都充分反应或吸收),结果装置①中无明显变化,装置③增重1.8g,装置④增重2.2g。下列关于气体X成分的分析中,错误的是( )
(提示:碱石灰的主要成分是氧化钙和氢氧化钠)
 A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能含有氢气和一氧化碳
A、一定没有二氧化碳 B、可能含有甲烷和氢气 C、可能只有甲烷 D、可能含有氢气和一氧化碳