-
1、碘在地壳中主要以NaIO3的形式存在,在海水中主要以I-的形式存在,几种粒子之间有如图所示关系,根据图示转化关系推测下列说法错误的是
 A、用KI淀粉试纸和食醋可以检验加碘盐中是否含 B、足量能使湿润的KI淀粉试纸变白的原因可能是: C、由图可知氧化性的强弱顺序为 D、途径Ⅱ反应生成I2 , 该反应中NaHSO3作还原剂
A、用KI淀粉试纸和食醋可以检验加碘盐中是否含 B、足量能使湿润的KI淀粉试纸变白的原因可能是: C、由图可知氧化性的强弱顺序为 D、途径Ⅱ反应生成I2 , 该反应中NaHSO3作还原剂 -
2、下列关于钠及其化合物的说法错误的是A、将金属钠放入盛有饱和溶液的小烧杯中,既有气体放出,又有沉淀产生 B、与的阴、阳离子个数比相同 C、、、、长期放置在空气中,最终都会转变成 D、溶液和发生反应时,产物不会随反应物用量的改变而改变
-
3、天然气是应用广泛的燃料,但含有少量H2S等气体。在酸性溶液中利用硫杆菌可实现天然气的催化脱硫,其原理如图所示。下列说法不正确的是
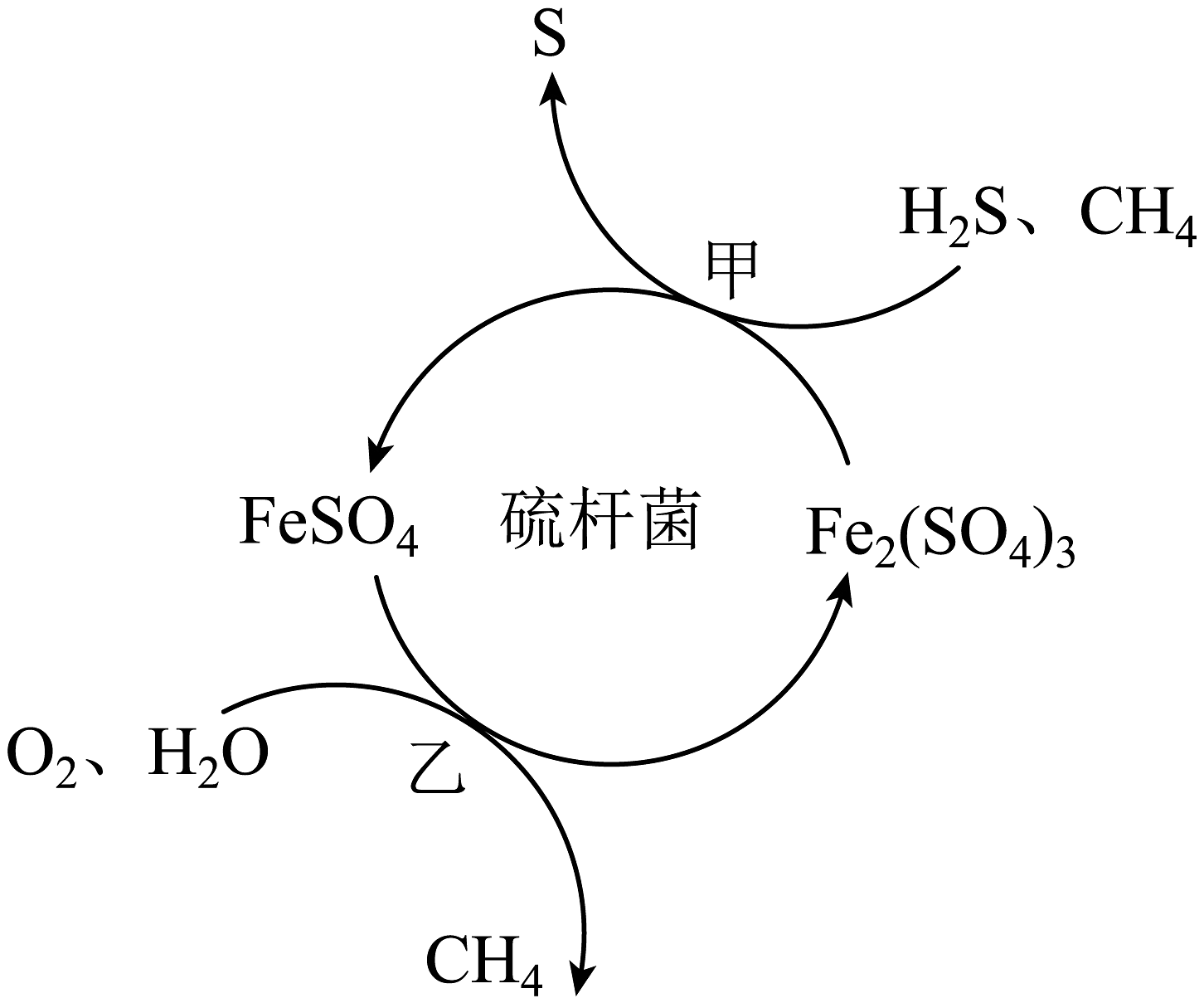 A、过程甲中氧化产物与还原产物的化学计量数之比为1:2 B、脱硫过程O2间接氧化H2S C、该脱硫过程需要不断添加Fe2(SO4)3溶液 D、过程乙发生反应的离子方程式为:
A、过程甲中氧化产物与还原产物的化学计量数之比为1:2 B、脱硫过程O2间接氧化H2S C、该脱硫过程需要不断添加Fe2(SO4)3溶液 D、过程乙发生反应的离子方程式为: -
4、使用如图装置(搅拌装置略)探究溶液离子浓度变化,灯光变化不可能出现“亮→暗(或灭)→亮”现象的是

试剂a
试剂b
A.
B.
C.
CuSO4
D.
CH3COOH
A、A B、B C、C D、D -
5、用图1所示装置向装有一瓶氯气的集气瓶中添加适量的蒸馏水,振荡,先利用注射器滴加溶液,再利用注射器滴加稀盐酸,用压强传感器测得集气瓶内的压强随时间变化的曲线如图2所示。下列说法正确的是
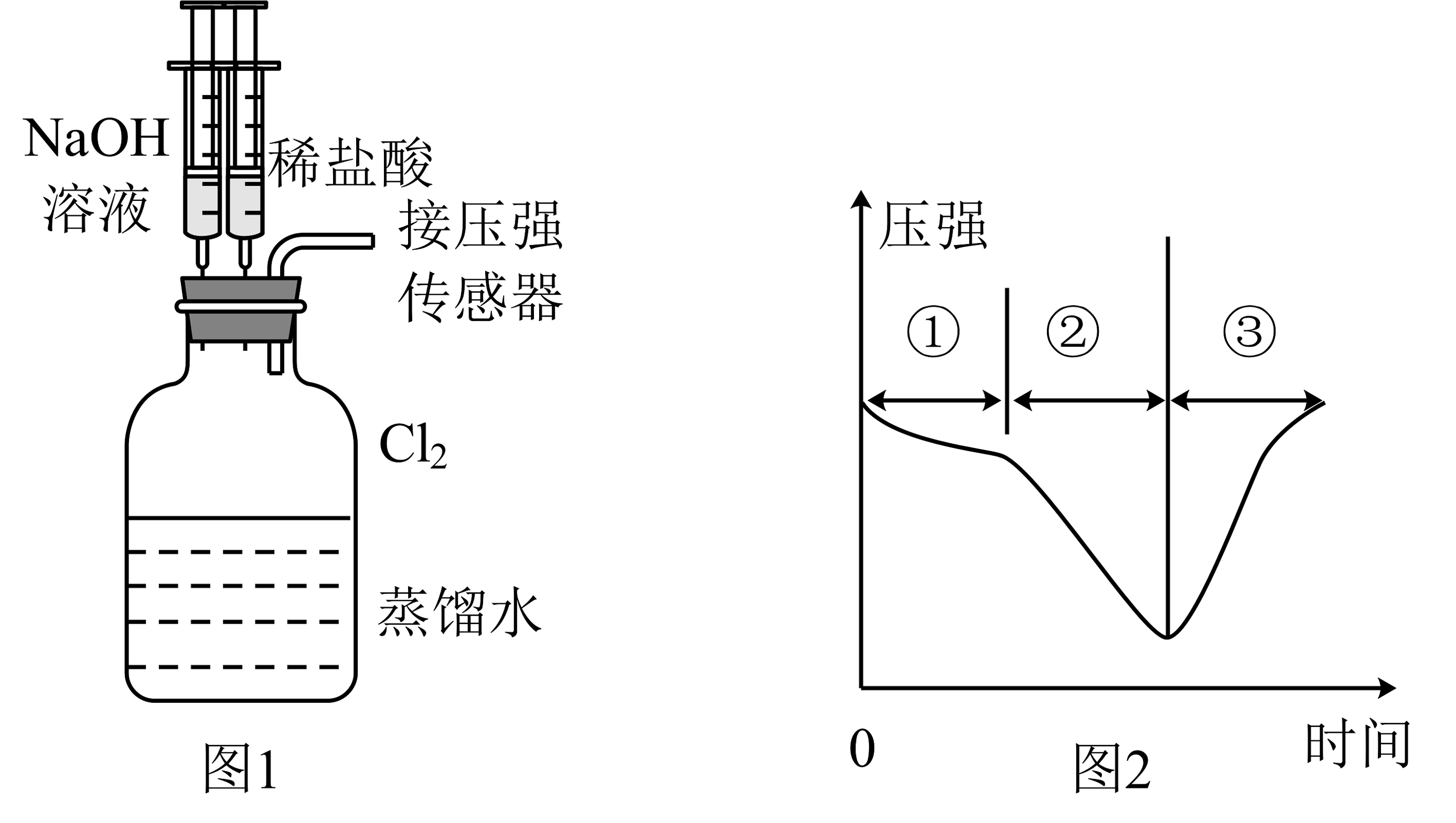 A、阶段①说明氯气溶于水,溶于水的氯气全部与水反应 B、阶段②的压强变小,可利用该过程发生的反应制备漂白粉 C、阶段③发生反应的离子方程式为 D、若将换成 , 则压强变化不会出现图2趋势
A、阶段①说明氯气溶于水,溶于水的氯气全部与水反应 B、阶段②的压强变小,可利用该过程发生的反应制备漂白粉 C、阶段③发生反应的离子方程式为 D、若将换成 , 则压强变化不会出现图2趋势 -
6、“光荣属于劳动者,幸福属于劳动者。”下列劳动项目与所述化学知识没有关联的是
选项
劳动项目
化学知识
A.
环保行动:用净水
具有氧化性
B.
化学实验员:检验是否失效
C.
用卤水点热豆浆制豆腐
卤水中电解质能使豆浆胶体聚沉
D.
农业活动:用生石灰改良酸性土壤
CaO是一种碱性氧化物
A、A B、B C、C D、D -
7、下列“类比”结果正确的是A、向固体中加入少量水放出热量,则向固体中加入少量水也放出热量 B、相同温度下,的溶解度比的大,则的溶解度也比的大 C、酸性氧化物与水反应生成碳酸,则酸性氧化物与水反应生成硫酸 D、少量通入溶液中产生白色沉淀,则通入溶液也产生白色沉淀
-
8、下列叙述正确的是A、NH3溶于水能导电,所以NH3为电解质 B、等质量的与足量氧气反应,在常温、加热条件下转移电子数一样多 C、漂白液和漂白粉都可用于棉、麻、纸张的漂白剂,但二者的原理不同 D、金属元素发生化学反应形成各种焰色用以制五彩缤纷的烟花
-
9、化学是一门以实验为基础的学科。下列实验方案能够达到实验目的的是
实验方案


实验目的
A.通过焰色反应确认溶液中是否含有K+
B.验证Na与水反应是否为放热反应
实验方案


实验目的
C.比较Na2CO3和NaHCO3的热稳定性
D.制备Fe(OH)3胶体
A、A B、B C、C D、D -
10、下列关于的化合物之间转化反应的离子方程式书写正确的是A、碱转化为酸式盐: B、过氧化物转化为碱: C、单质转化为一种盐: D、碱转化为两种盐:
-
11、利用可将废水中的转化为对环境无害的物质后排放。反应原理为:(未配平)下列说法正确的是A、是氧化产物 B、可用替换 C、氧化剂与还原剂的化学计量数之比为 D、若生成 , 则理论上消耗
-
12、碳酸钠和碳酸氢钠在生产生活中有广泛的应用,下列有关说法不合理的是A、通过化合反应可由碳酸钠制得碳酸氢钠 B、两者溶液能使用澄清石灰水鉴别 C、碳酸钠溶液和碳酸氢钠溶液均可用作食用碱 D、盐酸分别滴加到等浓度的碳酸钠、碳酸氢钠溶液中放出气体的速度:
-
13、化学与生活密切相关,下列说法不正确的是A、氧化钙易吸水,可用作干燥剂 B、豆浆能产生丁达尔效应是由于胶体粒子对光线的散射 C、连花清瘟胶囊的成分中石膏CaSO4∙2H2O属于纯净物 D、维生素C可用作水果罐头的抗氧化剂是由于其难以被氧化
-
14、下列现象不涉及氧化还原反应的是A、黑火药爆炸 B、高压钠灯广泛用于道路照明 C、“84”消毒液消毒 D、铁钉生锈
-
15、近年来我国航天事业发展迅速,下列对所涉及化学知识的叙述错误的是A、火焰喷雾技术制备纳米材料:在高温火焰喷雾中形成的胶体属于气溶胶 B、“侯氏制碱法”利用海水、氨和制备纯碱,不涉及氧化还原反应 C、“长征七号”采用了液氧煤油发动机,煤油是纯净物 D、2022年北京冬奥会展示的智能服饰含有石墨烯,石墨烯与金刚石互为同素异形体
-
16、以印刷线路板的碱性蚀刻废液(主要成分为)为原料可制取CuO。
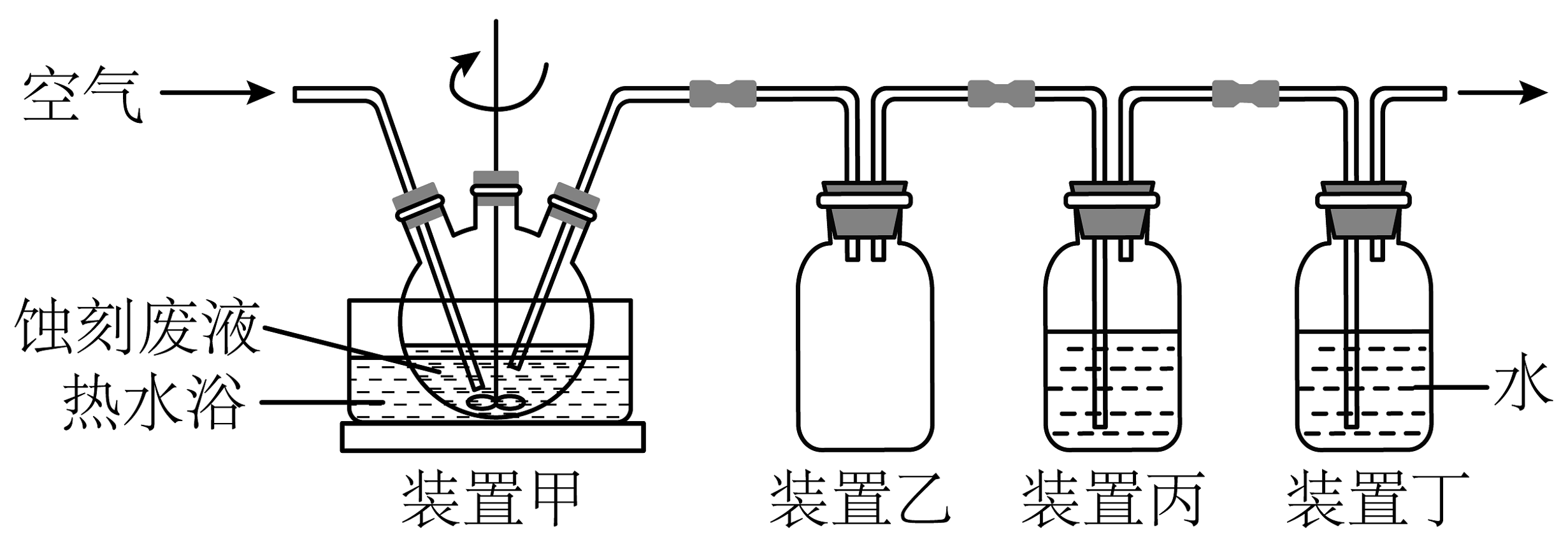 (1)、取一定量蚀刻废液和稍过量的NaOH溶液加入到装置甲的三颈瓶中,在搅拌下加热反应并通入空气,有产生,反应结束后将装置甲内混合物过滤,得到含NaCl的滤液,将滤渣洗涤,得到CuO。
(1)、取一定量蚀刻废液和稍过量的NaOH溶液加入到装置甲的三颈瓶中,在搅拌下加热反应并通入空气,有产生,反应结束后将装置甲内混合物过滤,得到含NaCl的滤液,将滤渣洗涤,得到CuO。①写出三颈瓶内反应的化学方程式:。
②检验滤渣已经洗涤干净的方式是:。
③装置乙的作用是:。
④为检验反应中有生成,装置丙中可盛装的溶液是。
(2)、将含少量杂质的CuO溶于稀硫酸中,向其中加入KI溶液,发生反应:。向溶液中滴加溶液,发生反应:。恰好完全反应时消耗的溶液20.00mL。计算CuO的质量,写出计算过程(杂质不参与反应)。 -
17、是常见的试剂,可用于有机物的转化。一定条件下,可以发生如下图所示的转化:
 (1)、写出转化Ⅰ反应的化学方程式:。(2)、乙酸中所含官能团的名称为。(3)、如图所示为实验室制取乙酸乙酯的实验装置(试剂未标注)。
(1)、写出转化Ⅰ反应的化学方程式:。(2)、乙酸中所含官能团的名称为。(3)、如图所示为实验室制取乙酸乙酯的实验装置(试剂未标注)。
①写出如图所示装置中乙醇和乙酸反应的化学方程式:。
②右侧小试管中应装有溶液。
-
18、固体为紫色,是一种高效水处理剂,为探究其性质,现进行如下实验:
实验1:取相同质量的二份固体,分别加入等体积的浓KOH溶液和水中,加入水中的完全溶解,溶液中有气体生成,用激光笔照射溶液,内部出现一条光亮的通路,浓KOH溶液中有大量紫色固体未溶解,溶液中无气体生成,用激光笔照射溶液,内部无光亮的通路。
实验2:向少量固体中加入足量盐酸,固体完全反应,有黄绿色气体产生。所得溶液为黄色,滴加KSCN溶液后变为红色。
依据实验现象所得结论不正确的是
A、可作水处理剂的原因是其具有强氧化性 B、在水中的溶解性大于在浓KOH溶液中 C、在水中可能有和胶体生成 D、与盐酸反应后有和生成 -
19、下列实验方案能达到预期目的的是A、用浓硫酸干燥氨气 B、用溶液鉴别溶液和溶液 C、用加热的方法除去固体中的 D、用焰色试验(又称焰色反应)鉴别NaCl和固体
-
20、短周期主族元素X、Y、Z的原子序数依次增大,X原子最外层电子数是次外层电子数的3倍,Y是短周期中金属性最强的元素,Z与X位于同一主族。下列叙述正确的是A、原子半径: r(Z)>r(X)>r(Y) B、X的简单气态氢化物的热稳定性比Z弱 C、X、Y、Z三种元素可形成化合物Y2ZX3 D、Y形成的最高价氧化物的水化物是弱碱