备考2026届高考 2021-2025全国各地真题汇编专题12有机物的结构烃和烃的衍生
试卷更新日期:2026-04-22 类型:二轮复习
一、选择题
-
1. 下列有关物质性质与用途对应关系错误的是( )A、单晶硅熔点高,可用于制造芯片 B、金属铝具有还原性,可用于冶炼金属 C、浓硫酸具有吸水性,可用作干燥剂 D、乙炔燃烧火焰温度高,可用于切割金属2. 下列化学用语表示不正确的是( )A、CH4的结构式:
 B、基态氧原子的轨道表示式
B、基态氧原子的轨道表示式 C、p 电子云轮廓图:
C、p 电子云轮廓图: D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
3. 化学实验充满着五颜六色的变化。下列描述错误的是( )A、
D、CH3CH(CH2CH3)CH2CH3的系统命名:2-乙基丁烷
3. 化学实验充满着五颜六色的变化。下列描述错误的是( )A、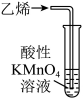
溶液褪色 B、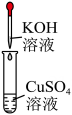
产生红色沉淀 C、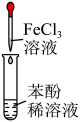
溶液呈紫色 D、
试纸变为蓝色
4. 下列说法不正确的是( )A、糖类、蛋白质和油脂均为天然高分子 B、蔗糖发生水解反应所得产物互为同分异构体 C、蛋白质在酶的作用下水解可得到氨基酸 D、不饱和液态植物油通过催化加氢可提高饱和度5. “稀土之父”徐光宪先生提出了稀土串级萃取理论,其基本操作是利用有机络合剂把稀土离子从水相富集到有机相再进行分离。分离时可用的玻璃装置是A、 B、
B、 C、
C、 D、
D、 6. 我国科学家报道了如下反应。
6. 我国科学家报道了如下反应。
有关该反应的说法错误的是( )
A、反应物与产物的摩尔质量相同 B、反应物与产物的红外光谱相同 C、反应物与产物均能使酸性高锰酸钾溶液褪色 D、反应过程中有碳氢键的断裂和碳碳双键的形成7. 仪器分析在化学研究中有重要应用。下列方法选择错误的是( )A、用pH计区分KCl溶液和NaNO3溶液 B、用X射线衍射法区分玻璃和蓝宝石 C、用原子光谱鉴定样品中含有元素Li D、用质谱区分正己醇和正庚醇8. 传统方法中,制备化合物c常用到NaCN。某课题组提出了一种避免使用NaCN的方法,机理如图所示(L表示配体,0、I、I、Ⅲ表示价态)。下列说法不正确的是( ) A、化合物 b是NaCN 的替代品 B、
A、化合物 b是NaCN 的替代品 B、 是该过程产生的副产物
C、M 可能是 R3SiBr 和 H+
D、整个过程中,含镍化合物发生了2次氧化反应
9. 人体皮肤细胞受到紫外线(UV)照射可能造成DNA损伤,原因之一是脱氧核苷上的碱基发生了如下反应。下列说法错误的是( )
是该过程产生的副产物
C、M 可能是 R3SiBr 和 H+
D、整个过程中,含镍化合物发生了2次氧化反应
9. 人体皮肤细胞受到紫外线(UV)照射可能造成DNA损伤,原因之一是脱氧核苷上的碱基发生了如下反应。下列说法错误的是( ) A、该反应为取代反应 B、Ⅰ和Ⅱ均可发生酯化反应 C、Ⅰ和Ⅱ均可发生水解反应 D、乙烯在UV下能生成环丁烷10. 在法拉第发现苯200周年之际,我国科学家首次制备了以金属M为中心的多烯环配合物。该配合物具有芳香性,其多烯环结构(如图)形似梅花。该多烯环上
A、该反应为取代反应 B、Ⅰ和Ⅱ均可发生酯化反应 C、Ⅰ和Ⅱ均可发生水解反应 D、乙烯在UV下能生成环丁烷10. 在法拉第发现苯200周年之际,我国科学家首次制备了以金属M为中心的多烯环配合物。该配合物具有芳香性,其多烯环结构(如图)形似梅花。该多烯环上 A、键是共价键 B、有8个碳碳双键 C、共有16个氢原子 D、不能发生取代反应11. 物质的微观结构决定其宏观性质。乙腈()是一种常见的有机溶剂,沸点较高,水溶性好。下列说法不正确的是( )A、乙腈的电子式:
A、键是共价键 B、有8个碳碳双键 C、共有16个氢原子 D、不能发生取代反应11. 物质的微观结构决定其宏观性质。乙腈()是一种常见的有机溶剂,沸点较高,水溶性好。下列说法不正确的是( )A、乙腈的电子式: B、乙腈分子中所有原子均在同一平面
C、乙腈的沸点高于与其分子量相近的丙炔
D、乙腈可发生加成反应
12. 劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是
B、乙腈分子中所有原子均在同一平面
C、乙腈的沸点高于与其分子量相近的丙炔
D、乙腈可发生加成反应
12. 劳动人民的发明创造是中华优秀传统文化的组成部分。下列化学原理描述错误的是发明
关键操作
化学原理
A
制墨
松木在窑内焖烧
发生不完全燃烧
B
陶瓷
黏土高温烧结
形成新的化学键
C
造纸
草木灰水浸泡树皮
促进纤维素溶解
D
火药
硫黄、硝石和木炭混合,点燃
发生氧化还原反应
A、A B、B C、C D、D13. 下列化学用语或图示正确的是A、 的系统命名:2-甲基苯酚
B、分子的球棍模型:
的系统命名:2-甲基苯酚
B、分子的球棍模型: C、激发态H原子的轨道表示式:
C、激发态H原子的轨道表示式: D、键形成的轨道重叠示意图:
D、键形成的轨道重叠示意图: 14. 酯在NaOH溶液中发生水解反应,历程如下:
14. 酯在NaOH溶液中发生水解反应,历程如下: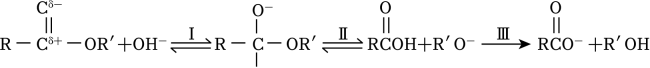
已知:
①
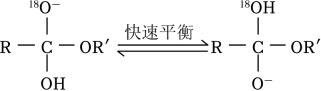
②RCOOCH2CH3水解相对速率与取代基R的关系如下表:
取代基R
CH3
ClCH2
Cl2CH
水解相对速率
1
290
7200
下列说法不正确的是( )
A、步骤Ⅰ是OH﹣与酯中Cδ+作用 B、步骤Ⅲ使Ⅰ和Ⅱ平衡正向移动,使酯在NaOH溶液中发生的水解反应不可逆 C、酯的水解速率:FCH2COOCH2CH3>ClCH2COOCH2CH3 D、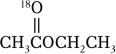 与OH﹣反应、
与OH﹣反应、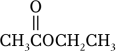 与18OH﹣反应,两者所得醇和羧酸盐均不同
15. 利用如图装置进行实验:打开 , 一定时间后,a中溶液变蓝;关闭 , 打开 , 点燃酒精灯加热数分钟后,滴入无水乙醇。下列说法错误的是
与18OH﹣反应,两者所得醇和羧酸盐均不同
15. 利用如图装置进行实验:打开 , 一定时间后,a中溶液变蓝;关闭 , 打开 , 点燃酒精灯加热数分钟后,滴入无水乙醇。下列说法错误的是 A、a中现象体现了的还原性 B、b中既作氧化剂也作还原剂 C、乙醇滴加过程中,c中的铜丝由黑变红,说明乙醇被氧化 D、d中有银镜反应发生,说明c中产物有乙酸
A、a中现象体现了的还原性 B、b中既作氧化剂也作还原剂 C、乙醇滴加过程中,c中的铜丝由黑变红,说明乙醇被氧化 D、d中有银镜反应发生,说明c中产物有乙酸二、综合题
-
16.
已知反应1
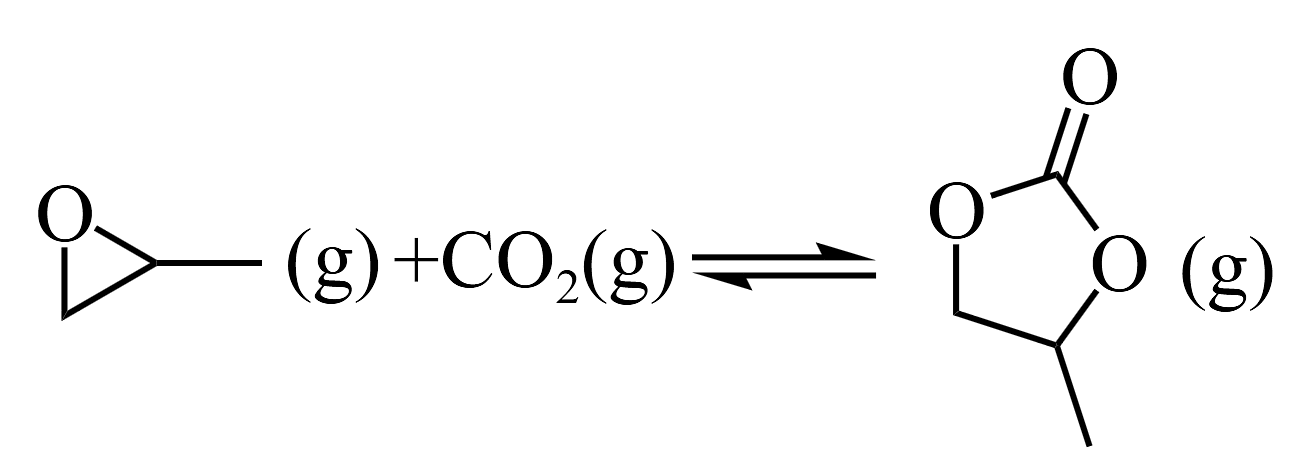 的
的反应2的
反应3的
反应4的
物质
环氧丙烷
(1)计算出_______。
A. B. 613.2 C. 395.2 D. (2)随温度T的变化趋势________。
(3)
 中电负性最大的是________。
中电负性最大的是________。A.C B.H C.O
(4)
 分了中键的数目为_______。
分了中键的数目为_______。A. 7 B. 12 C. 13 D. 14 已知:环氧丙烷生成
 会发生副反应
会发生副反应选择性=转化生成A的环氧丙烷/消耗环氧丙烷
M(环氧丙烷) ρ(环氧丙烷)
容器容积的高压反应釜反应后体积缩小为 , 选择性为95%,反应。
(5)求环氧丙烷的化学反应速率________(精确到小数点后2位)
(6)下列哪种操作可以使得活化分子的百分数变大_______。
A. 升高温度 B. 增大浓度 C. 压缩容器 D. 充入惰性气体 (7)碳酸丙烯酯相同时间内随温度变化如图所示,请解释产率随温度先升后下降的原因________。
(8)达到平衡的判据_______。
A. v正=v逆 B. 体系总质量不变 C. 气体体积不再变化 D. 混合气体密度(可能是摩尔质量)不变 (9)制备
 还有一种光气法,用
还有一种光气法,用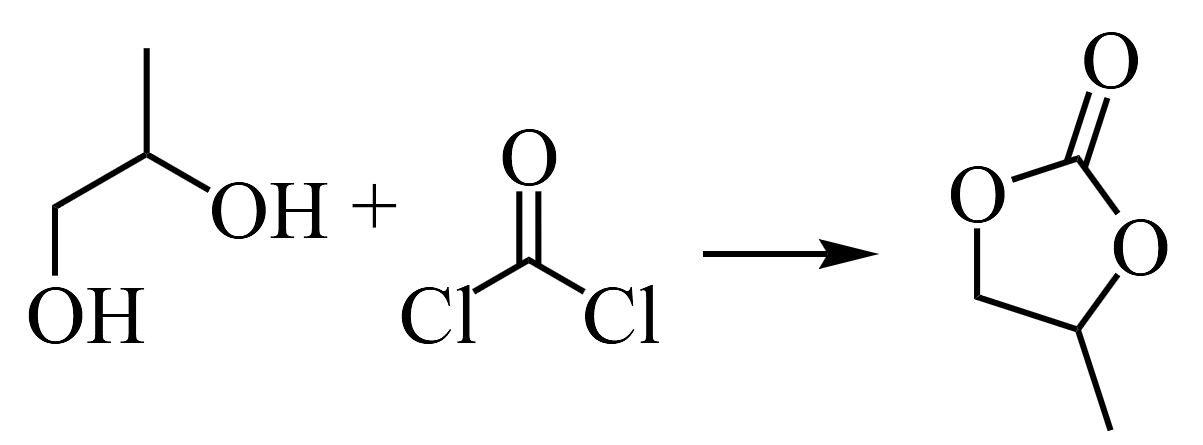 。请从绿色化学的角度解释,写出3点与光气-二醇法相比,法合成的优势________。17. 我国化学工作者成功开发出新型零排放的制氢技术,这项突破性工艺的反应式为。回答下列问题:(1)、认识一种有机物,可以先从其结构入手。某有机物的分子结构模型如图所示,该物质是(填标号),它属于(填“烃”或“烃的衍生物”),其中所含官能团的名称是。
。请从绿色化学的角度解释,写出3点与光气-二醇法相比,法合成的优势________。17. 我国化学工作者成功开发出新型零排放的制氢技术,这项突破性工艺的反应式为。回答下列问题:(1)、认识一种有机物,可以先从其结构入手。某有机物的分子结构模型如图所示,该物质是(填标号),它属于(填“烃”或“烃的衍生物”),其中所含官能团的名称是。
A. B. C. D.
(2)、乙醇和乙酸之间可以发生如图所示的转化(反应条件已略去):
写出乙醇在一定条件下发生催化氧化生成有机物B的化学方程式:(有机物用结构简式表示)。
(3)、由乙酸得到有机物A的反应类型是 , 实验室制备A时,为加快反应速率,一般需加热并加入浓硫酸,浓硫酸的作用是;并将产生的A蒸气经导管通到饱和溶液的液面上方,饱和溶液的作用是。18. 将3D打印制备的固载铜离子陶瓷催化材料,用于化学催化和生物催化一体化技术,以实现化合物Ⅲ的绿色合成,示意图如下(反应条件路)。 (1)、化合物I的分子式为 , 名称为。(2)、化合物Ⅱ中含氧官能团的名称是。化合物Ⅱ的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且能够发生银镜反应,其结构简式为。(3)、关于上述示意图中的相关物质及转化,下列说法正确的有____。A、由化合物I到Ⅱ的转化中,有键的断裂与形成 B、由葡萄糖到葡萄糖酸内酯的转化中,葡萄糖被还原 C、葡萄糖易溶于水,是因为其分子中有多个羟基,能与水分子形成氢键 D、由化合物Ⅱ到Ⅲ的转化中,存在C、O原子杂化方式的改变,有手性碳原子形成(4)、对化合物Ⅲ,分析预测其可能的化学性质,完成下表。
(1)、化合物I的分子式为 , 名称为。(2)、化合物Ⅱ中含氧官能团的名称是。化合物Ⅱ的某同分异构体含有苯环,在核磁共振氢谱图上只有4组峰,且能够发生银镜反应,其结构简式为。(3)、关于上述示意图中的相关物质及转化,下列说法正确的有____。A、由化合物I到Ⅱ的转化中,有键的断裂与形成 B、由葡萄糖到葡萄糖酸内酯的转化中,葡萄糖被还原 C、葡萄糖易溶于水,是因为其分子中有多个羟基,能与水分子形成氢键 D、由化合物Ⅱ到Ⅲ的转化中,存在C、O原子杂化方式的改变,有手性碳原子形成(4)、对化合物Ⅲ,分析预测其可能的化学性质,完成下表。序号
反应试剂、条件
反应形成的新结构
反应类型
①

②
取代反应
(5)、在一定条件下,以原子利用率的反应制备。该反应中,①若反应物之一为非极性分子,则另一反应物为(写结构简式)。
②若反应物之一为V形结构分子,则另一反应物为(写结构简式)。
(6)、以2-溴丙烷为唯一有机原料,合成。基于你设计的合成路线,回答下列问题:①最后一步反应的化学方程式为(注明反应条件)。
②第一步反应的化学方程式为(写一个即可,注明反应条件)。
19. 我国学者报道了一种制备醇的新方法,其合成及进一步转化为化合物H的反应路线如下所示。
已知:

R1:烷基、芳香基;R2:芳香基、烷基、H;R3:芳香基、烷基
(1)、A→B的反应试剂及条件为。(2)、B的含有碳氧双键的同分异构体数目为(不考虑立体异构)。(3)、C的系统命名法的名称为 , 其核磁共振氢谱有组吸收峰。(4)、D中最多共平面原子数目为。(5)、E中官能团的名称为 , 含有的手性碳原子数目为。(6)、E→F的反应类型为。(7)、G→H的反应方程式为。(8)、以 及题干中的有机化合物为原料(无机试剂任选),参考所给反应路线及条件,完成下列目标化合物的合成。
及题干中的有机化合物为原料(无机试剂任选),参考所给反应路线及条件,完成下列目标化合物的合成。
三、实验探究题
-
20. 酸及盐在生活生产中应用广泛。(1)、甲苯氧化可生成苯甲酸。向盛有2mL甲苯的试管中,加入几滴酸性溶液,振荡,观察到体系颜色。(2)、某苯甲酸粗品含少量泥沙和氯化钠。用重结晶法提纯该粗品过程中,需要的操作及其顺序为:加热溶解、(填下列操作编号)。
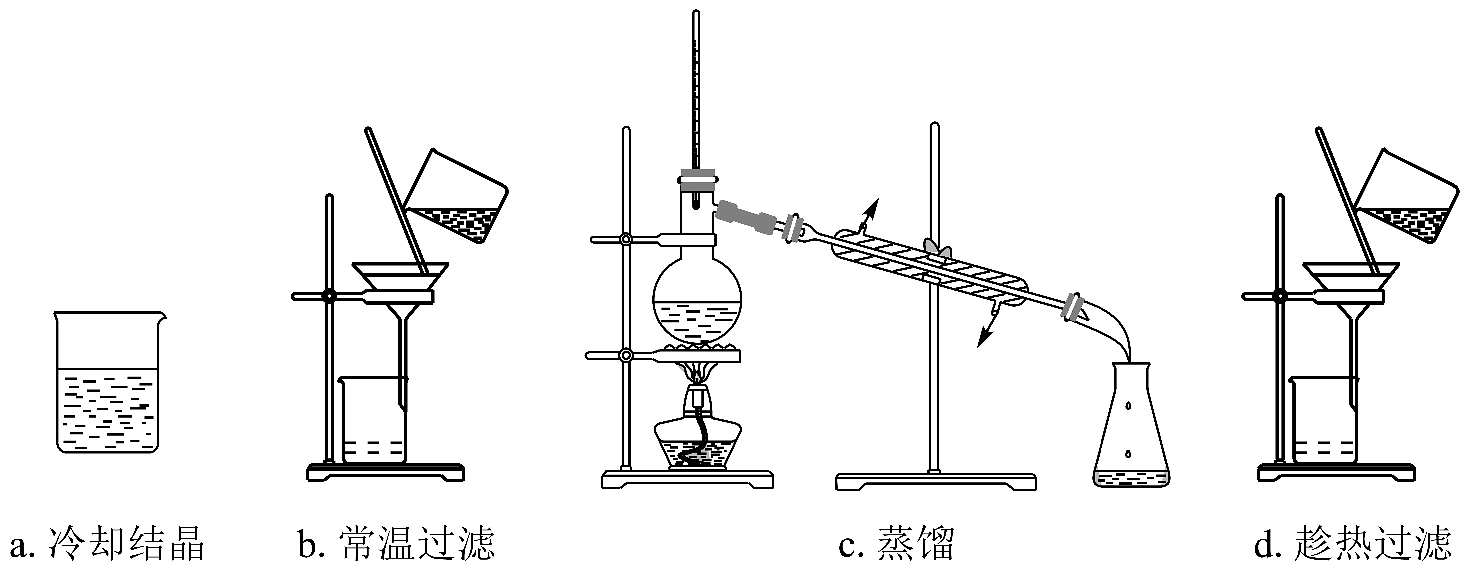 (3)、兴趣小组测定常温下苯甲酸饱和溶液的浓度和苯甲酸的 , 实验如下:取50.00mL苯甲酸饱和溶液,用溶液滴定,用pH计测得体系的pH随滴入溶液体积V变化的曲线如图。据图可得:
(3)、兴趣小组测定常温下苯甲酸饱和溶液的浓度和苯甲酸的 , 实验如下:取50.00mL苯甲酸饱和溶液,用溶液滴定,用pH计测得体系的pH随滴入溶液体积V变化的曲线如图。据图可得:
①。
②苯甲酸的(列出算式,水的电离可忽略)。
(4)、该小组继续探究取代基对芳香酸酸性的影响。①知识回顾 羧酸酸性可用衡量。下列羧酸的变化顺序为:。随着卤原子电负性 , 羧基中的羟基增大,酸性增强。
②提出假设 甲同学根据①中规律推测下列芳香酸的酸性强弱顺序为:

③验证假设 甲同学测得常温下三种酸的饱和溶液的pH大小顺序为Ⅲ>Ⅱ>Ⅰ,据此推断假设成立。但乙同学认为该推断依据不足,不能用所测得的pH直接判断大小顺序,因为。
乙同学用(3)中方法测定了上述三种酸的 , 其顺序为Ⅱ>Ⅰ>Ⅲ。
④实验小结 假设不成立,芳香环上取代基效应较复杂,①中规律不可随意推广。
(5)、该小组尝试测弱酸HClO的。①丙同学认为不宜按照(3)中方法进行实验,其原因之一是次氯酸易分解。该分解反应的离子方程式为。
②小组讨论后,选用0.100mol/LNaClO溶液(含少量NaCl)进行实验,以获得HClO的。简述该方案(包括所用仪器及数据处理思路)。
③教师指导:设计实验方案时,需要根据物质性质,具体问题具体分析。
21. 某小组在探究的还原产物组成及其形态过程中,观察到的实验现象与理论预测有差异。根据实验描述,回答下列问题:(1)、向溶液加入5滴溶液,振荡后加入葡萄糖溶液,加热。①反应产生的砖红色沉淀为(写化学式),葡萄糖表现出(填“氧化”或“还原”)性。
②操作时,没有加入葡萄糖溶液就加热,有黑色沉淀生成。用化学反应方程式说明该沉淀产生的原因:。
(2)、向溶液中加入粉使蓝色完全褪去,再加入盐酸并加热至溶液中无气泡产生为止。过滤得固体,洗涤并真空干燥。①加入盐酸的目的是
②同学甲一次性加入粉,得到红棕色固体,其组成是(填标号)。
a. b.包裹 c. d.和
③同学乙搅拌下分批加入粉,得到黑色粉末X。分析结果表明,X中不含和。关于X的组成提出了三种可能性:Ⅰ ;Ⅱ 和;Ⅲ , 开展了下面2个探究实验:

由实验结果可知,X的组成是(填“Ⅰ”“Ⅱ”或“Ⅲ”)。从物质形态角度分析,X为黑色的原因是。
22. 市售的溴(纯度)中含有少量的和 , 某化学兴趣小组利用氧化还原反应原理,设计实验制备高纯度的溴。回答下列问题:(1)、装置如图(夹持装置等略),将市售的溴滴入盛有浓溶液的B中,水浴加热至不再有红棕色液体馏出。仪器C的名称为;溶液的作用为;D中发生的主要反应的化学方程式为。 (2)、将D中溶液转移至(填仪器名称)中,边加热边向其中滴加酸化的溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成的离子方程式为。(3)、利用图示相同装置,将R和固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓 , 水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为和。(4)、为保证溴的纯度,步骤(3)中固体的用量按理论所需量的计算,若固体R质量为m克(以计),则需称取(用含m的代数式表示)。(5)、本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内壁,转移溶液时用 , 滤液沿烧杯壁流下。
(2)、将D中溶液转移至(填仪器名称)中,边加热边向其中滴加酸化的溶液至出现红棕色气体,继续加热将溶液蒸干得固体R。该过程中生成的离子方程式为。(3)、利用图示相同装置,将R和固体混合均匀放入B中,D中加入冷的蒸馏水。由A向B中滴加适量浓 , 水浴加热蒸馏。然后将D中的液体分液、干燥、蒸馏,得到高纯度的溴。D中蒸馏水的作用为和。(4)、为保证溴的纯度,步骤(3)中固体的用量按理论所需量的计算,若固体R质量为m克(以计),则需称取(用含m的代数式表示)。(5)、本实验所用钾盐试剂均经重结晶的方法纯化。其中趁热过滤的具体操作为漏斗下端管口紧靠烧杯内壁,转移溶液时用 , 滤液沿烧杯壁流下。