备考2026届高考 2021-2025全国各地真题汇编专题2离子反应氧化还原反应
试卷更新日期:2026-04-22 类型:二轮复习
一、选择题
-
1. 下列化学用语或图示表示正确的是( )A、的VSEPR模型:
 B、的电子式:
B、的电子式: C、Cl的原子结构示意图:
C、Cl的原子结构示意图: D、溶于水的电离方程式:
2. 下列离子在溶液中能大量共存的是( )A、 B、 C、 D、3. 下列离子方程式正确的是( )A、HCO3-的水解反应:HCO3-+ H2O=H3O++ CO32- B、CaCO3与醋酸反应:CaCO3+ 2H+ =Ca2++ CO2↑+ H2O C、FeO与硝酸反应:FeO+ 2H+ 一 Fe2++H2O D、苯酚钠水溶液中通入少量CO2气体:
D、溶于水的电离方程式:
2. 下列离子在溶液中能大量共存的是( )A、 B、 C、 D、3. 下列离子方程式正确的是( )A、HCO3-的水解反应:HCO3-+ H2O=H3O++ CO32- B、CaCO3与醋酸反应:CaCO3+ 2H+ =Ca2++ CO2↑+ H2O C、FeO与硝酸反应:FeO+ 2H+ 一 Fe2++H2O D、苯酚钠水溶液中通入少量CO2气体: 4. 阅读下列材料,完成下列小题.
4. 阅读下列材料,完成下列小题.氨是其他含氮化合物的生产原料.氨可在氧气中燃烧生成N2。金属钠的液氨溶液放置时缓慢放出气体,同时生成NaNH2 , NaNH2遇水转化为NaOH。Cu(OH)2溶于氨水得到深蓝色溶液,加入稀硫酸又转化为蓝色溶液。氨可以发生类似于水解反应的氨解反应,浓氨水与溶液反应生成沉淀。
(1)、下列有关反应的化学方程式错误的是( )A、氨在氧气中燃烧: B、液氨与金属钠反应: C、氨水溶解: D、浓氨水与HgCl2反应:(2)、下列有关物质结构或性质的比较中,正确的是( )A、与 结合的能力: B、与氨形成配位键的能力: C、H2O和分子中的键长:O-H>N-H D、微粒所含电子数:5. 室温下,有色金属冶炼废渣(含等的氧化物)用过量的较浓溶液酸浸后,提取铜和镍的过程如下所示。
已知:。下列说法正确的是( )
A、较浓溶液中: B、溶液中:的平衡常数 C、溶液中: D、“提铜”和“沉镍”后的两份滤液中:6. 下列实验产生的废液中,可能大量存在的粒子组是( )选项
实验
化学知识
A
稀硝酸与铜片制NO
H+、Cu2+、NO3-、NO
B
70%硫酸与Na2SOз制 SO3
H+、Na+、SO42-、HSO3-
C
浓盐酸与KMnO4制Cl2
H+、K+、Mn2+、Cl-
D
双氧水与FeCl3溶液制O2
H+、Fe2+、Cl-、H2O2
A、A B、B C、C D、D7. 微粒邂逅时的色彩变化是化学馈赠的视觉浪漫。下列对颜色变化的解释错误的是( )选项
颜色变化
解释
A
空气中灼烧过的铜丝伸入乙醇中,黑色铜丝恢复光亮的紫红色
=
B
悬浊液中加入溶液,固体由白色变为红褐色
=
C
溶液中加入 , 浅绿色溶液出现蓝色浑浊
=
D
溶液中加入NaOH溶液,溶液由橙色变为黄色
A、A B、B C、C D、D8. 兴趣小组设计了从中提取的实验方案,下列说法正确的是( ) A、还原性: B、按上述方案消耗可回收 C、反应①的离子方程式是 D、溶液①中的金属离子是9. 阅读下列材料,完成问题:
A、还原性: B、按上述方案消耗可回收 C、反应①的离子方程式是 D、溶液①中的金属离子是9. 阅读下列材料,完成问题:倠化剂能改变化学反应速率而不改变反应的焓变,常见倠化剂有金属及其氧化物、酸和碱等.倠化反应广泛存在,如豆科植物固氮、石墨制金刚石、和制(二甲醚)、倠化氧化等.催化剂有选择性,如与反应用Ag催化生成
 (环氧乙烷)、用催化生成 . 催化作用能消除污染和影响环境,如汽车尾气处理、废水中电倠化生成、氯自由基催化分解形成臭氧空洞.我国在石油催化领域领先世界,高效、经济、绿色是未来催化剂研究的发展方向.(1)、下列说法正确的是( )A、豆科植物固氮过程中,固氮酶能提高该反应的活化能 B、与反应中,Ag催化能提高生成的选择性 C、制反应中,能加快化学反应速率 D、与反应中,能减小该反应的焓变(2)、下列化学反应表示正确的是( )A、汽车尾气处理: B、电催化为的阳极反应: C、硝酸工业中的氧化反应: D、和催化制二甲醚:(3)、下列有关反应描述正确的是( )A、催化氧化为 , 断裂键 B、氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变分解的历程 C、丁烷催化裂化为乙烷和乙烯,丁烷断裂键和键 D、石墨转化为金刚石,碳原子轨道的杂化类型由转变为10. 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )
(环氧乙烷)、用催化生成 . 催化作用能消除污染和影响环境,如汽车尾气处理、废水中电倠化生成、氯自由基催化分解形成臭氧空洞.我国在石油催化领域领先世界,高效、经济、绿色是未来催化剂研究的发展方向.(1)、下列说法正确的是( )A、豆科植物固氮过程中,固氮酶能提高该反应的活化能 B、与反应中,Ag催化能提高生成的选择性 C、制反应中,能加快化学反应速率 D、与反应中,能减小该反应的焓变(2)、下列化学反应表示正确的是( )A、汽车尾气处理: B、电催化为的阳极反应: C、硝酸工业中的氧化反应: D、和催化制二甲醚:(3)、下列有关反应描述正确的是( )A、催化氧化为 , 断裂键 B、氟氯烃破坏臭氧层,氟氯烃产生的氯自由基改变分解的历程 C、丁烷催化裂化为乙烷和乙烯,丁烷断裂键和键 D、石墨转化为金刚石,碳原子轨道的杂化类型由转变为10. 下列陈述Ⅰ与陈述Ⅱ均正确,且具有因果关系的是( )选项
陈述Ⅰ
陈述Ⅱ
A
将浓硫酸加入蔗糖中形成多孔炭
浓硫酸具有氧化性和脱水性
B
装有的密闭烧瓶冷却后颜色变浅
转化为的反应吸热
C
久置空气中的漂白粉遇盐酸产生
漂白粉的有效成分是
D
溶液导电性比同浓度醋酸强
溶液的比醋酸的高
A、A B、B C、C D、D11. 甘氨酸是人体必需氨基酸之一、在时,、和的分布分数【如】与溶液关系如图。下列说法错误的是( )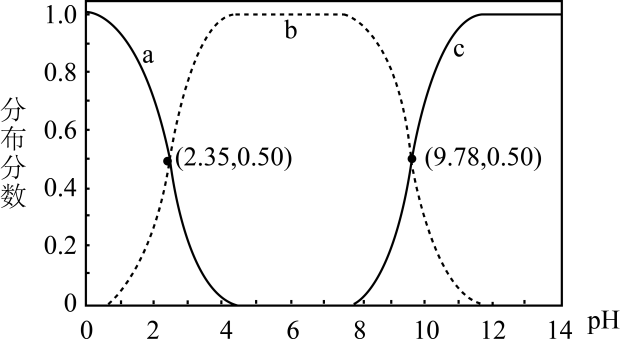 A、甘氨酸具有两性 B、曲线c代表 C、的平衡常数 D、12. CuCl微溶于水,但在浓度较高的溶液中因形成和而溶解。将适量CuCl完全溶于盐酸,得到含和的溶液,下列叙述正确的是A、加水稀释,浓度一定下降 B、向溶液中加入少量NaCl固体,浓度一定上升 C、的电离方程式为: D、体系中,13. 某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合要求的是( )
A、甘氨酸具有两性 B、曲线c代表 C、的平衡常数 D、12. CuCl微溶于水,但在浓度较高的溶液中因形成和而溶解。将适量CuCl完全溶于盐酸,得到含和的溶液,下列叙述正确的是A、加水稀释,浓度一定下降 B、向溶液中加入少量NaCl固体,浓度一定上升 C、的电离方程式为: D、体系中,13. 某同学按图示装置进行实验,欲使瓶中少量固体粉末最终消失并得到澄清溶液。下列物质组合不符合要求的是( )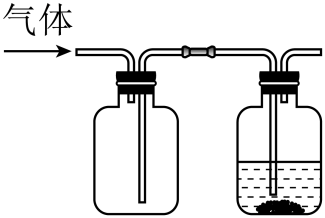
气体
液体
固体粉末
A
饱和溶液
B
溶液
Fe
C
溶液
D
A、A B、B C、C D、D14. 某同学在两个相同的特制容器中分别加入20mL0.4mol·L-1Na2CO3溶液和40mL0.2mol·L-1NaHCO3溶液,再分别用0.4mol·L-1盐酸滴定,利用pH计和压力传感器检测,得到如图曲线:
下列说法正确的的是( )
A、图中甲、丁线表示向NaHCO3溶液中滴加盐酸,乙、丙线表示向Na2CO3溶液中滴加盐酸 B、当滴加盐酸的体积为V1mL时(a点、b点),所发生的反应用离子方程式表示为:HCO+H+=CO2↑+H2O C、根据pH—V(HCl)图,滴定分析时,c点可用酚酞、d点可用甲基橙作指示剂指示滴定终点 D、Na2CO3和NaHCO3溶液中均满足:c(H2CO3)-c(CO)=c(OH-)-c(H+)二、实验探究题
-
15.
学习小组为探究、能否催化的分解及相关性质,室温下进行了实验I~Ⅳ。
实验I
实验Ⅱ
实验Ⅲ



无明显变化
溶液变为红色,伴有气泡产生
溶液变为墨绿色,并持续产生能使带火星木条复燃的气体
已知:为粉红色、为蓝色、为红色、为墨绿色。回答下列问题:
(1)配制的溶液,需要用到下列仪器中的(填标号)。
a.
 b.
b.  c.
c.  d.
d.
(2)实验I表明(填“能”或“不能”)催化的分解。实验Ⅱ中大大过量的原因是。实验Ⅲ初步表明能催化的分解,写出在实验Ⅲ中所发生反应的离子方程式、。
(3)实验I表明,反应难以正向进行,利用化学平衡移动原理,分析、分别与配位后,正向反应能够进行的原因。
实验Ⅳ:

(4)实验Ⅳ中,A到B溶液变为蓝色,并产生气体;B到C溶液变为粉红色,并产生气体。从A到C所产生的气体的分子式分别为、。
三、解答题
-
16. 矿物资源的综合利用有多种方法,如铅锌矿(主要成分为PbS、ZnS)的利用有火法和电解法等。


已知:①PbCl2(s) PbCl2(aq)H2[PbCl4];
②电解前后ZnS总量不变;③AgF易溶于水。
请回答:
(1)、根据富氧煅烧(在空气流中煅烧)和通电电解(如图)的结果,PbS中硫元素体现的性质是(选填“氧化性”、“还原性”、“酸性”、“热稳定性”之一)。产物B中有少量Pb3O4 , 该物质可溶于浓盐酸,Pb元素转化为[PbCl4]2− , 写出该反应的化学方程式;从该反应液中提取PbCl2的步骤如下:加热条件下,加入(填一种反应试剂),充分反应,趁热过滤,冷却结晶,得到产品。(2)、下列说法正确的是____。A、电解池中发生的总反应是PbS=Pb+S(条件省略) B、产物B主要是铅氧化物与锌氧化物 C、1mol化合物C在水溶液中最多可中和2mol NaOH D、ClF的氧化性弱于Cl2(3)、D的结构为HO--X(X=F或Cl),设计实验先除去样品D中的硫元素,再用除去硫元素后的溶液探究X为何种元素。①实验方案:取D的溶液,加入足量NaOH溶液,加热充分反应,然后;
②写出D(用HSO3X表示)的溶液与足量NaOH溶液反应的离子方程式。
17. Fe3O4是一种用途广泛的磁性材料,以FeCl2为原料制备Fe3O4并获得副产物CaCl2水合物的工艺如图。
25℃时各物质溶度积见表:
物质
Fe(OH)2
Fe(OH)3
Ca(OH)2
溶度积(Ksp)
4.9×10﹣17
2.8×10﹣39
5.0×10﹣6
回答下列问题:
(1)、Fe3O4中Fe元素的化合价是+2和 。O2﹣的核外电子排布式为 。(2)、反应釜1中的反应需在隔绝空气条件下进行,其原因是 。(3)、反应釜2中,加入CaO和分散剂的同时通入空气。①反应的离子方程式为 。
②为加快反应速率,可采取的措施有 (写出两项即可)。
(4)、①反应釜3中,25℃时,Ca2+浓度为5.0mol/L,理论上pH不超过 。②称取CaCl2水合物1.000g,加水溶解,加入过量Na2C2O4 , 将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用0.1000mol/LKMnO4标准溶液滴定,消耗24.00mL。滴定达到终点的现象为 , 该副产物中CaCl2的质量分数为 。
18. 含硫化合物是实验室和工业上的常用化学品。请回答:(1)、实验室可用铜与浓硫酸反应制备少量 : 。判断该反应的自发性并说明理由。(2)、已知 。 时,在一恒容密闭反应器中充入一定量的 和 ,当反应达到平衡后测得 、 和 的浓度分别为 、 和 。①该温度下反应的平衡常数为。
②平衡时 的转化率为。
(3)、工业上主要采用接触法由含硫矿石制备硫酸。①下列说法正确的是。
A.须采用高温高压的反应条件使 氧化为
B.进入接触室之前的气流无需净化处理
C.通入过量的空气可以提高含硫矿石和 的转化率
D.在吸收塔中宜采用水或稀硫酸吸收 以提高吸收速率
②接触室结构如图1所示,其中1~4表示催化剂层。图2所示进程中表示热交换过程的是。
A. B. C. D. E. F. G.

③对于放热的可逆反应,某一给定转化率下,最大反应速率对应的温度称为最适宜温度。在图3中画出反应 的转化率与最适宜温度(曲线Ⅰ)、平衡转化率与温度(曲线Ⅱ)的关系曲线示意图(标明曲线Ⅰ、Ⅱ)。
 (4)、一定条件下,在 溶液体系中,检测得到pH-时间振荡曲线如图4,同时观察到体系由澄清→浑浊→澄清的周期性变化。可用一组离子方程式表示每一个周期内的反应进程,请补充其中的2个离子方程式。
(4)、一定条件下,在 溶液体系中,检测得到pH-时间振荡曲线如图4,同时观察到体系由澄清→浑浊→澄清的周期性变化。可用一组离子方程式表示每一个周期内的反应进程,请补充其中的2个离子方程式。
Ⅰ.
Ⅱ.①;
Ⅲ. ;
Ⅳ.②。
19. 聚合氯化铝用于城市给排水净化。氧化铝法制取无水三氯化铝的反应如下:Al2O3(s)+3C(s)+3Cl2(g) 2AlCl3(g)+3CO(g)。 (1)、标出上述反应的电子转移方向和数目 。(2)、写出该反应的平衡常数表达式:K=。(3)、Al原子核外有 种不同能量的电子。
2AlCl3(g)+3CO(g)。 (1)、标出上述反应的电子转移方向和数目 。(2)、写出该反应的平衡常数表达式:K=。(3)、Al原子核外有 种不同能量的电子。聚合氯化铝(PAC)是一种介于AlCl3和Al(OH)3之间的水溶性无机高分子聚合物,PAC的水解过程中会有一种聚合稳定态物质[AlO4Al12(OH)24(H2O)12]7+称为Al13 , Al13对水中胶体和颗粒物具有高度电中和桥联作用,是净水过程中的重要物质。
(4)、Al13在水解过程中会产生[Al(OH)2]+、[Al(OH)]2+等产物,请写出Al3+水解产生[Al(OH)]2+的离子方程式:。(5)、AlCl3溶液与NaOH溶液反应,若参加反应的铝离子最终转化生成Al13 , 则理论上参与反应的Al3+与OH﹣的物质的量之比是 。(6)、使用Al3+净水时应控制pH在6.8~8.02之间,否则净水效果不佳。请结合使用Al3+水解净化水时铝元素存在的形态,分析在强酸性和强碱性环境时净水效果差的原因 。20. 氢气是一种清洁能源,绿色环保制氢技术研究具有重要意义。(1)、“热电循环制氢”经过溶解、电解、热水解和热分解4个步骤,其过程如图所示。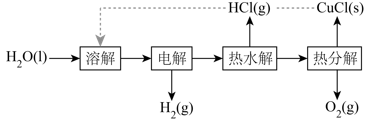
①电解在质子交换膜电解池中进行。阳极区为酸性溶液,阴极区为盐酸,电解过程中转化为。电解时阳极发生的主要电极反应为(用电极反应式表示)。
②电解后,经热水解和热分解的物质可循环使用。在热水解和热分解过程中,发生化合价变化的元素有(填元素符号)。
(2)、“热循环制氢和甲酸”的原理为:在密闭容器中,铁粉与吸收制得的溶液反应,生成、和;再经生物柴油副产品转化为Fe。①实验中发现,在时,密闭容器中溶液与铁粉反应,反应初期有生成并放出 , 该反应的离子方程式为。
②随着反应进行,迅速转化为活性 , 活性是转化为的催化剂,其可能反应机理如图所示。根据元素电负性的变化规律。如图所示的反应步骤Ⅰ可描述为。

③在其他条件相同时,测得Fe的转化率、的产率随变化如题图所示。的产率随增加而增大的可能原因是。
 (3)、从物质转化与资源综合利用角度分析,“热循环制氢和甲酸”的优点是。
(3)、从物质转化与资源综合利用角度分析,“热循环制氢和甲酸”的优点是。四、流程题
-
21. 工业上以氟磷灰石[ , 含等杂质]为原料生产磷酸和石膏,工艺流程如下:

回答下列问题:
(1)、酸解时有产生。氢氟酸与反应生成二元强酸 , 离子方程式为。(2)、部分盐的溶度积常数见下表。精制Ⅰ中,按物质的量之比加入脱氟,充分反应后,;再分批加入一定量的 , 首先转化为沉淀的离子是。(3)、浓度(以计)在一定范围时,石膏存在形式与温度、浓度(以计)的关系如图甲所示。酸解后,在所得、为45的混合体系中,石膏存在形式为(填化学式);洗涤时使用一定浓度的硫酸溶液而不使用水,原因是 , 回收利用洗涤液X的操作单元是;一定温度下,石膏存在形式与溶液中和的关系如图乙所示,下列条件能实现酸解所得石膏结晶转化的是(填标号)。
A.、、 B.、、
C.、、 D.、、
22. 盐湖卤水(主要含、和硼酸根等)是锂盐的重要来源。一种以高镁卤水为原料经两段除镁制备的工艺流程如下: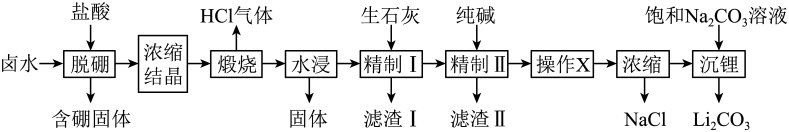
已知:常温下,。相关化合物的溶解度与温度的关系如图所示。

回答下列问题:
(1)、含硼固体中的在水中存在平衡:(常温下,);与溶液反应可制备硼砂。常温下,在硼砂溶液中,水解生成等物质的量浓度的和 , 该水解反应的离子方程式为 , 该溶液。(2)、滤渣Ⅰ的主要成分是(填化学式);精制Ⅰ后溶液中的浓度为 , 则常温下精制Ⅱ过程中浓度应控制在以下。若脱硼后直接进行精制Ⅰ,除无法回收外,还将增加的用量(填化学式)。(3)、精制Ⅱ的目的是;进行操作时应选择的试剂是 , 若不进行该操作而直接浓缩,将导致。23. 均是重要的战略性金属。从处理后的矿石硝酸浸取液(含)中,利用氨浸工艺可提取 , 并获得高附加值化工产品。工艺流程如下: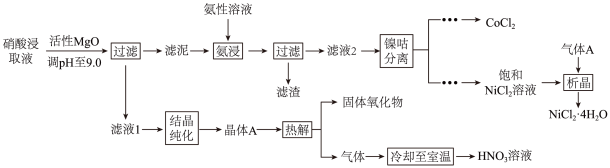
已知:氨性溶液由、和配制。常温下,与形成可溶于水的配离子:;易被空气氧化为;部分氢氧化物的如下表。
氢氧化物
回答下列问题:
(1)、活性可与水反应,化学方程式为。(2)、常温下,的氨性溶液中, (填“>”“<”或“=”)。(3)、“氨浸”时,由转化为的离子方程式为。(4)、会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物。滤渣的X射线衍射图谱中,出现了的明锐衍射峰。①属于(填“晶体”或“非晶体”)。
②提高了的浸取速率,其原因是。
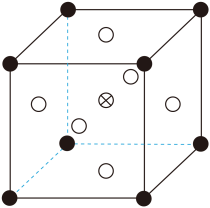
(5)、①“析晶”过程中通入的酸性气体A为。②由可制备晶体,其立方晶胞如图。与O最小间距大于与O最小间距,x、y为整数,则在晶胞中的位置为;晶体中一个周围与其最近的O的个数为。
 (6)、①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得溶液中与的比值,理论上最高为。
(6)、①“结晶纯化”过程中,没有引入新物质。晶体A含6个结晶水,则所得溶液中与的比值,理论上最高为。②“热解”对于从矿石提取工艺的意义,在于可重复利用和(填化学式)。
-