2026年中考化学第一轮复习学案:第1讲 水和溶液
试卷更新日期:2026-03-16 类型:复习试卷
一、
-
1. 流溪河是城市饮用水的重要来源。下列说法正确的是( )A、过滤能使河水变成纯净水 B、加入絮凝剂明矾能进行杀菌消毒 C、河水中没有氧气 D、电解水得到的氧气和氢气的体积比是1:22. 水是重要和不可替代的生命源泉。下列对水的认识错误的是A、采取有效措施降低水资源消耗 B、明矾可用于吸附水中悬浮杂质 C、废水、污水均须处理,不能直接排放 D、活性炭用于自来水杀菌消毒3. 小华通过微信公众号“胜哥课程”观看了《电解水的微观解释》化学视频,对相关知识有了深刻的理解。电解水的实验如图所示,以下说法正确的是( )
 A、a、b管内气体质量比约为 B、a管内产生的气体是氢气 C、该实验说明水由氢元素和氧元素组成 D、反应前后元素种类可能发生改变4. “胜哥”在班级内布置了一项以“水”为主题的实践探究活动。下列表述不正确的是( )
A、a、b管内气体质量比约为 B、a管内产生的气体是氢气 C、该实验说明水由氢元素和氧元素组成 D、反应前后元素种类可能发生改变4. “胜哥”在班级内布置了一项以“水”为主题的实践探究活动。下列表述不正确的是( ) A、试管a收集的气体是氢气 B、试管b收集的气体可用于炼钢、气焊等 C、电解水和水蒸发都属于化学变化 D、电解水的微观实质是分子分成原子,原子重新组合成新的分子5. 小华同学通过视频号“胜哥课程”观看了相关视频后,对“水是一切生命赖以生存的根本”有了深刻的理解。下列说法不正确的是( )A、自然界中的水都是纯水 B、生活污水应集中处理排放 C、肥皂遇到硬水易起浮渣 D、生活中可以软化硬水的方法是煮沸6. 2025年3月22日是第三十三届“世界水日”,3月22—28日是第三十八届“中国水周”。联合国2025年“世界水日”主题定为“冰川保护”。下列措施或做法符合该主题的是( )A、洗手接洗手液时不关水龙头 B、工业用水不重复利用 C、园林浇灌采用大水浸灌 D、生活提倡“一水多用”7. 下列溶液中水不是溶剂的是A、稀硫酸 B、医用酒精 C、硫酸铜溶液 D、碘酒溶液8. 下列有关溶液的说法正确的是A、具有均一性、稳定性的液体一定是溶液 B、溶液中溶质只能是固体或者液体,不能是气体 C、某物质的饱和溶液在温度不改变的情况下不能再溶解其他物质 D、硝酸铵在水中溶解时,溶液的温度降低9. 下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
A、试管a收集的气体是氢气 B、试管b收集的气体可用于炼钢、气焊等 C、电解水和水蒸发都属于化学变化 D、电解水的微观实质是分子分成原子,原子重新组合成新的分子5. 小华同学通过视频号“胜哥课程”观看了相关视频后,对“水是一切生命赖以生存的根本”有了深刻的理解。下列说法不正确的是( )A、自然界中的水都是纯水 B、生活污水应集中处理排放 C、肥皂遇到硬水易起浮渣 D、生活中可以软化硬水的方法是煮沸6. 2025年3月22日是第三十三届“世界水日”,3月22—28日是第三十八届“中国水周”。联合国2025年“世界水日”主题定为“冰川保护”。下列措施或做法符合该主题的是( )A、洗手接洗手液时不关水龙头 B、工业用水不重复利用 C、园林浇灌采用大水浸灌 D、生活提倡“一水多用”7. 下列溶液中水不是溶剂的是A、稀硫酸 B、医用酒精 C、硫酸铜溶液 D、碘酒溶液8. 下列有关溶液的说法正确的是A、具有均一性、稳定性的液体一定是溶液 B、溶液中溶质只能是固体或者液体,不能是气体 C、某物质的饱和溶液在温度不改变的情况下不能再溶解其他物质 D、硝酸铵在水中溶解时,溶液的温度降低9. 下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( ) A、t2℃时,在甲、乙两种溶液中,溶质甲的质量一定大于乙 B、t1℃时,甲、乙两种物质的溶解度都是50g C、t2℃时,将甲的饱和溶液降温至t1℃,其溶质的质量分数减小 D、甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯甲10. “侯氏联合制碱法”生产过程涉及到Na2CO3、NH4Cl、NaCl等物质,其溶解度曲线如下图所示,下列说法正确的是
A、t2℃时,在甲、乙两种溶液中,溶质甲的质量一定大于乙 B、t1℃时,甲、乙两种物质的溶解度都是50g C、t2℃时,将甲的饱和溶液降温至t1℃,其溶质的质量分数减小 D、甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯甲10. “侯氏联合制碱法”生产过程涉及到Na2CO3、NH4Cl、NaCl等物质,其溶解度曲线如下图所示,下列说法正确的是 A、Na2CO3、NH4Cl、NaCl的溶解度均随温度升高而增大 B、除去NH4Cl中混有的少量NaCl,宜用降温结晶的方法 C、40℃时,将25克NH4Cl溶于50克水中形成不饱和溶液 D、40℃时,将Na2CO3溶液升温和降温都会降低溶液浓度11. 小华通过视频号“胜哥课程”观看了《盐水选种》视频,如图所示,“胜哥”配制了15%的溶液用于选种,部分操作如下,其中正确的是( )
A、Na2CO3、NH4Cl、NaCl的溶解度均随温度升高而增大 B、除去NH4Cl中混有的少量NaCl,宜用降温结晶的方法 C、40℃时,将25克NH4Cl溶于50克水中形成不饱和溶液 D、40℃时,将Na2CO3溶液升温和降温都会降低溶液浓度11. 小华通过视频号“胜哥课程”观看了《盐水选种》视频,如图所示,“胜哥”配制了15%的溶液用于选种,部分操作如下,其中正确的是( ) A、取用 B、称量 C、读取水的体积 D、溶解12. 除去中混有的细砂,并利用得到的固体配制溶液,实验过程如图所示:
A、取用 B、称量 C、读取水的体积 D、溶解12. 除去中混有的细砂,并利用得到的固体配制溶液,实验过程如图所示:除去细砂:混合物→溶解→步骤a→蒸发→装瓶贴标签
配制溶液:计算→称量→量取—→溶解→装瓶贴标签
下列说法中错误的是( )
A、步骤a为过滤 B、蒸发时,待蒸发皿内液体全部蒸干后撤去酒精灯 C、配制溶液时,需称量提纯后干燥的 D、量取水时,若俯视读数会导致溶质质量分数偏大13. 要使100克10%的食盐溶液的浓度增大一倍,下列做法正确的是A.蒸发45克的水 B.蒸发50克的水
C.加入200克20%的食盐溶液 D.加入克的食盐
14. 在60℃时,“胜哥”分别取X g氯化钠固体和X g硝酸钾固体进行图1的实验(图2是氯化钠、硝酸钾的溶解度曲线)。
(1)、加入甲烧杯中的固体是(选填“NaCl”或“”),X的取值范围是。(2)、下列说法错误的是。A.状态1时,甲烧杯为饱和溶液,乙烧杯为不饱和溶液
B.乙烧杯在状态2时的溶质质量分数是状态1时的2倍
C.若将状态1时的甲、乙烧杯溶液降温至10℃,所得溶液溶质质量分数甲>乙
15. 下列有关水和溶液的说法正确的是( )A、河水经静置、过滤后所得液体属于纯净物 B、电解水实验说明水由氢气和氧气组成 C、物质溶于水形成溶液时,溶质以分子或离子形式存在 D、均一、稳定的无色液体一定是溶液16. 2025年“世界水日”的主题是“冰川保护”。下列有关水的认识不正确的是( )A、水是一种重要的溶剂 B、水和冰是同一种物质 C、水是由氢分子和氧原子构成的 D、水的天然循环是通过其三态变化实现的17. 下列单一操作净化水程度较高的方法是( )A、沉降 B、过滤 C、吸附 D、蒸馏18. 我国首次将太阳能规模转化为液体燃料甲醇,又称“液态阳光”技术。其合成项目示意图如图所示,下列有关说法不正确的是( ) A、反应Ⅰ化学方程式为 B、反应Ⅱ中●●●和∞的分子个数比为1:1 C、生产48t甲醇,理论上可以吸收66t CO2 D、实现了CO2的资源化利用和“零碳”排放19. 下列对实验现象的解释正确的是( )
A、反应Ⅰ化学方程式为 B、反应Ⅱ中●●●和∞的分子个数比为1:1 C、生产48t甲醇,理论上可以吸收66t CO2 D、实现了CO2的资源化利用和“零碳”排放19. 下列对实验现象的解释正确的是( )选项
实验现象
解释
A
25℃下,向某蔗糖溶液中加入少量蔗糖,蔗糖逐渐消失
原溶液是25℃下蔗糖的饱和溶液
B
80t的NH4CI饱和溶液冷却至20℃时,有晶体析出
温度降低.NH4CI的溶解度增大
C
将铁丝浸人CuSO4溶液、·段时间后,铁丝表面有红色固体出现
Cu的金属活动性比 Fe强
D
将干冷的烧杯罩在蜡烛火焰上方,烧杯内有黑烟和水雾
蜡烛中含有碳元素、氢元素
A、A B、B C、C D、D20. 20℃时,用150g质量分数为15%的NaCI溶液进行如图所示的实验。
已知:20℃时,NaCl的溶解度为36g。
下列有关说法正确的是( )
A、烧杯①中NaCl的质量分数为5% B、烧杯②中溶剂的质量为60g C、烧杯③中NaCI的质量分数计算式可表示为 D、烧杯②③中溶液质量相等21. 某医用冷敷袋的内部结构如右下图。使用时挤压冷敷袋,内包装膜破裂,里面的水接触到夹层中的NH4NO3 , 温度降低。下列说法错误的是( ) A、用于制作外包装袋的塑料属于金属材料 B、与外包装袋相比,内包装膜更易破裂 C、NH4NO3溶于水时吸热使温度降低 D、运输、储存该医用冷敷袋时应防止挤压22. 我国某盐湖地区有“夏天晒盐(NaCl),冬天捞碱()”的说法。图1是NaCl和的溶解度曲线,下列说法正确的( )
A、用于制作外包装袋的塑料属于金属材料 B、与外包装袋相比,内包装膜更易破裂 C、NH4NO3溶于水时吸热使温度降低 D、运输、储存该医用冷敷袋时应防止挤压22. 我国某盐湖地区有“夏天晒盐(NaCl),冬天捞碱()”的说法。图1是NaCl和的溶解度曲线,下列说法正确的( ) A、的溶解度随温度的升高而增大 B、冬天捞“碱”,需要经过降温结晶的过程 C、晒“盐”捞“碱”后的溶液是不饱和溶液 D、室温下,向图2烧杯的水中加入硝酸铵固体,试管中无晶体析出23. T1℃时,分别向盛有10.0g水的甲、乙试管加入等质量的和固体,溶解情况如图所示。下列说法不正确的是( )
A、的溶解度随温度的升高而增大 B、冬天捞“碱”,需要经过降温结晶的过程 C、晒“盐”捞“碱”后的溶液是不饱和溶液 D、室温下,向图2烧杯的水中加入硝酸铵固体,试管中无晶体析出23. T1℃时,分别向盛有10.0g水的甲、乙试管加入等质量的和固体,溶解情况如图所示。下列说法不正确的是( ) A、甲试管中加入的固体是 B、乙试管中溶液的溶质质量分数小于或等于50.0% C、加热甲试管(忽略水分蒸发),溶液的溶质质量分数先变大后不变 D、将甲、乙试管分别升温至T2℃,为使溶液恰好饱和,加入固体的质量:甲<乙24. 取10 g某种固体物质R在不同温度下加水溶解,恰好溶解时所需水的质量随温度的变化如图所示,下列说法正确的是( )
A、甲试管中加入的固体是 B、乙试管中溶液的溶质质量分数小于或等于50.0% C、加热甲试管(忽略水分蒸发),溶液的溶质质量分数先变大后不变 D、将甲、乙试管分别升温至T2℃,为使溶液恰好饱和,加入固体的质量:甲<乙24. 取10 g某种固体物质R在不同温度下加水溶解,恰好溶解时所需水的质量随温度的变化如图所示,下列说法正确的是( ) A、R的溶解度随温度的升高而减小 B、时,R的溶解度为40 g C、时,R的饱和溶液中溶质的质量分数为25% D、时,将20 gR加入50g水中得到62.5 g溶液25. 向密闭玻璃瓶中装入硝酸钾、氯化铵、蒸馏水、樟脑和乙醇溶液,可制成“天气瓶”。硝酸钾和氯化铵的溶解度曲线如图。
A、R的溶解度随温度的升高而减小 B、时,R的溶解度为40 g C、时,R的饱和溶液中溶质的质量分数为25% D、时,将20 gR加入50g水中得到62.5 g溶液25. 向密闭玻璃瓶中装入硝酸钾、氯化铵、蒸馏水、樟脑和乙醇溶液,可制成“天气瓶”。硝酸钾和氯化铵的溶解度曲线如图。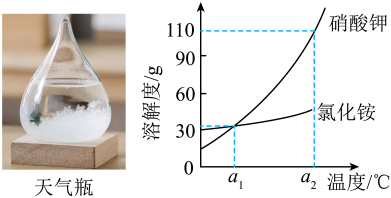
下列说法正确的是( )
A、a1℃时,硝酸钾和氯化铵溶液的溶质质量分数一定相等 B、a2℃时,向50g水中加入60g硝酸钾,充分溶解,可得到110g溶液 C、氯化铵溶液中混有少量的硝酸钾,可用降温结晶的方法提纯 D、a2℃时,等质量的硝酸钾和氯化铵饱和溶液降温至a1℃,析出晶体的质量:硝酸钾>氯化铵26. 《天工开物》记载的“淋煎”法制取海盐,主要包含“海水淋洗”和“卤水煎炼”两个环节。NaCl的溶解度曲线如图,下列说法正确的是( ) A、“海水淋洗”可以增大NaCl的溶解度 B、“卤水煎炼”是蒸发结晶的过程 C、20℃时,NaCl饱和溶液中溶质和溶液质量比为35.9:100 D、20℃时,将20gNaCl溶于50g水中得到不饱和溶液27. KNO3和NaCl的溶解度曲线如图所示。下列说法正确的是( )
A、“海水淋洗”可以增大NaCl的溶解度 B、“卤水煎炼”是蒸发结晶的过程 C、20℃时,NaCl饱和溶液中溶质和溶液质量比为35.9:100 D、20℃时,将20gNaCl溶于50g水中得到不饱和溶液27. KNO3和NaCl的溶解度曲线如图所示。下列说法正确的是( ) A、20℃时,向50g水中加入20g NaCl,充分搅拌后得到70g NaCl溶液 B、50℃时,100g KNO3饱和溶液中,含有85.5g KNO3 C、分别将t℃的KNO3和NaCl饱和溶液蒸发掉等质量的水,恢复至t℃,析出晶体质量相等 D、20℃时,分别将等质量的KNO3和NaCl饱和溶液升温至50℃,所得溶液中溶质的质量分数:KNO3溶液>NaCl溶液28. 用含质量分数为10%的KNO3(密度为1.2g/mL)浓溶液,加水稀释为含KNO30.03%(密度约为1g/mL)的水培生菜营养液。下列说法正确的是( )A、配制过程需要用到托盘天平、药匙等 B、浓溶液和稀释用水的体积比约为1:400 C、稀释时玻璃棒的作用是加速固体溶解 D、量取浓溶液后在量筒中完成配制过程29. 配制50g质量分数为6%的NaCl溶液,并用该溶液配制50g质量分数为3%的稀溶液,可能用到的仪器如图。下列说法正确的是( )
A、20℃时,向50g水中加入20g NaCl,充分搅拌后得到70g NaCl溶液 B、50℃时,100g KNO3饱和溶液中,含有85.5g KNO3 C、分别将t℃的KNO3和NaCl饱和溶液蒸发掉等质量的水,恢复至t℃,析出晶体质量相等 D、20℃时,分别将等质量的KNO3和NaCl饱和溶液升温至50℃,所得溶液中溶质的质量分数:KNO3溶液>NaCl溶液28. 用含质量分数为10%的KNO3(密度为1.2g/mL)浓溶液,加水稀释为含KNO30.03%(密度约为1g/mL)的水培生菜营养液。下列说法正确的是( )A、配制过程需要用到托盘天平、药匙等 B、浓溶液和稀释用水的体积比约为1:400 C、稀释时玻璃棒的作用是加速固体溶解 D、量取浓溶液后在量筒中完成配制过程29. 配制50g质量分数为6%的NaCl溶液,并用该溶液配制50g质量分数为3%的稀溶液,可能用到的仪器如图。下列说法正确的是( ) A、配制6%的溶液选择仪器①③⑤⑥ B、将NaCl固体倒入量筒中溶解 C、稀释时,用量筒量取48.5mL水 D、量取6%的溶液时仰视读数,所配稀溶液浓度偏大30. 实验室里配制一定溶质质量分数的氯化钠溶液,过程中不涉及的实验操作是( )A、用天平称量一定质量的氣化钠 B、用量筒量取所需体积的水 C、将氯化钠和水放入烧杯中进行搅拌溶解 D、将配好的氯化钠溶液倒入蒸发皿中进行蒸发31. 下列实验设计能达到实验目的的是( )
A、配制6%的溶液选择仪器①③⑤⑥ B、将NaCl固体倒入量筒中溶解 C、稀释时,用量筒量取48.5mL水 D、量取6%的溶液时仰视读数,所配稀溶液浓度偏大30. 实验室里配制一定溶质质量分数的氯化钠溶液,过程中不涉及的实验操作是( )A、用天平称量一定质量的氣化钠 B、用量筒量取所需体积的水 C、将氯化钠和水放入烧杯中进行搅拌溶解 D、将配好的氯化钠溶液倒入蒸发皿中进行蒸发31. 下列实验设计能达到实验目的的是( ) A、鉴别蔗糖和碱面,可分别加水溶解后测溶液导电性 B、除去铜片表面的氧化铜,可将铜片在空气中充分灼烧 C、判断酸碱恰好完全反应,可利用上图装置进行实验 D、检验二氧化碳,可将气体通入紫色石蕊溶液32. 处处留心皆学问。小博同学一家到度假村享受周末的温馨时光。(1)、繁星点点的夜晚,一家人围炉煮羊排,羊肉中富含的营养物质是。羊汤中各处味道相同,说明溶液具有性。(2)、小博畅饮一瓶汽水后连着打嗝,因为气体的溶解度与有关。(3)、小博发现炉火中的木柴是架空的,这样做的目的是。33. 我国化学家侯德榜为纯碱工业的发展做出了杰出贡献。将NH3、CO2通入饱和NaCI溶液,发生反应:NaCI+CO2+H2O +NH3 = NaHCO3+ NH4CI,过滤得到NaHCO3晶体,加热分解即制得纯碱。下图为NH4CI、NaCI、NaHCO3三种物质的溶解度曲线。
A、鉴别蔗糖和碱面,可分别加水溶解后测溶液导电性 B、除去铜片表面的氧化铜,可将铜片在空气中充分灼烧 C、判断酸碱恰好完全反应,可利用上图装置进行实验 D、检验二氧化碳,可将气体通入紫色石蕊溶液32. 处处留心皆学问。小博同学一家到度假村享受周末的温馨时光。(1)、繁星点点的夜晚,一家人围炉煮羊排,羊肉中富含的营养物质是。羊汤中各处味道相同,说明溶液具有性。(2)、小博畅饮一瓶汽水后连着打嗝,因为气体的溶解度与有关。(3)、小博发现炉火中的木柴是架空的,这样做的目的是。33. 我国化学家侯德榜为纯碱工业的发展做出了杰出贡献。将NH3、CO2通入饱和NaCI溶液,发生反应:NaCI+CO2+H2O +NH3 = NaHCO3+ NH4CI,过滤得到NaHCO3晶体,加热分解即制得纯碱。下图为NH4CI、NaCI、NaHCO3三种物质的溶解度曲线。 (1)、将等质量的NH4CI、NaCI、NaHCO3分别配成60℃时的饱和溶液,所需水的质量最大的是。(2)、充分反应后,NaHCO3晶体先从溶液中析出的原因是(3)、60℃时,60gNH4CI溶液中含10gNH4CI使该溶液达到饱和状态,至少需要加入NH4CI 的质量是。34. 我国某盐湖地区有“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”的说法。根据溶解度表和溶解度曲线回答下列问题:
(1)、将等质量的NH4CI、NaCI、NaHCO3分别配成60℃时的饱和溶液,所需水的质量最大的是。(2)、充分反应后,NaHCO3晶体先从溶液中析出的原因是(3)、60℃时,60gNH4CI溶液中含10gNH4CI使该溶液达到饱和状态,至少需要加入NH4CI 的质量是。34. 我国某盐湖地区有“夏天晒盐(NaCl),冬天捞碱(Na2CO3)”的说法。根据溶解度表和溶解度曲线回答下列问题:溶解度/g
温度/℃
0
10
20
30
40
氯化钠
35.7
35.8
36.0
36.3
36.6
碳酸钠
7.0
12.2
21.8
39.7
48.0
 (1)、表示NaCl的溶解度曲线的是(填“甲”或“乙”)。(2)、A点表示的意义是。(3)、夏天晒“盐”,需要经过(填“蒸发结晶”或“降温结晶”)的过程。析出晶体后的母液为NaCl的(填“饱和”或“不饱和”)溶液。(4)、某同学暑假旅游时,在该湖中取一瓶湖水,静置后取上层清液,完成图中实验,观察到瓶中有晶体析出,析出晶体后的湖水中一定含有的溶质是。
(1)、表示NaCl的溶解度曲线的是(填“甲”或“乙”)。(2)、A点表示的意义是。(3)、夏天晒“盐”,需要经过(填“蒸发结晶”或“降温结晶”)的过程。析出晶体后的母液为NaCl的(填“饱和”或“不饱和”)溶液。(4)、某同学暑假旅游时,在该湖中取一瓶湖水,静置后取上层清液,完成图中实验,观察到瓶中有晶体析出,析出晶体后的湖水中一定含有的溶质是。 35. 氯化钠和硝酸钾在不同温度时的溶解度如表,回答下列问题:
35. 氯化钠和硝酸钾在不同温度时的溶解度如表,回答下列问题:温度/℃
10
20
30
40
50
溶解度/g
氧化钠
35.8
36.0
36.3
36.6
37.0
硝酸钾
20.9
31.6
45.8
63.9
85.5
(1)、30℃时,氯化钠的溶解度为g。(2)、由表中数据分析,二者具有相同溶解度的温度范围是20℃<t<℃。(3)、40℃时,将20.0g氯化钠固体加入50.0g水中,充分溶解后所得溶液为溶液(填“饱和”或“不饱和”)。(4)、20℃时,向100.0g质量分数为12.0%的硝酸钾溶液中加入100g硝酸钾固体,充分溶解后,所得溶液中溶质的质量分数为。36. 化学实验是进行科学探究的重要方式。利用下列装置(部分夹持装置已略去)进行实验。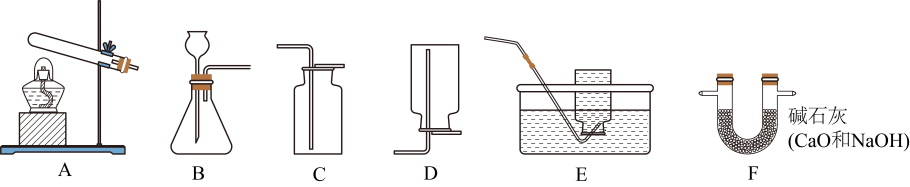
回答下列问题:
(1)、配制200g溶质质量分数为10%的过氧化氢溶液,需要取用溶质质量分数为30%的过氧化氢溶液的质量为g(结果精确至0.1g).(2)、用10%的过氧化氢溶液和二氧化锰制取一瓶干燥的O2 , 反应的化学方程式为 , 所选仪器的连接顺序为(按气流方向,用字母表示)。(3)、用坩埚钳夹取一块木炭,在酒精灯上加热至燃烧,再将其插入集满O2的集气瓶中,木炭燃烧更剧烈、发出白光、放出热量。由此实验可得出促进燃烧的方法为。燃烧停止后,为检验集气瓶中是否有CO2 , 需加入的试剂为。37. 正确的使用实验仪器和规范的操作是实验成功的重要前提和保障。请回答下列问题:(1)、固体试剂通常保存在(填仪器名称)里。(2)、胶头滴管使用后,未经清洗就吸取其他试剂,可能造成的后果是。(3)、用氯化钠固体和水配制50g溶质质量分数为6%的氯化钠溶液时,若量取水的体积时仰视读数,其它操作均正确,则所配制溶液的溶质质量分数(填“大于”、“等于”或“小于”)6%。(4)、“粗盐中难溶性杂质的去除”实验中,蒸发时用玻璃棒不断搅拌的目的是。当蒸发皿中出现时,停止加热。38. 黑火药是我国古代的四大发明之一,其成分含有。古代以硝土和草木灰(主要成分)为原料生产的部分流程如下图1所示。【查阅资料】①硝土的主要成分是、和NaCl等。
②与能发生复分解反应。
 (1)、淋硝过程中与反应的化学方程式是。淋硝所得的溶液称为“硝水”,其溶质中一定含有的物质是。(2)、熬硝主要是将淋硝过程中得到的硝水浓缩成浓硝水。根据图2中的溶解度曲线分析,冷却热浓硝水,主要获得晶体的原因是。若将80℃的269g硝酸钾饱和溶液降温到20℃,则析出硝酸钾晶体质量是g。(3)、滤液A可以循环使用,原因是。(4)、黑火药爆炸时发生反应的化学方程式是 , 则X的化学式是。39. 实验室里有一瓶久置氢氧化钠固体,为测定固体中是否含有碳酸钠,同学取干燥后固体4.52 g放入烧杯中,加入蒸馏水配成51.94 g溶液。向烧杯中逐滴加入氢氧化钡溶液,发现有白色沉淀生成,白色沉淀质量与加入氢氧化钡溶液的质量关系如图所示。回答下列问题。
(1)、淋硝过程中与反应的化学方程式是。淋硝所得的溶液称为“硝水”,其溶质中一定含有的物质是。(2)、熬硝主要是将淋硝过程中得到的硝水浓缩成浓硝水。根据图2中的溶解度曲线分析,冷却热浓硝水,主要获得晶体的原因是。若将80℃的269g硝酸钾饱和溶液降温到20℃,则析出硝酸钾晶体质量是g。(3)、滤液A可以循环使用,原因是。(4)、黑火药爆炸时发生反应的化学方程式是 , 则X的化学式是。39. 实验室里有一瓶久置氢氧化钠固体,为测定固体中是否含有碳酸钠,同学取干燥后固体4.52 g放入烧杯中,加入蒸馏水配成51.94 g溶液。向烧杯中逐滴加入氢氧化钡溶液,发现有白色沉淀生成,白色沉淀质量与加入氢氧化钡溶液的质量关系如图所示。回答下列问题。 (1)、氢氧化钠固体中(选填“是”或“否”)含有碳酸钠。(2)、恰好完全反应时,计算所得溶液中溶质的质量分数。(写出计算过程)40. 向一定质量的CuSO4 , 溶液中逐滴加入BaCl溶液.产生沉淀的质量与所加 BAC溶液的质量关系如右图所示。计算:
(1)、氢氧化钠固体中(选填“是”或“否”)含有碳酸钠。(2)、恰好完全反应时,计算所得溶液中溶质的质量分数。(写出计算过程)40. 向一定质量的CuSO4 , 溶液中逐滴加入BaCl溶液.产生沉淀的质量与所加 BAC溶液的质量关系如右图所示。计算: (1)、图中(填字母)点表示恰好完全反应。(2)、所加BaCl2溶液中溶质的质量分数。41. 小静同学通过课外阅读了解到过氧化钠(Na2O2)固体在常温下与水反应能产生氧气,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑。于是进行跨学科实践,设计了如图所示的便携式制氧器。矿泉水瓶中盛有39.0 g Na2O2 , 将输液袋中的369.0 g水全部滴入使Na2O2完全反应。完成下列计算:(1)、Na2O2中钠元素与氧元素的质量比为。(2)、计算产生氧气的质量;(3)、计算反应后所得溶液中溶质的质量分数。
(1)、图中(填字母)点表示恰好完全反应。(2)、所加BaCl2溶液中溶质的质量分数。41. 小静同学通过课外阅读了解到过氧化钠(Na2O2)固体在常温下与水反应能产生氧气,化学方程式为:2Na2O2+2H2O=4NaOH+O2↑。于是进行跨学科实践,设计了如图所示的便携式制氧器。矿泉水瓶中盛有39.0 g Na2O2 , 将输液袋中的369.0 g水全部滴入使Na2O2完全反应。完成下列计算:(1)、Na2O2中钠元素与氧元素的质量比为。(2)、计算产生氧气的质量;(3)、计算反应后所得溶液中溶质的质量分数。注:(2)和(3)要求写出简明的计算过程
