三年(2023-2025)中考科学真题分类汇编14 水和溶液
试卷更新日期:2026-03-03 类型:二轮复习
一、真题回顾
-
1. NH4Cl、KNO3是两种盐。30℃时,NHCl的溶解度为41.4g/100g水,KNO3的溶解度为45.8g/100g水。取这两种盐各22g,按图示进行实验。下列说法错误的是( )
 A、盐A是NH4Cl B、①中加足量的水可使未溶的盐A溶解 C、②中溶液为不饱和溶液 D、②中溶液溶质质量分数为45.8%2. 20℃时,在盛有50克水的烧杯中加入20克硝酸钾,充分搅拌后如图甲;加入20克水,充分搅拌后如图乙。再加入10克水如图丙。下列说法正确的是( )
A、盐A是NH4Cl B、①中加足量的水可使未溶的盐A溶解 C、②中溶液为不饱和溶液 D、②中溶液溶质质量分数为45.8%2. 20℃时,在盛有50克水的烧杯中加入20克硝酸钾,充分搅拌后如图甲;加入20克水,充分搅拌后如图乙。再加入10克水如图丙。下列说法正确的是( ) A、甲中溶液是不饱和溶液 B、乙中溶液一定是饱和溶液 C、丙中溶液的溶质质量分数为20% D、乙→丙过程中,溶液的溶质质量分数变大3. 实验规范操作是实验成功的关键。粗盐提纯实验中,下列实验操作正确的是( )A、
A、甲中溶液是不饱和溶液 B、乙中溶液一定是饱和溶液 C、丙中溶液的溶质质量分数为20% D、乙→丙过程中,溶液的溶质质量分数变大3. 实验规范操作是实验成功的关键。粗盐提纯实验中,下列实验操作正确的是( )A、 称量
B、
称量
B、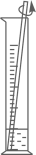 溶解
C、
溶解
C、 过滤
D、
过滤
D、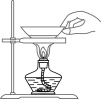 蒸发
4. 已知氯化钾的溶解度随温度升高而增大。向盛有40克氯化钾的烧杯中加入100克水,充分搅拌溶解后现象如图所示。此时溶液温度为20℃,下列说法正确的是( )
蒸发
4. 已知氯化钾的溶解度随温度升高而增大。向盛有40克氯化钾的烧杯中加入100克水,充分搅拌溶解后现象如图所示。此时溶液温度为20℃,下列说法正确的是( ) A、20℃时氯化钾的溶解度为40克 B、烧杯中氯化钾溶液的质量为140克 C、若加热使烧杯中的固体全部溶解,则溶质的质量分数一定比加热前大 D、若加水使烧杯中的固体全部溶解,则溶质的质量分数一定比加水前大5. 分布在地球各处的水处于不断运动和相互转化之中。如图为部分水循环的示意图,下列有关水循环说法正确的是( )
A、20℃时氯化钾的溶解度为40克 B、烧杯中氯化钾溶液的质量为140克 C、若加热使烧杯中的固体全部溶解,则溶质的质量分数一定比加热前大 D、若加水使烧杯中的固体全部溶解,则溶质的质量分数一定比加水前大5. 分布在地球各处的水处于不断运动和相互转化之中。如图为部分水循环的示意图,下列有关水循环说法正确的是( ) A、图中环节②代表水汽输送,环节③代表降水 B、水会不断地循环,无需提倡节约用水 C、地球上的水,大部分以气态形式存在于大气中 D、水循环中,水仅在固液两态之间相互转化6. 透水砖是一种绿色环保建材,透水性好。如图所示,用透水砖替代传统的混凝土路面砖,有效减少了地面积水。从水循环的过程分析,道路铺设透水砖主要有利于( )
A、图中环节②代表水汽输送,环节③代表降水 B、水会不断地循环,无需提倡节约用水 C、地球上的水,大部分以气态形式存在于大气中 D、水循环中,水仅在固液两态之间相互转化6. 透水砖是一种绿色环保建材,透水性好。如图所示,用透水砖替代传统的混凝土路面砖,有效减少了地面积水。从水循环的过程分析,道路铺设透水砖主要有利于( ) A、水汽输送 B、降水 C、下渗 D、地表径流7. 为拓展能量来源,我国推广种植一种“生物柴油”树——麻疯树,其果实内含有果仁油。果仁油常用有机溶剂通过浸取法提取,主要过程如图。下列有关说法错误的是( )
A、水汽输送 B、降水 C、下渗 D、地表径流7. 为拓展能量来源,我国推广种植一种“生物柴油”树——麻疯树,其果实内含有果仁油。果仁油常用有机溶剂通过浸取法提取,主要过程如图。下列有关说法错误的是( ) A、粉碎果仁能加快果仁油的溶解速度 B、加热溶解时温度升高果仁油溶解度变大 C、过滤利用了果仁油与滤渣的溶解性不同 D、蒸发过程中果仁油的溶质质量分数变小8. 许多物质都能溶解在溶剂里形成溶液,溶液在日常生活和生产中的应用广泛。下列说法错误的是( )A、溶液由溶质和溶剂组成,水是一种较好的溶剂 B、海水晒盐的过程可以实现溶剂和溶质的分离 C、两种不同溶液混合后,有可能形成悬浊液 D、凡是均一、稳定、透明的液体都是溶液9. 20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。下列有关所得溶液的说法,错误的是( )A、该溶液是饱和溶液 B、溶液中 Na+和Cl-个数一定相等 C、溶液的质量为100克 D、溶质与溶剂的质量比为9:2510. 海水中含有氯化钠、氯化镁等可溶性物质和少量细小泥沙颗粒。海水晒盐是获取食盐的途径之一,某同学模拟海水晒盐的部分实验流程如图所示。
A、粉碎果仁能加快果仁油的溶解速度 B、加热溶解时温度升高果仁油溶解度变大 C、过滤利用了果仁油与滤渣的溶解性不同 D、蒸发过程中果仁油的溶质质量分数变小8. 许多物质都能溶解在溶剂里形成溶液,溶液在日常生活和生产中的应用广泛。下列说法错误的是( )A、溶液由溶质和溶剂组成,水是一种较好的溶剂 B、海水晒盐的过程可以实现溶剂和溶质的分离 C、两种不同溶液混合后,有可能形成悬浊液 D、凡是均一、稳定、透明的液体都是溶液9. 20℃时,把36克氯化钠放入64克水中,使其充分溶解(20℃时氯化钠的溶解度为36克)。下列有关所得溶液的说法,错误的是( )A、该溶液是饱和溶液 B、溶液中 Na+和Cl-个数一定相等 C、溶液的质量为100克 D、溶质与溶剂的质量比为9:2510. 海水中含有氯化钠、氯化镁等可溶性物质和少量细小泥沙颗粒。海水晒盐是获取食盐的途径之一,某同学模拟海水晒盐的部分实验流程如图所示。 (1)、按照物质的组成分类,海水属于。(2)、滤液中氯化镁的质量分数(填“大于”“等于”或“小于”)其在海水中的质量分数。(3)、粗盐还需进一步提纯,将下列操作合理排序(填序号)。
(1)、按照物质的组成分类,海水属于。(2)、滤液中氯化镁的质量分数(填“大于”“等于”或“小于”)其在海水中的质量分数。(3)、粗盐还需进一步提纯,将下列操作合理排序(填序号)。①溶解②蒸发结晶③过滤
11. 在配制硝酸钾(KNO3)营养液时,小敏操作过程如图所示,请回答下列问题:
硝酸钾在不同温度时的溶解度
温度/℃
20
30
40
50
溶解度/克
31.6
45.8
63.9
85.5
(1)、硝酸钾能为农作物的生长提供养料,属于(选填”钾”、“氨”或”复合”)肥。(2)、上述溶液中属于饱和溶液的是 (填序号)。(3)、现要配制20%的硝酸钾营养液,需向烧杯③溶液中加水 克。12. 20℃时,取一定量CuSO4固体溶解在水中,按如图所示进行操作。回答下列问题: (1)、甲、乙、丙三种溶液,一定属于饱和溶液的是;(2)、甲、乙、丙三种溶液的溶质质量分数从大到小依次为。13. 织物处理工艺中蕴含着很多的科学知识。请回答:(1)、古法工艺:采用贝壳灼烧而成的灰烬(主要成分CaO)和草木灰(含K2CO3)在水中浸泡并不断搅拌,得到强碱性溶液,用于织物的处理。浸泡获取强碱性溶液时,发生的化学反应有:Ⅰ.CaO+H2O=Ca(OH)2;Ⅱ.K2CO3+Ca(OH)2=CaCO3↓+2KOH。
(1)、甲、乙、丙三种溶液,一定属于饱和溶液的是;(2)、甲、乙、丙三种溶液的溶质质量分数从大到小依次为。13. 织物处理工艺中蕴含着很多的科学知识。请回答:(1)、古法工艺:采用贝壳灼烧而成的灰烬(主要成分CaO)和草木灰(含K2CO3)在水中浸泡并不断搅拌,得到强碱性溶液,用于织物的处理。浸泡获取强碱性溶液时,发生的化学反应有:Ⅰ.CaO+H2O=Ca(OH)2;Ⅱ.K2CO3+Ca(OH)2=CaCO3↓+2KOH。①Ⅰ的化学反应类型是。
②该强碱性溶液中,有效成分是。
(2)、现代工艺:通常用氢氧化钠溶液来处理织物。①配制100千克溶质的质量分数为0.4%的氢氧化钠溶液,需要溶质的质量分数为20%的氢氧化钠溶液多少千克?
100×0.4%=20%m浓 m浓=2kg
②碱液处理后的织物,用醋酸调节pH至7.5~4.0之间。为什么用醋酸呢?表中是在60毫升0.4%的氢氧化钠溶液(pH=13.0)中加入酸的体积和溶液pH的部分数据。根据表中信息,解释使用醋酸的原因:。
组别 酸 加入酸的体积(毫升) 溶液pH 1 3.6%醋酸(pH=2.5) 10.1 6.7 30.0 4.4 2 3.6%醋酸(pH=2.5) 5.9 11.4 6.1 3.6 3 0.012%盐酸(pH=2.5) 1824 8.2 1825 7.0 14. 古籍中有记载制烧碱的方法,其核心反应可表示为:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓小宁模仿古法,以实验室中的Na2CO3、Ca(OH)2固体为原料,制备400g溶质质量分数为10%的NaOH溶液用于制作叶脉书签。
(1)、制作叶脉书签时,用NaOH溶液去除叶肉,是利用了NaOH的性。(2)、400g溶质质量分数为10%的NaOH溶液中,含NaOH的质量为g,水的质量为g。(3)、需称取Na2CO3、Ca(OH)2的质量各为多少?二、对点训练
-
15. 60℃时,向烧杯A、B、C、D中均倒入100克水,并分别加入50克、25克、15克、10克同种固体物质,同时将D烧杯中的液体降温到20℃,充分溶解后静置一段时间,现象如图所示。则四个烧杯中的溶液一定是该固体物质不饱和溶液的是( )A、
 B、
B、 C、
C、 D、
D、 16. 如图为小明自制“棒棒糖”的流程,则下列烧杯内溶液一定为饱和溶液的是( )
16. 如图为小明自制“棒棒糖”的流程,则下列烧杯内溶液一定为饱和溶液的是( ) A、甲、丁 B、乙、丙 C、甲、丙 D、乙、丁17. 某同学配制50克溶质质量分数为10%氯化钠溶液,步骤如图所示,下列说法正确的是( )
A、甲、丁 B、乙、丙 C、甲、丙 D、乙、丁17. 某同学配制50克溶质质量分数为10%氯化钠溶液,步骤如图所示,下列说法正确的是( ) A、配制过程中出现了一处操作错误 B、溶液配制的实验步骤:称量和量取、溶解 C、溶解过程中用玻璃棒搅拌的目的是增大氯化钠在水中的溶解度 D、若所有操作都正确,称量时所用砝码生锈,会导致所配制溶液的溶质质量分数偏大18. 水是人类宝贵的自然资源,下列关于水的说法正确的是( )A、水在达到100℃时,一定会沸腾 B、水结冰后体积会变小,密度会变小 C、水在通电的条件下能分解成氧气和氢气 D、水是由氧气和氢气构成的19. 在制备硫酸铜晶体时,小明在50克的70℃热水(图甲)中,加入80克硫酸铜粉末后现象如图乙所示,后续过程如下图。
A、配制过程中出现了一处操作错误 B、溶液配制的实验步骤:称量和量取、溶解 C、溶解过程中用玻璃棒搅拌的目的是增大氯化钠在水中的溶解度 D、若所有操作都正确,称量时所用砝码生锈,会导致所配制溶液的溶质质量分数偏大18. 水是人类宝贵的自然资源,下列关于水的说法正确的是( )A、水在达到100℃时,一定会沸腾 B、水结冰后体积会变小,密度会变小 C、水在通电的条件下能分解成氧气和氢气 D、水是由氧气和氢气构成的19. 在制备硫酸铜晶体时,小明在50克的70℃热水(图甲)中,加入80克硫酸铜粉末后现象如图乙所示,后续过程如下图。 (1)、请判断图丙(填“是”或“不是”)饱和溶液。(2)、图丙到图丁的实验过程中获得硫酸铜晶体的方法是。(3)、硫酸铜溶解度随温度变化的数据如表所示,则图丁中溶液的溶质质量分数为.(结果保留小数点后一位)
(1)、请判断图丙(填“是”或“不是”)饱和溶液。(2)、图丙到图丁的实验过程中获得硫酸铜晶体的方法是。(3)、硫酸铜溶解度随温度变化的数据如表所示,则图丁中溶液的溶质质量分数为.(结果保留小数点后一位)温度/℃
。
10
20
30
40
60
70
80
溶解度/g
14.8
17.6
20.5
24.2
28.5|
39.6
48.0
53.6
20. 如图甲所示为西藏芒康盐井古盐田,该地仍然保留着我国最原始的手工晒盐方法,江边的盐田经阳光蒸晒,晒干之后得到粗盐。小金按如图乙所示的操作流程提纯含少量泥沙的粗盐。
 (1)、通过①操作得到的物质为(选填“纯净物”或“混合物”)。(2)、如图所示的实验操作中,需要用到玻璃棒的有(填序号)。(3)、测定粗盐中氯化钠的质量分数时,下列实验操作中,会使测量结果偏大的是()(填字母)。A、蒸发过程中晶体飞溅 B、蒸发所得的精盐比较潮湿 C、蒸发皿中的精盐没有全部转移到称量纸上21. 解放战争时期,为红军运送食盐的老百姓将“土盐”全部溶解成盐水,再将浸有盐水的棉袄带到根据地,以此躲过敌人的盘查。
(1)、通过①操作得到的物质为(选填“纯净物”或“混合物”)。(2)、如图所示的实验操作中,需要用到玻璃棒的有(填序号)。(3)、测定粗盐中氯化钠的质量分数时,下列实验操作中,会使测量结果偏大的是()(填字母)。A、蒸发过程中晶体飞溅 B、蒸发所得的精盐比较潮湿 C、蒸发皿中的精盐没有全部转移到称量纸上21. 解放战争时期,为红军运送食盐的老百姓将“土盐”全部溶解成盐水,再将浸有盐水的棉袄带到根据地,以此躲过敌人的盘查。 (1)、为了将“土盐”快速溶于水中,可采用的方法是(写出一种即可)。(2)、老百姓将棉袄中的液体挤出,再将液体置于铁锅中煎煮得盐,“煎煮”类似于下图中的操作(填字母)。(3)、“土盐”因含有较多的MgCl2而口感苦涩,若要除去“土盐”中的MgCl2 , 可使用适量的试剂。22. 我国南海的永暑岛扩大面积之后慢慢在岛的地下形成了淡水,如图为海岛上的小型水循环模型。
(1)、为了将“土盐”快速溶于水中,可采用的方法是(写出一种即可)。(2)、老百姓将棉袄中的液体挤出,再将液体置于铁锅中煎煮得盐,“煎煮”类似于下图中的操作(填字母)。(3)、“土盐”因含有较多的MgCl2而口感苦涩,若要除去“土盐”中的MgCl2 , 可使用适量的试剂。22. 我国南海的永暑岛扩大面积之后慢慢在岛的地下形成了淡水,如图为海岛上的小型水循环模型。 (1)、可以用“全年高温、降水丰富”来描述永暑岛的(选填“天气”或“气候”)。(2)、永暑岛的地下淡水的补给直接来自水循环的环节。(3)、岛上的水资源比较宝贵,下列利于水资源保护的是(填序号)。
(1)、可以用“全年高温、降水丰富”来描述永暑岛的(选填“天气”或“气候”)。(2)、永暑岛的地下淡水的补给直接来自水循环的环节。(3)、岛上的水资源比较宝贵,下列利于水资源保护的是(填序号)。①工业废水直接排入地下
②农业上采用滴灌技术
③生活污水净化后再排放
23. 如图是硫酸铜晶体的制备和生长实验过程。 (1)、按照物质的组成分类,硫酸铜饱和溶液属于。(2)、硫酸铜饱和溶液在温度下降析出晶体的过程中,溶质质量分数(选填“变大”、“不变”或“变小”)。(3)、在冷却至室温后,通过法硫酸铜晶体继续生长。24. 硝酸钾(KNO3)是一种常见的化肥,在农业生产中常需配制成不同浓度的溶液后再使用,其溶解度随温度变化如下表:
(1)、按照物质的组成分类,硫酸铜饱和溶液属于。(2)、硫酸铜饱和溶液在温度下降析出晶体的过程中,溶质质量分数(选填“变大”、“不变”或“变小”)。(3)、在冷却至室温后,通过法硫酸铜晶体继续生长。24. 硝酸钾(KNO3)是一种常见的化肥,在农业生产中常需配制成不同浓度的溶液后再使用,其溶解度随温度变化如下表:温度/℃
10
20
30
40
硝酸钾溶解度/g
20.9
31.6
45.8
63.9
(1)、硝酸钾中除钾元素外,元素也对植物的生长至关重要,属于复合肥。(2)、某农户在40℃时将30g硝酸钾加入100g水中,充分搅拌后得到溶液。若将此溶液降温至20℃,得到的是(填“饱和”或“不饱和”)溶液。(3)、上述40℃时所得溶液需稀释为5%的硝酸钾溶液用于育苗,需再加水g。25. 小科用硝酸钾进行了如图所示的实验(忽略水的蒸发)。已知温度在 时硝酸钾的溶解度分别为40g、110g。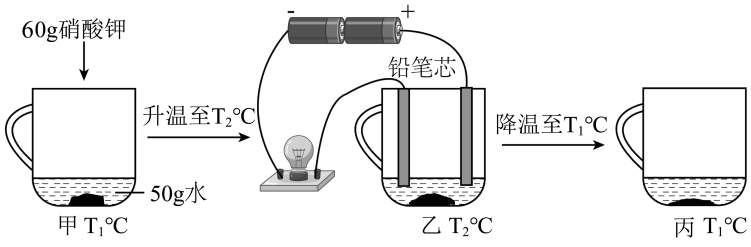 (1)、甲中硝酸钾溶液(填“是”或“不是”)饱和溶液。(2)、乙溶液的质量分数(填“大于”“等于”或“小于”)丙溶液的质量分数。(3)、图乙中硝酸钾溶液相当于(填“用电器”或“电源”)。26. 为保护环境,工业废水检测合格才能排放,某废水经过处理后还含有氢氧化钡而呈碱性(不含其它杂质),小滨取该废水样品,配制溶质质量分数为9.8%的硫酸溶液来测定氢氧化钡的浓度。(1)、用98%的浓硫酸配制成100克溶质质量分数为9.8%的稀硫酸,将下列操作合理排序。
(1)、甲中硝酸钾溶液(填“是”或“不是”)饱和溶液。(2)、乙溶液的质量分数(填“大于”“等于”或“小于”)丙溶液的质量分数。(3)、图乙中硝酸钾溶液相当于(填“用电器”或“电源”)。26. 为保护环境,工业废水检测合格才能排放,某废水经过处理后还含有氢氧化钡而呈碱性(不含其它杂质),小滨取该废水样品,配制溶质质量分数为9.8%的硫酸溶液来测定氢氧化钡的浓度。(1)、用98%的浓硫酸配制成100克溶质质量分数为9.8%的稀硫酸,将下列操作合理排序。A量取 B 计算 C 溶解
(2)、溶解时,小滨将适量水缓慢倒入装有适量浓硫酸的量筒中,此操作存在问题,请将其改正:。(3)、取废水样品20克,滴加酚酞试液1克,逐滴加入9.8%稀硫酸,恰好褪色时用去稀硫酸4克,则该样品中氢氧化钡的质量分数为。27. 棉、麻等植物在生长的过程中会积累油脂、果胶等杂质,从而影响制成布料的染色效果和手感。在布料加工时,人们往往会通过“碱煮”“酸洗”等过程改善布料性能。
①碱煮:将布料浸泡在质量分数为2%—5%的氢氧化钠溶液中,高温处理去除果胶等杂质,使布料变得柔软。
②酸洗:用盐酸清洗残留的碱液,调整布料pH至中性,避免后续加工变色或纤维损伤。(1)、某次配制过程中,需要2%的氢氧化钠溶液20千克,则应称取氢氧化钠的质量为千克。(2)、用水清洁后,每吨布料上仍残留12千克氢氧化钠(不考虑其他杂质),用质量分数为7.3%盐酸进行清洗,请计算清洗一吨布料需要消耗盐酸多少千克? (已知: