初中科学浙教版 七年级下册 第二章 第3节 建构原子模型同步练习
试卷更新日期:2026-02-27 类型:同步测试
一、选择题
-
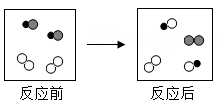
1. 臭氧(O3)、二氧化氯(ClO2)、过氧化氢(H2O2)都是生产、生活中最常用的消毒剂.三种物质中都含有( )A、氧分子 B、氧离子 C、氧气 D、氧元素2. 如图是某化学反应的微观模拟示意图,每个小球代表一种元素的原子。下列说法正确的是( )
 A、该反应前后元素的种类发生了改变 B、在“
A、该反应前后元素的种类发生了改变 B、在“ ”分子中,若“●”元素化合价为+1价,则“◯”元素化合价为-2价
C、该图示说明化学变化中分子、原子都可分
D、参加反应的“
”分子中,若“●”元素化合价为+1价,则“◯”元素化合价为-2价
C、该图示说明化学变化中分子、原子都可分
D、参加反应的“ ”和“
”和“ ”分子的个数比为1:2
3. 我国科学家张青莲教授主持测定了铟、铱、锗等十种元素的相对原子质量,被采用为国际标准。在元素周期表中,铟与铝同族,铟的有关信息如图。关于铟说法正确的是
”分子的个数比为1:2
3. 我国科学家张青莲教授主持测定了铟、铱、锗等十种元素的相对原子质量,被采用为国际标准。在元素周期表中,铟与铝同族,铟的有关信息如图。关于铟说法正确的是 A、属于非金属元素 B、原子核内有49个中子 C、相对原子质量为114.8克 D、最外层电子数与铝原子相等4. 原子核内有6个质子和6个中子的一个碳原子的质量为akg,另一种元素的相对原子质量 b, 则该元素的一个原子的质量为( )A、 B、 C、 D、5. 如图表示四种原子的结构模型 (“●”、 “◯”和“”分别表示电子、中子、质子),下列说法正确的是( )
A、属于非金属元素 B、原子核内有49个中子 C、相对原子质量为114.8克 D、最外层电子数与铝原子相等4. 原子核内有6个质子和6个中子的一个碳原子的质量为akg,另一种元素的相对原子质量 b, 则该元素的一个原子的质量为( )A、 B、 C、 D、5. 如图表示四种原子的结构模型 (“●”、 “◯”和“”分别表示电子、中子、质子),下列说法正确的是( ) A、甲、丙的核电荷数不同 B、甲、丙为同一种原子 C、乙、丁属于同一种元素 D、甲、乙互为同位素原子6. 分析图所示测定相对原子质量的示意图,则A原子的相对原子质量约为( )
A、甲、丙的核电荷数不同 B、甲、丙为同一种原子 C、乙、丁属于同一种元素 D、甲、乙互为同位素原子6. 分析图所示测定相对原子质量的示意图,则A原子的相对原子质量约为( ) A、5 B、10 C、12 D、167. 1911年,英国科学家卢瑟福进行了著名的α粒子轰击金箔实验,根据这个实验获得的正确结论是( )
A、5 B、10 C、12 D、167. 1911年,英国科学家卢瑟福进行了著名的α粒子轰击金箔实验,根据这个实验获得的正确结论是( ) A、金原子核带正电荷 B、金原子是实心球体,紧密排列 C、金原子中有带负电的电子 D、金原子核的质量与α粒子质量相当8. 如图所示,正确反映原子模型建立先后顺序的是( )
A、金原子核带正电荷 B、金原子是实心球体,紧密排列 C、金原子中有带负电的电子 D、金原子核的质量与α粒子质量相当8. 如图所示,正确反映原子模型建立先后顺序的是( )


①原子行星模型 ②原子葡萄干蛋糕模型 ③氦原子电子云模型
A、①②③ B、①③② C、②①③ D、①③②9. 下列关于构成物质的微粒说法正确的是( )A、目前发现的微粒只有分子、原子、离子三种 B、分子由原子构成,因此原子一定比分子小 C、Cl和Cl-属于同种元素,但化学性质不同 D、构成O2 、CO2 两种物质的微粒中都含有氧分子10. 已知钠离子带一个单位正电荷,其结构示意图如图所示。下列说法正确的是( ) A、图中a的值为9 B、钠离子符号为Na+ C、钠离子是钠原子得到一个电子形成的 D、氧化钠的化学式为NaO11. 研究发现,苍蝇体内能够产生抗细菌感染的过氧化氢 下列关于过氧化氢(H2O2) 和水(H2O) 的叙述正确的是()A、是同种物质 B、具有相同的化学性质 C、都是由氢元素和氧元素组成的 D、都是由氢分子和氧分子构成的12. 科学上用符号“”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知 和 的核外电子数相等。则下列关系正确的是 ( )A、b-a=d-c B、 C、 D、13. 如右图是氯化钠形成的微观过程。下列说法错误的是 ( )
A、图中a的值为9 B、钠离子符号为Na+ C、钠离子是钠原子得到一个电子形成的 D、氧化钠的化学式为NaO11. 研究发现,苍蝇体内能够产生抗细菌感染的过氧化氢 下列关于过氧化氢(H2O2) 和水(H2O) 的叙述正确的是()A、是同种物质 B、具有相同的化学性质 C、都是由氢元素和氧元素组成的 D、都是由氢分子和氧分子构成的12. 科学上用符号“”表示原子的组成,其中X代表元素符号,Z表示原子核内的质子数,A表示原子核内质子数与中子数之和。已知 和 的核外电子数相等。则下列关系正确的是 ( )A、b-a=d-c B、 C、 D、13. 如右图是氯化钠形成的微观过程。下列说法错误的是 ( ) A、钠原子与钠离子最大的区别是核外电子数不同 B、原子得到电子形成阳离子,失去电子形成阴离子 C、氯化钠是由氯离子和钠离子构成 D、整个变化过程中元素的种类没变14. 如图是水分子分解示意图,结合该示意图分析,下列说法正确的是( )
A、钠原子与钠离子最大的区别是核外电子数不同 B、原子得到电子形成阳离子,失去电子形成阴离子 C、氯化钠是由氯离子和钠离子构成 D、整个变化过程中元素的种类没变14. 如图是水分子分解示意图,结合该示意图分析,下列说法正确的是( ) A、原子是化学变化中的最小粒子 B、该示意图可用于解释水的蒸发现象 C、水分子是由氢元素和氧元素组成的 D、化学变化中,原子可任意结合成新的分子15. 现有一瓶未贴标签的常见金属R。为了测定R的相对原子质量,准确称取45g该金属粉末,在坩埚内加热使其完全氧化,形成金属氧化物(由R 和氧两种元素组成的化合物)冷却后称得质量为85g。已知R的化合价为+3价,则R 的相对原子质量为( )A、18 B、24 C、27 D、48
A、原子是化学变化中的最小粒子 B、该示意图可用于解释水的蒸发现象 C、水分子是由氢元素和氧元素组成的 D、化学变化中,原子可任意结合成新的分子15. 现有一瓶未贴标签的常见金属R。为了测定R的相对原子质量,准确称取45g该金属粉末,在坩埚内加热使其完全氧化,形成金属氧化物(由R 和氧两种元素组成的化合物)冷却后称得质量为85g。已知R的化合价为+3价,则R 的相对原子质量为( )A、18 B、24 C、27 D、48二、填空题
-
16. 如图为某粒子R的结构示意图:

①当x=10+y时,该粒子为(填“原子”或“阳离子”或“阴离子”)。
②若该结构示意图表示的粒子是Cl﹣ , 则y=。
17. 在宏观、微观和符号之间建立联系是科学学科的特点。(1)、物质的组成及构成关系如图所示,图中①是。 (2)、下列说法正确的是____(填字母)。A、氯化钠是由钠、氯两种元素组成的 B、氯化钠是由钠和氯气混合而成的 C、氯化钠是由一个钠原子和一个氯原子构成的(3)、氧和氯两种元素最本质的区别是它们原子中的不同;18. 图1是构成物质的微粒间的关系;图2是三种微粒的微观示意图;图3 是元素周期表的部分。回答下列问题:
(2)、下列说法正确的是____(填字母)。A、氯化钠是由钠、氯两种元素组成的 B、氯化钠是由钠和氯气混合而成的 C、氯化钠是由一个钠原子和一个氯原子构成的(3)、氧和氯两种元素最本质的区别是它们原子中的不同;18. 图1是构成物质的微粒间的关系;图2是三种微粒的微观示意图;图3 是元素周期表的部分。回答下列问题:
 (1)、 图1中甲是。(2)、图2中三种微粒共表示种元素。(3)、图3中与④代表的元素,化学性质最相似的是。 (用序号表示)19. 原子结构模型的建立,经过了几代科学家的艰辛努力,直到现在仍在探索中。如图所示为锂原子的核式结构模型,原子内有3个质子,4个中子。
(1)、 图1中甲是。(2)、图2中三种微粒共表示种元素。(3)、图3中与④代表的元素,化学性质最相似的是。 (用序号表示)19. 原子结构模型的建立,经过了几代科学家的艰辛努力,直到现在仍在探索中。如图所示为锂原子的核式结构模型,原子内有3个质子,4个中子。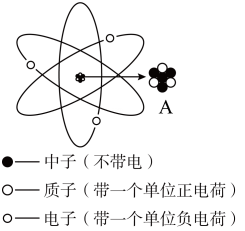 (1)、图中 A 表示的原子结构是;(2)、该锂原子的相对原子质量约为;(3)、锂(Li)原子易失去一个电子形成锂离子,用符号表示锂离子。20. 用锶材料制成的原子钟精准度极高,常被用于卫星的精准计时。图甲是锶元素在元素周期表中的信息以及锶原子的结构示意图,图乙为A、B、C三种微粒的结构示意图。
(1)、图中 A 表示的原子结构是;(2)、该锂原子的相对原子质量约为;(3)、锂(Li)原子易失去一个电子形成锂离子,用符号表示锂离子。20. 用锶材料制成的原子钟精准度极高,常被用于卫星的精准计时。图甲是锶元素在元素周期表中的信息以及锶原子的结构示意图,图乙为A、B、C三种微粒的结构示意图。 (1)、在化学变化中锶原子容易失去电子变为阳离子,其离子符号为。(2)、图乙中A、B、C三种微粒中与锶原子化学性质相似的是。(3)、 若C为离子, 则x=。21. 用
(1)、在化学变化中锶原子容易失去电子变为阳离子,其离子符号为。(2)、图乙中A、B、C三种微粒中与锶原子化学性质相似的是。(3)、 若C为离子, 则x=。21. 用 和
和 分别表示氮原子和氧原子,如图所示是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题:
分别表示氮原子和氧原子,如图所示是氮气与氧气在放电条件下发生反应的微观模拟图。请回答下列问题: (1)、在B图中将相关粒子图形补充完整(画图)。(2)、此过程中发生变化的粒子是(选填“质子”、“原子”或“分子”)。(3)、结合该图,从微观角度解释由A到C变化的实质是。(4)、下列物质中,由原子直接构成的是____。A、甲烷 B、金刚石 C、水银 D、氮气
(1)、在B图中将相关粒子图形补充完整(画图)。(2)、此过程中发生变化的粒子是(选填“质子”、“原子”或“分子”)。(3)、结合该图,从微观角度解释由A到C变化的实质是。(4)、下列物质中,由原子直接构成的是____。A、甲烷 B、金刚石 C、水银 D、氮气三、实验与探究题
-
22. 为探究原子结构,1911年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验,发现现象如图甲。根据α粒子散射实验,统计不同偏转角度的α粒子数量,并绘制成图像如图乙。
现象1:大多数α粒子能穿透金箔而不改变原来运动方向;
现象2:少部分α粒子改变原来的运动方向:
现象3:极少数α粒子被弹了回来。
 (1)、图乙中能说明原子内部绝大部分是空的数据是点(用字母表示);是(2)、请分析现象3的原因;(3)、通过α粒子散射实验,可以推测出原子结构为如图丙所示中的。23. 如图是钠在氯气中燃烧的装置图和其微观示意图。
(1)、图乙中能说明原子内部绝大部分是空的数据是点(用字母表示);是(2)、请分析现象3的原因;(3)、通过α粒子散射实验,可以推测出原子结构为如图丙所示中的。23. 如图是钠在氯气中燃烧的装置图和其微观示意图。 (1)、化学符号“Na”表示的含义有:钠元素、钠单质,还能表示。(2)、金属的实验现象:。(3)、从该反应的微观示意图可知,该反应的实质是原子中的发生了转移。
(1)、化学符号“Na”表示的含义有:钠元素、钠单质,还能表示。(2)、金属的实验现象:。(3)、从该反应的微观示意图可知,该反应的实质是原子中的发生了转移。四、综合题
-
24. 科学家对元素的相对原子质量的认识经历了漫长的时间
材料一:19世纪初,有化学家认为:氢是母体,其他元素原子的相对原子质量理论上都是氢的整数倍,少数元素如C1是35.5倍,则是由于实验误差造成的。
材料二:1886年,英国科学家克鲁克斯大胆假设:同一元素的原子,可以有不同的相对原子质量。化学家定出的元素相对原子质量是其不同原子相对原子质量的平均值。
材料三:1961年8月,国际上采用12C的1/12作为相对原子质量的标准,确定各个同位素原子的相对原子质量。某元素的相对原子质量是其各种同位素原子的相对原子质量乘以各自在该元素中所占的百分比之和。
(1)、在克鲁克斯假设中,同种元素的原子,相对原子质量却不同,是因为原子核中质子数相同,而不同。(2)、氢的三种同位素原子气氘氚相对原子质量分别为1、2、3,氢元素的相对原子质量为1.008,则三种原子中百分比含量最多的是。(3)、结合已学知识和上述材料分析,下列说法正确的____(可多选)A、元素的相对原子质量一定大于它所有的同位素原子的相对原子质量 B、自然界中大部分元素都有同位素原子,由此推测大部分元素的相对原子质量不是整数。 C、若相对原子质量采用12C的1/6作为标准,则各元素的相对原子质量也会改变 D、氯元素的相对原子质量是35.5,自然界仅有的两种同位素原子35C1和37C1,二者数量百分比各占一半 E、在化学变化中某金属原子失去电子与其他原子化合,计算该化合物相对分子质量时仍能使用该金属元素原来的相对原子质量25. 人类为揭示原子结构奥秘,经历了漫长的探究过程。原子结构的认识发展史简单归纳如下: (1)、卢瑟福核式结构模型,是基于“用带正电的α粒子轰击金属箔”的实验提出的。荧光屏设计成 360°环绕,是因为卢瑟福在实验前认为α粒子可能穿过金箔,也可能。
(1)、卢瑟福核式结构模型,是基于“用带正电的α粒子轰击金属箔”的实验提出的。荧光屏设计成 360°环绕,是因为卢瑟福在实验前认为α粒子可能穿过金箔,也可能。
①a粒子发生器——放出a粒子(带正电荷)质量是电子质量的7000多倍;
②金箔——作为靶子,厚度1μm,重叠了3000层左右的原子;
③荧光屏——a粒子打在上面发出闪光。
(2)、根据实验现象(如图),不能获得的结论是____;(填字母) A、原子核体积很小 B、原子核质量较大 C、原子核带正电荷 D、核外电子带负电荷(3)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有微粒从氮原子中被击出,而α粒子留在了氮原子中,将氮原子变成了氧原子。从现代观点看,被击出的微粒一定含有。(提示:α粒子由2个质子和2个中子构成)26. 从微观层面认识物质是化学独特的视角。许多物质是由分子初晚的,分子又由原子构成。原子虽然眼小,但本身也存在质量。如图是水分子的揯观模型图,表中是几种原子的质量,请根据要求回答下列问题:
A、原子核体积很小 B、原子核质量较大 C、原子核带正电荷 D、核外电子带负电荷(3)、1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有微粒从氮原子中被击出,而α粒子留在了氮原子中,将氮原子变成了氧原子。从现代观点看,被击出的微粒一定含有。(提示:α粒子由2个质子和2个中子构成)26. 从微观层面认识物质是化学独特的视角。许多物质是由分子初晚的,分子又由原子构成。原子虽然眼小,但本身也存在质量。如图是水分子的揯观模型图,表中是几种原子的质量,请根据要求回答下列问题:
原子种类
1个原子的质量/kg
相对原子质量
氢
1
氧
16
碳-12
12
(1)、 1个水分子的质量是多少? (在横线上列出算式) =2.9918×10-26kg(2)、由上述计算可知分子根小,书写、记忆和使用都很不方便。为此可采用类似“原子”的处理方法。即以碳-12原子质量的 作为标准,用分子的质量跟它的比值,得到分子的相对质量。请用该思路求H2O的相对分子质量。 (请列式计算,计算结果保留整数)