广东省湛江市寸金培才学校等七校2025-2026学年九年级上学期化学期末试卷
试卷更新日期:2026-01-23 类型:期末考试
一、选择题
-
1. 北宋《千里江山图》中的颜料来自矿物,并经研磨、溶解、过滤等工序获得。下列颜料的制作方法中一定涉及化学变化的是A、研磨法 B、沉淀法 C、焙烧法 D、溶剂法2. 下列图标与实验“硫在空气中燃烧”无关的是A、护目镜
 B、明火
B、明火 C、排风
C、排风 D、用电
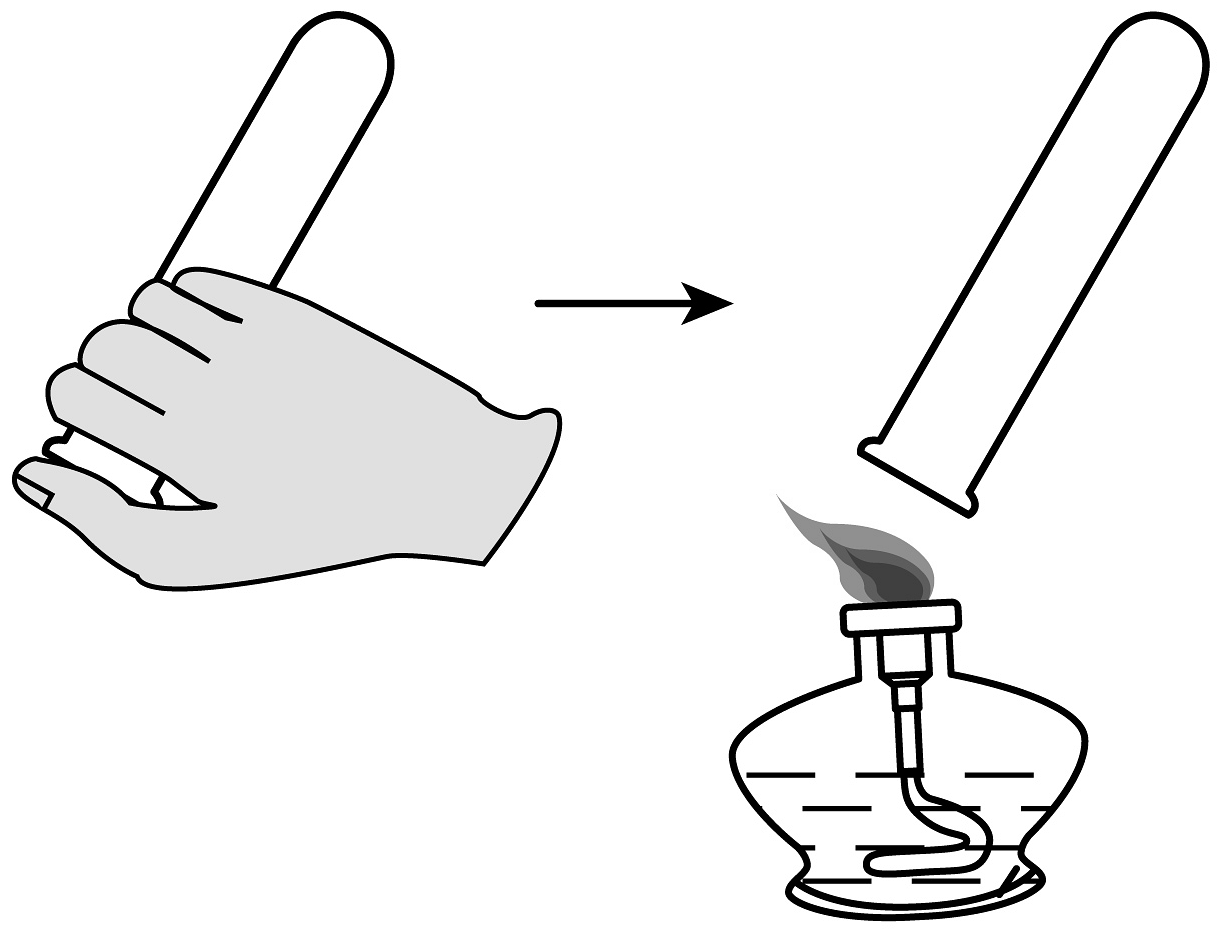
D、用电 3. 规范的实验操作是学习化学的基本素养,下列所示实验操作正确的是A、点燃酒精灯
3. 规范的实验操作是学习化学的基本素养,下列所示实验操作正确的是A、点燃酒精灯 B、倾倒液体
B、倾倒液体 C、蒸发溶液
C、蒸发溶液 D、滴加稀盐酸
D、滴加稀盐酸 4. 长银同学的下面化学用语表示正确的是( )A、锌: B、氯化钙: C、镁离子: D、四个磷原子:5. 空气是人类生产活动的重要资源。下列关于空气的说法不正确的是( )A、空气是工业制取氧气的廉价、易得的原料 B、倡导“低碳”生活有利于减少温室气体的排放 C、将氮气充入食品包装袋中可起到防腐作用 D、人呼吸空气时呼出的气体中只含有二氧化碳6. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、溶液是无色透明的,则无色透明的液体都是溶液 B、铝在空气中比铁更耐腐蚀,则铝的金属活动性弱于铁 C、含碳元素的物质充分燃烧会生成CO2 , 则燃烧能生成CO2的物质一定含碳元素 D、硝酸钾的溶解度随温度的升高而增大,则所有物质的溶解度都随温度的升高而增大7. 图A是两种元素在元素周期表中的信息,图B是氟元素的原子结构示意图,下列说法正确的是
4. 长银同学的下面化学用语表示正确的是( )A、锌: B、氯化钙: C、镁离子: D、四个磷原子:5. 空气是人类生产活动的重要资源。下列关于空气的说法不正确的是( )A、空气是工业制取氧气的廉价、易得的原料 B、倡导“低碳”生活有利于减少温室气体的排放 C、将氮气充入食品包装袋中可起到防腐作用 D、人呼吸空气时呼出的气体中只含有二氧化碳6. 推理是化学学习中常用的思维方法。下列推理正确的是( )A、溶液是无色透明的,则无色透明的液体都是溶液 B、铝在空气中比铁更耐腐蚀,则铝的金属活动性弱于铁 C、含碳元素的物质充分燃烧会生成CO2 , 则燃烧能生成CO2的物质一定含碳元素 D、硝酸钾的溶解度随温度的升高而增大,则所有物质的溶解度都随温度的升高而增大7. 图A是两种元素在元素周期表中的信息,图B是氟元素的原子结构示意图,下列说法正确的是 A、图A“钠”方框右上角横线上应填写NA B、图B方框横线上的数字是8 C、氟元素属稀有气体元素 D、11号元素与9号元素可以形成化学式为NaF的化合物8. “劳动点亮生命之灯”。下列劳动实践对应的化学知识没有关联的是
A、图A“钠”方框右上角横线上应填写NA B、图B方框横线上的数字是8 C、氟元素属稀有气体元素 D、11号元素与9号元素可以形成化学式为NaF的化合物8. “劳动点亮生命之灯”。下列劳动实践对应的化学知识没有关联的是选项
劳动实践
化学知识
A
用干冰人工增雨
干冰升华吸热
B
调小灶具进气口
燃气是可燃物
C
用铅笔芯制作电极
石墨有导电性
D
给铁栏杆刷防锈漆
金属刷漆可隔绝氧气和水
A、A B、B C、C D、D9. “天宫”建造全面展开,我国载人航天进入“空间站时代”。结合所学知识,完成下面小题。(1)、“天宫二号”太空舱利用作催化剂,将航天员呼出的二氧化碳转化为氧气。已知中元素的化合价为 , 则元素的化合价是( )A、 B、 C、 D、(2)、生产航天服的原料之一是二苯甲烷二异氰酸酯 , 关于二苯甲烷二异氰酸酯的说法正确的是( )A、是一种氧化物 B、含有个氮分子和个氧分子 C、由碳元素、氢元素、氮元素和氧元素组成 D、由个碳原子、个氢原子、个氮原子、个氧原子构成10. 建立模型是学习化学的重要方法,下列不正确的是A、地壳元素含量 B、氢原子结构模型
B、氢原子结构模型 C、物质分类模型
C、物质分类模型 D、空气组成模型
D、空气组成模型 11. 三种固体物质A、B、C的溶解度曲线如图所示,则下列说法不正确的是( )
11. 三种固体物质A、B、C的溶解度曲线如图所示,则下列说法不正确的是( ) A、t1℃时,三种物质的溶解度大小顺序为C>B>A B、t3℃时,将等质量的A、B、C三种物质的饱和溶液降温至t2℃,t2℃三种溶液的溶质质量分数为B>A=C C、若A物质中混有少量的B物质,可以用降温结晶的方法提纯A D、若要将组成在b点的A溶液转变为a点的A溶液,可以采用恒温蒸发溶剂的方法12. 对比实验是进行科学探究的重要方式。如图所示实验均用到了对比的方法。
A、t1℃时,三种物质的溶解度大小顺序为C>B>A B、t3℃时,将等质量的A、B、C三种物质的饱和溶液降温至t2℃,t2℃三种溶液的溶质质量分数为B>A=C C、若A物质中混有少量的B物质,可以用降温结晶的方法提纯A D、若要将组成在b点的A溶液转变为a点的A溶液,可以采用恒温蒸发溶剂的方法12. 对比实验是进行科学探究的重要方式。如图所示实验均用到了对比的方法。
下列说法错误的是( )
A、图实验能验证二氧化碳与水发生了反应 B、图实验能说明红磷的着火点比白磷的高 C、图实验能验证金属活动性顺序为 D、图实验能说明硝酸铵固体溶于水会吸收热量13. 下列实验设计与对应的实验目的表述不一致的是


A. 检查装置气密性
B. 检验收集到的氢气的纯度
C. 检验氧气是否已经收集满
D. 验证质量守恒定律
A、A B、B C、C D、D二、非选择题
-
14. 氯化钠是一种应用广泛的物质,常用于生产氯气、烧碱、做调味品。(1)、海水中含有大量的氯化钠,其中氯化钠是以形式存在填“分子”或“离子”。(2)、海水晒盐过程中,将结晶池的物质分离可以得到粗盐和母液。母液中氯化钠属于填“饱和”或“不饱和”状态,将粗盐和母液分开的操作是。(3)、利用氯化钠可以配制质量分数为的洗鼻喷雾剂,配制洗鼻喷雾剂密度约为 , 需要的氯化钠的质量为。(4)、如表是不同温度下氯化钠和氯化钙的溶解度。
温度
溶解度
氯化钠
氯化钙
现有氯化钙和氯化钠的混合物,向其中加入适量的水溶解,蒸发浓缩,降低温度至时有大量晶体,所得的晶体主要成分是 , 你的依据是;此时混合溶液中氯化钙和水的质量比为。
15. 【科普阅读】氢气燃烧热值高,约是煤的四倍,是理想的清洁能源,年中国各能源消费占比如图所示。
分解海水制氢被认为是最可行的清洁制氢技术,主要有以下两种研究方向。
光解水,在太阳光驱动下催化水发生分解。使用氮化铟镓作为催化剂,不同温度下的制氢效率如图所示。因光腐蚀、能量转换效率低等技术问题,目前并未实际投入生产。
电解水,利用电能将水分解。海水中成分复杂,电解时易对电极等材料造成腐蚀或生成不需要的副产物。我国科学家研制的海上制氢平台,将海水中的水以水汽的形式跨膜转移,实现了海水中的杂质完全分离,而电解海水所需电能完全来自于风能和太阳能,向世界展示零碳能源的中国方案。
 (1)、由图可知,年我国能源消费占比最高的是。(2)、光解水目前未实际投入生产,其原因是。(3)、由图可知,使用氮化铟镓为催化剂进行光解水时,温度越填“高”或“低” , 制氢效率越高。(4)、电解水的化学方程式为 , 该过程中将能转化为化学能。(5)、下列说法正确的是多选,填字母。
(1)、由图可知,年我国能源消费占比最高的是。(2)、光解水目前未实际投入生产,其原因是。(3)、由图可知,使用氮化铟镓为催化剂进行光解水时,温度越填“高”或“低” , 制氢效率越高。(4)、电解水的化学方程式为 , 该过程中将能转化为化学能。(5)、下列说法正确的是多选,填字母。煤的燃烧热值比氢气高
电解海水时,海水中成分易对电极造成腐蚀
化学与新能源开发密切相关
16. 根据下列实验装置回答问题: (1)、仪器的名称是。(2)、实验室用装置或装置制取氧气的化学方程式是;对比装置 , 使用装置制取氧气的优点是;若要收集一瓶干燥的 , 可选择的收集装置是填字母。(3)、实验室常用稀盐酸与大理石制取 , 实验操作步骤如下:加入稀盐酸开始收集气体;验满;加入大理石并固定仪器;检查装置的气密性;将收集满的集气瓶正放在桌面上。正确的操作顺序是( )填字母。A、 B、 C、 D、(4)、装置中,紫色石蕊溶液变红的原因是用化学方程式表示。17. 某研究小组以“食品中的脱氧剂”为主题进行项目式探究学习。(1)、【任务一】认识脱氧剂的作用
(1)、仪器的名称是。(2)、实验室用装置或装置制取氧气的化学方程式是;对比装置 , 使用装置制取氧气的优点是;若要收集一瓶干燥的 , 可选择的收集装置是填字母。(3)、实验室常用稀盐酸与大理石制取 , 实验操作步骤如下:加入稀盐酸开始收集气体;验满;加入大理石并固定仪器;检查装置的气密性;将收集满的集气瓶正放在桌面上。正确的操作顺序是( )填字母。A、 B、 C、 D、(4)、装置中,紫色石蕊溶液变红的原因是用化学方程式表示。17. 某研究小组以“食品中的脱氧剂”为主题进行项目式探究学习。(1)、【任务一】认识脱氧剂的作用食品包装中加入脱氧剂的作用是( )。填字母
A、除去氧气,抑制霉菌生长 B、防止食品因氧化而变色、变质(2)、【任务二】探究脱氧剂的成分用剪刀剪开一包脱氧剂,倾倒于白纸上,观察到有黑色粉末和少量的白色固体。结合查阅的资料,推测黑色粉末可能是铁粉、活性炭、二氧化锰、四氧化三铁等。
探究过程
实验现象
实验结论
用磁铁靠近该混合物
部分黑色粉末被吸引
粉末可能含有和
取少量磁铁上吸引的黑色粉末于试管中,加入足量。
黑色固体完全消失,。
黑色粉末中含有铁粉:反应的化学方程式。
另取少量黑色粉末,采用以下装置加热。

。
固体中含有活性炭。
资料还显示,脱氧剂中还含有食盐、生石灰、吸水性树脂等物质。
(3)、【任务三】解密脱氧原理剪开一包脱氧剂,用磁铁靠近,将吸引的黑色粉末装入一个无纺布袋中,滴加滴水,封口,轻轻揉搓布袋。
打开布袋看到黑色粉末变为色,表明铁粉发生氧化生锈。
(4)、研究表明,铁粉能与空气中的反应,从而实现包装食品的保鲜、防腐。(5)、钢铁生锈腐蚀会造成巨大经济损失,常见的钢铁防腐措施有。写一种即可。18. 古代用“失蜡法”铸造青铜器:用蜂蜡做成铸件模型,再用黏土敷成外范,烧成陶模,烧制过程蜂蜡全部熔化流失,使整个铸件模型变成空壳,再往内浇灌高温青铜液,便铸成器物。(1)、上述过程中主要涉及化学变化的步骤是____(填标号)。A、蜂蜡成模 B、黏土烧陶 C、浇灌成器(2)、青铜器属于(填“金属”“无机非金属”或“合成”)材料。(3)、青铜为铜与锡的合金,青铜的熔点(填“高于”或“低于”)纯铜的熔点。(4)、古代火法炼铜中,氧化铜与碳在高温条件下能反应生成铜与二氧化碳,该反应的化学方程式为。(5)、铜锈赋予青铜器历史感。铜锈主要有 Cu2(OH)2CO3和 Cu2(OH)3Cl,考古界根据铜锈是否会加速铜的锈蚀分为“有害锈”和“无害锈”,其作用示意图如下:
据图可知 Cu2(OH)3Cl 具有(填“致密”或“疏松”)结构,因此属于(填“有害锈”或“无害锈”)。
19. 从古至今,钢铁及其铁的化合物一直被人类广泛应用。 (1)、梦溪笔谈记载南北朝时“灌钢”法:将生铁液注入熟铁中快速炼钢。生铁与钢的区别是不同。
(1)、梦溪笔谈记载南北朝时“灌钢”法:将生铁液注入熟铁中快速炼钢。生铁与钢的区别是不同。梦溪笔谈记载“熬胆矾铁釜久亦化为铜”胆矾为晶体 , 用化学方程式表示其原理。
“釜”指生铁制作的铁锅,利用铁的选填序号之一。
A.导热性 B.导电性 C.硬度大
(2)、化学兴趣小组的同学为确定某铁合金样品是生铁还是钢,他们取铁合金样品盛放到锥形瓶中,将稀硫酸分成等份,分次加入锥形瓶,每次待充分反应后记录实验数据假设铁合金样品中只含有铁、碳两种元素。实验数据整理如表所示:次数
第次
第次
第次
第次
第次
加入稀硫酸的质量
瓶中物质总质量
请回答下列问题:
实验室若要用的浓硫酸配制质量分数为硫酸,所需要水的质量为。
表格中的的值为。
通过计算判断该铁合金样品是生铁还是钢。请写出计算过程,结果精确到生铁含碳量为 , 钢含碳量为