人教版初中化学九年级上册期末专题复习专题十 制取气体的反应原理的探究(B卷)
试卷更新日期:2025-12-21 类型:复习试卷
一、选择题
-
1.
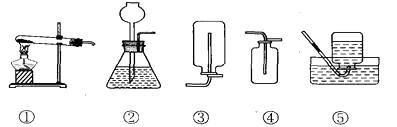
利用如图所示装置,能完成实验室制取气体的是( )
 A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳2. 潜水艇里需要配备氧气的再生装置,以保证长时间潜航。下列反应都能产生氧气,其中最适宜在潜水艇里供给氧气的反应是A、高锰酸钾锰酸钾+二氧化锰+氧气 B、水氢气+氧气 C、过氧化钠+二氧化碳碳酸钠+氧气 D、过氧化氢水+氧气3. 实验室加热氯酸钾和加热高锰酸钾制取氧气,两者的相同点是()A、都生成了两种物质 B、都使用二氧化锰作催化剂 C、都发生了化合反应 D、都发生分解反应4. 下列关于实验操作中先后顺序的叙述错误的是( )
A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳2. 潜水艇里需要配备氧气的再生装置,以保证长时间潜航。下列反应都能产生氧气,其中最适宜在潜水艇里供给氧气的反应是A、高锰酸钾锰酸钾+二氧化锰+氧气 B、水氢气+氧气 C、过氧化钠+二氧化碳碳酸钠+氧气 D、过氧化氢水+氧气3. 实验室加热氯酸钾和加热高锰酸钾制取氧气,两者的相同点是()A、都生成了两种物质 B、都使用二氧化锰作催化剂 C、都发生了化合反应 D、都发生分解反应4. 下列关于实验操作中先后顺序的叙述错误的是( )
A、用托盘天平称量药品时,先调节天平平衡,后称量 B、检查装置气密性时,先用手捂住试管一会儿,再将导管伸入烧杯内水中 C、使用胶头滴管吸取液体时,先将胶头滴管伸入液体中,后挤压胶头吸入液体。 D、制备气体时,先检查装置的气密性,后装入药品5. 下列反应都能产生氧气,其中最适宜在潜水艇里供给氧气的反应是( )A、高锰酸钾 锰酸钾+二氧化锰+氧气 B、过氧化钠+二氧化碳→碳酸钠+氧气 C、分离液态空气 D、过氧化氢 水+氧气6. 实验室制取氧气时,必须满足的条件是()A、必须使用催化剂 B、必须用含氧元素的物质作反应物 C、必须加热 D、必须用排水法收集7.利用下图所示装置,能完成实验室制取气体的是( )
 A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳8. 从安全、节能、环保和简便等方面考虑,实验室制取氧气的最佳方法是( )A、 B、 C、 D、9. 工业上可用二氧化硫制取氢气,流程如下图。下列有关说法错误的是( )
A、用①③制取氧气 B、用②③制取二氧化碳 C、用②④制取氧气 D、用①⑤制取二氧化碳8. 从安全、节能、环保和简便等方面考虑,实验室制取氧气的最佳方法是( )A、 B、 C、 D、9. 工业上可用二氧化硫制取氢气,流程如下图。下列有关说法错误的是( ) A、采用该流程可减少二氧化硫对大气的污染 B、膜反应器中反应为:2HI=H2+I2 C、分离器中分离出的副产品是硫酸 D、生产流程中能被循环利用的物质是I210. 质量相等的两份氯酸钾a和b,a中再加少量二氧化锰,b中再加入少量高锰酸钾,将药品分别加热到完全反应,则收集到氧气的质量随加热时间变化的图象如下,其中相对正确的是( )A、
A、采用该流程可减少二氧化硫对大气的污染 B、膜反应器中反应为:2HI=H2+I2 C、分离器中分离出的副产品是硫酸 D、生产流程中能被循环利用的物质是I210. 质量相等的两份氯酸钾a和b,a中再加少量二氧化锰,b中再加入少量高锰酸钾,将药品分别加热到完全反应,则收集到氧气的质量随加热时间变化的图象如下,其中相对正确的是( )A、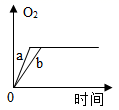 B、
B、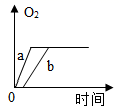 C、
C、 D、
D、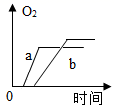
二、综合题
-
11. 实验室常用如图装置制取气体,请你根据所学知识回答下列问题。
 (1)、写出仪器名称:a。(2)、实验室用高锰酸钾制取氧气,写出该反应的文字表达式:;该反应属于(填基本反应类型)。(3)、实验室用过氧化氢溶液和二氧化锰制取并收集一瓶较纯净的氧气时,选用的发生和收集装置是(填字母),若用F装置收集O2气体,则气体从导管(填“c”或“d”)端通入。12. 某化学兴趣小组对二氧化碳的制取原理进行了如下探究:(1)、(一)能利用碳的燃烧获得较纯净的二氧化碳吗?
(1)、写出仪器名称:a。(2)、实验室用高锰酸钾制取氧气,写出该反应的文字表达式:;该反应属于(填基本反应类型)。(3)、实验室用过氧化氢溶液和二氧化锰制取并收集一瓶较纯净的氧气时,选用的发生和收集装置是(填字母),若用F装置收集O2气体,则气体从导管(填“c”或“d”)端通入。12. 某化学兴趣小组对二氧化碳的制取原理进行了如下探究:(1)、(一)能利用碳的燃烧获得较纯净的二氧化碳吗?描述图1所示的木炭在氧气瓶中的燃烧现象:。
 (2)、能用此法收集一瓶较纯净的二氧化碳吗?写出你的分析:。(3)、(二)探究碳酸钙和稀硫酸反应
(2)、能用此法收集一瓶较纯净的二氧化碳吗?写出你的分析:。(3)、(二)探究碳酸钙和稀硫酸反应小组同学向石灰石中加入稀硫酸,实验一开始时,烧杯中出现了不少气泡,请写出该反应的化学方程式:。
(4)、放置一段时间后,观察到烧杯中出现了很多白色粉末状物质,如图2所示。请写出该白色粉末主要成分的名称:。 (5)、小组同学向稀盐酸中加入适量的碳酸钙粉末,观察到有气泡产生,同时固体溶解,推测向稀硫酸溶液中加入适量的碳酸钙粉末,观察到的现象为。
(5)、小组同学向稀盐酸中加入适量的碳酸钙粉末,观察到有气泡产生,同时固体溶解,推测向稀硫酸溶液中加入适量的碳酸钙粉末,观察到的现象为。小组同学将一定浓度的稀盐酸、稀硫酸分别加入装有等质量碳酸钙粉末的容器中,测得两者产生的二氧化碳体积(V)与反应时间(t)的关系如图3所示。
 (6)、由图3可知反应Ⅱ中0~100s内产生的CO2体积比100~200s内产生的少mL。(7)、观察图3中数据可知反应Ⅰ、Ⅱ在0~100s内生成CO2的速率均先慢后快,在200s以后生成CO2的速率越来越慢。请解释其可能的原因:。13. 有六种途径可以制得氧气,如图所示:
(6)、由图3可知反应Ⅱ中0~100s内产生的CO2体积比100~200s内产生的少mL。(7)、观察图3中数据可知反应Ⅰ、Ⅱ在0~100s内生成CO2的速率均先慢后快,在200s以后生成CO2的速率越来越慢。请解释其可能的原因:。13. 有六种途径可以制得氧气,如图所示: (1)、写出E、F两种途径的文字表达式E:;F:;基本反应类型是。(2)、(填序号)途径发生的是物理变化。(3)、A、F两种途径中二氧化锰的作用是 , 反应前后其和不变。(4)、根据“绿色化学”理念,(填序号)途径是实验室制氧气的最佳方法。14. 为探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330 ℃或380 ℃(其他实验条件如表),并设计了如下实验。
(1)、写出E、F两种途径的文字表达式E:;F:;基本反应类型是。(2)、(填序号)途径发生的是物理变化。(3)、A、F两种途径中二氧化锰的作用是 , 反应前后其和不变。(4)、根据“绿色化学”理念,(填序号)途径是实验室制氧气的最佳方法。14. 为探究影响氯酸钾分解速率的因素,小明把实验温度恒定在330 ℃或380 ℃(其他实验条件如表),并设计了如下实验。实验编号
氯酸钾的质量
催化剂及其质量∕g
温度∕℃
反应的时间/s
氧气体积/mL
①
2.0
无
330
100
V1
②
2.0
氧化铁0.5
330
100
V2
③
2.0
二氧化锰0.5
330
100
V3
④
2.0
二氧化锰0.5
380
100
V4
请回答:
(1)、若想证明氧化铁是氯酸钾分解制取氧气的催化剂,除测定结果V1<V2外,还需要证明氧化铁在化学反应前后的不变。(2)、探究氧化铁对氯酸钾分解速率的影响,要选用实验进行对比。(填写实验编号)(3)、若V3<V4 , 则得到的实验结论是;实验③反应的化学方程式是。(4)、如图所示,在KClO3和Fe2O3质量比为5:4之前,氧化铁质量越多,反应速率越快,可能的原因是。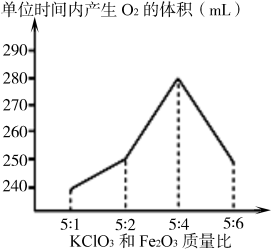 15. 某小组设计如下图所示实验装置,既可用于制取气体,又可用于探究物质性质。(1)、当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是(填字母序号)。
15. 某小组设计如下图所示实验装置,既可用于制取气体,又可用于探究物质性质。(1)、当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是(填字母序号)。a、大理石与稀盐酸反应制取二氧化碳
b、锌粒和稀硫酸反应制取氢气
(2)、当打开K2、关闭K1时,可以利用I、Ⅲ装置制得二氧化碳并验证其性质。实验室制取二氧化碳往往会混有杂质,原因是(不考虑操作和装置因素);澄清石灰水检验二氧化碳的化学方程式 , 若要证明二氧化碳能与水反应(化学方程式为),应向烧杯的水中加入试剂,现象是。 (3)、某同学用下图甲所示的装置制取二氧化碳并测定其体积,装置中植物油的作用是 , 另一位同学对装置进行认真分析,认为即使操作均正确,测量结果也会偏大,于是设计如乙图所示装置。你认为造成甲装置实验结果偏大的原因 , 乙装置中橡皮管的作用是。
(3)、某同学用下图甲所示的装置制取二氧化碳并测定其体积,装置中植物油的作用是 , 另一位同学对装置进行认真分析,认为即使操作均正确,测量结果也会偏大,于是设计如乙图所示装置。你认为造成甲装置实验结果偏大的原因 , 乙装置中橡皮管的作用是。 (4)、若用1.0g石灰石与足量稀盐酸完全反应,利用装置乙测得量筒内水的体积为176.0mL。已知此时二氧化碳气体的密度约为2.0g/L。反应生成的二氧化碳的质量为g;假设石灰石中的杂质不与稀盐酸反应,试计算该石灰石中碳酸钙的质量分数。
(4)、若用1.0g石灰石与足量稀盐酸完全反应,利用装置乙测得量筒内水的体积为176.0mL。已知此时二氧化碳气体的密度约为2.0g/L。反应生成的二氧化碳的质量为g;假设石灰石中的杂质不与稀盐酸反应,试计算该石灰石中碳酸钙的质量分数。三、实验探究题
-
16. 某兴趣小组同学对实验室制取气体和性质应用的若干问题进行如下探究。(1)、【问题一】实验室制取氧气的原料的选择。
在KClO3、H2O、KMnO4、KCl这些物质中寻找制取氧气的原料,肯定不能作为分解反应原料的物质是 , 理由是。(2)、【问题二】实验室制取二氧化碳的反应原理的选择。实验室利用大理石和稀盐酸制取二氧化碳的化学方程式为 , 实验室不采用木炭燃烧制取二氧化碳气体的原因有。(写一条,合理即可)
(3)、【问题三】实验室制取气体的装置的选择。
写出装置A中仪器①的名称。
(4)、若实验室用A(无棉花)制氧气,反应的化学方程式为。(5)、已知NH3是一种无色有刺激性气味的气体,密度比空气小、极易溶于水。实验室可采用浓氨水和氧化钙固体常温下反应制取氨气,应选用的制取装置是(从A-F中选择),若用G装置来收集氨气,气体应从端(填b或c)进入集气瓶。17. 利用如下装置完成气体的制取探究。 (1)、仪器a的名称为。(2)、实验室用高锰酸钾制取氧气,应选择的气体发生装置为 , 收集装置为 , 其反应方程式为。(3)、实验室用大理石和稀盐酸制取二氧化碳,若用C装置收集二氧化碳,气体从(填“m”或“n”)口通入,其反应方程式为。(4)、D装置相对于A装置在制取气体时的优点是。(5)、实验室可用下图装置比较MnO2、CuO对过氧化氢分解的催化效果,实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据。下列说法正确的是____。
(1)、仪器a的名称为。(2)、实验室用高锰酸钾制取氧气,应选择的气体发生装置为 , 收集装置为 , 其反应方程式为。(3)、实验室用大理石和稀盐酸制取二氧化碳,若用C装置收集二氧化碳,气体从(填“m”或“n”)口通入,其反应方程式为。(4)、D装置相对于A装置在制取气体时的优点是。(5)、实验室可用下图装置比较MnO2、CuO对过氧化氢分解的催化效果,实验时,分别将过氧化氢溶液一次性注入盛有催化剂的小试管中,测量并记录数据。下列说法正确的是____。 A、实验数据只需记录产生的氧气体积 B、实验中所用MnO2、CuO的质量相 C、实验过程中发现U型管内右侧液面上升,说明过氧化氢分解吸收热量18. 某化学兴趣小组设计了一组“吹气球”实验,三套装置如图所示:
A、实验数据只需记录产生的氧气体积 B、实验中所用MnO2、CuO的质量相 C、实验过程中发现U型管内右侧液面上升,说明过氧化氢分解吸收热量18. 某化学兴趣小组设计了一组“吹气球”实验,三套装置如图所示: (1)、甲装置:向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置的气密性。(2)、乙装置:若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是。(3)、丙装置:若锥形瓶中盛满CO2 , 欲使气球胀大,则分液漏斗中的液体可以是 , 反应的化学方程式为。19. 实验室现有氯酸钾、大理石、二氧化锰、盐酸、硝酸银溶液、澄清石灰水等药品以及下列装置。请回答下列问题:
(1)、甲装置:向a中加水会看到气球胀大,一段时间内气球大小没有变化,说明该装置的气密性。(2)、乙装置:若生成O2使气球胀大,则锥形瓶中所装的固体物质可以是。(3)、丙装置:若锥形瓶中盛满CO2 , 欲使气球胀大,则分液漏斗中的液体可以是 , 反应的化学方程式为。19. 实验室现有氯酸钾、大理石、二氧化锰、盐酸、硝酸银溶液、澄清石灰水等药品以及下列装置。请回答下列问题: (1)、I.制取氧气时:
(1)、I.制取氧气时:
写出利用上述药品制取氧气的化学方程式。(2)、收集较纯净的氧气,需选择收集装置(填字母),当时,再把导管口伸入。(3)、Ⅱ.制取二氧化碳时:为检验二氧化碳,将B与E连接,观察到E中导管口有气泡冒出,其原因是装置B中发生反应,使其中的气体增多,压强 , , 在压强差作用下,二氧化碳从B中逸出进入E中。试剂均未失效,但却未观察到E中澄清石灰水变白色浑浊。经反思,同学们认为可能与(填药品名称)有关,连接B与F,观察到F(Ⅰ)和F(Ⅱ)中都出现白色沉淀。请结合图像分析,t1~t2期间,F(Ⅱ)的溶液中减少的阳离子是(填离子符号)。

四、计算题
-
20. 某小组利用如图所示装置对KClO3制氧气进行了探究:
(资料卡片):
①KClO3的熔点约为356℃,MnO2在加热条件下不分解。
②KClO3分解时,传感器得到氧气浓度随温度的变化示意图及使用不同催化剂时的固体残留率示意图如下:
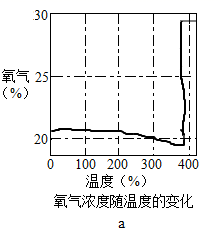
 (1)、将2.45gKClO3和一定质量的MnO2混合物后,加热至完全反应,可得氧气的质量为多少?(写出计算过程)(2)、由图a可知KClO3分解温度(填“高于”、“等于”或“低于”)其熔点。(3)、图a中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是。(4)、分析图b,对KClO3分解催化效果更好的催化剂是。
(1)、将2.45gKClO3和一定质量的MnO2混合物后,加热至完全反应,可得氧气的质量为多少?(写出计算过程)(2)、由图a可知KClO3分解温度(填“高于”、“等于”或“低于”)其熔点。(3)、图a中,在KClO3分解前,传感器测得氧气浓度降低的原因可能是。(4)、分析图b,对KClO3分解催化效果更好的催化剂是。