广东省广州市番禺区华南碧桂园学校2025-2026学年九年级上学期化学11月期中考试试卷
试卷更新日期:2025-11-11 类型:期中考试
一、单选题(每小题3分,共14题,共42分)
-
1. 下列过程中,发生了化学变化的是( )A、固体CO2变成CO2气体 B、从含SiO2的沙子中提炼高纯Si C、海水晒盐 D、从潮湿空气中分离出水2. 空气是人类生产活动的重要资源。下列生活生产中用到的气体不是来自空气的是( )A、炼钢过程用到的氧气 B、磁悬浮列车用到的氮气 C、用于生产氮肥的氨气 D、制作电光源的稀有气体3. 下述说法中正确的是( )A、空气中的氮气、氧气经混合,他们的化学性质都已改变 B、经过液化、蒸发从空气中得到氮气和氧气的过程,属于化学变化 C、空气里氮气、氧气等分子均匀地混合在一起 D、空气中的二氧化碳会造成酸雨4. 钋广泛用于抗静电刷。钋元素的信息如图所示,下列说法错误的是( )
 A、属于金属元素 B、质子数为84 C、核外电子数为84 D、相对原子质量为209g5. 下列说法中正确的是( )
A、属于金属元素 B、质子数为84 C、核外电子数为84 D、相对原子质量为209g5. 下列说法中正确的是( )
A、铁丝在氧气中能燃烧,在空气中也能剧烈燃烧 B、在自来水厂净水的过程中,发生的变化都是物理变化 C、碳在氧气中燃烧后生成无色无味的气体 D、红磷在空气中燃烧时,产生大量的白雾6. 下列物质中,含有氧分子的是( )A、KMnO4 B、O2 C、O3 D、H2O27. 铷(Rb)原子钟被称作北斗卫星的“心脏”、下图为铷原子的结构示意图,下列说法不正确的是( ) A、铷原子核内的质子数为37 B、铷原子在化学变化中容易失去1个电子 C、铷原子的核外电子分5层排布 D、氯化铷的化学式为RbCl28. 下列有关分子、原子和离子的说法正确的是( )A、加碘食盐的主要成分是氯化钠,氯化钠是由氯化钠离子构成的 B、分子、原子、离子都可以直接构成物质 C、在化学反应中,分子不能再分 D、物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变9. 化学用语是学好化学的工具,下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、
A、铷原子核内的质子数为37 B、铷原子在化学变化中容易失去1个电子 C、铷原子的核外电子分5层排布 D、氯化铷的化学式为RbCl28. 下列有关分子、原子和离子的说法正确的是( )A、加碘食盐的主要成分是氯化钠,氯化钠是由氯化钠离子构成的 B、分子、原子、离子都可以直接构成物质 C、在化学反应中,分子不能再分 D、物体有热胀冷缩现象,主要是因为物体中的粒子大小随温度的改变而改变9. 化学用语是学好化学的工具,下列有关化学用语的说法正确的是( )A、H2O和H2O2中O的化合价相同 B、KMnO4和K2MnO4中有相同的原子团 C、Fe2+和Fe3+都属于铁元素,核外电子数不同 D、 和
和 化学性质相同
10. 测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)
化学性质相同
10. 测定空气里氧气含量的实验装置和步骤如下:(已完成装置气密性检查)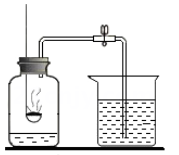
①在集气瓶内加入少量水,并将水面上方空间分为5等份;
②用弹簧夹夹紧胶皮管;
③点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察现象;
④红磷熄灭后,立即打开弹簧夹,观察现象。
其中有错误的实验步骤是( )
A、① B、② C、③ D、④11. 我国药学家屠呦呦因创制新型抗疟药——青蒿素(C15H22O5)和双氢青蒿素成为2015年度诺贝尔生理医学奖得主之一。下列说法正确的是( )A、一个青蒿素分子由32个原子构成 B、每个青蒿素分子中含5个H2O分子 C、青蒿素中碳元素的质量分数的计算式为 D、青蒿素在空气中完全燃烧只生成H2O12. 如图为某反应的微观示意图,“ ”、“
”、“ ”各表示一种原子,下列说法不正确的是
”各表示一种原子,下列说法不正确的是 A、反应物是两种单质 B、反应物有剩余 C、该反应为化合反应 D、该反应生成了多种产物13. 逻辑推理是学习化学常用的思维方法,下列分析推理说法正确的是( )A、原子在化学变化中不能再分,则原子是化学变化中的最小粒子 B、氧化物中都含有氧元素,所以含有氧元素的化合物都是氧化物 C、离子是带电的原子或原子团,所以带电的微粒一定是离子 D、催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂14. 通过下列实验操作和现象能得出相应结论的是( )
A、反应物是两种单质 B、反应物有剩余 C、该反应为化合反应 D、该反应生成了多种产物13. 逻辑推理是学习化学常用的思维方法,下列分析推理说法正确的是( )A、原子在化学变化中不能再分,则原子是化学变化中的最小粒子 B、氧化物中都含有氧元素,所以含有氧元素的化合物都是氧化物 C、离子是带电的原子或原子团,所以带电的微粒一定是离子 D、催化剂在反应前后质量不变,因此反应前后质量不变的物质一定是催化剂14. 通过下列实验操作和现象能得出相应结论的是( )实验操作
现象
结论
A
在火焰上方罩一冷而干燥的小烧杯
烧杯内壁有水雾
该气体一定是H2
B
把硫在空气中点燃,再伸进充满氧气的集气瓶里
硫在空气中燃烧发出淡蓝色火焰,在氧气中燃烧发出蓝紫色火焰
硫在空气中燃烧生成SO2 , 在氧气中燃烧生成SO3
C
在电解器的玻璃管中加满水,接通直流电源
两极玻璃管中有气体生成,体积比是1:2
水是化合物,可分解
D
将带火星的木条置于一瓶盛有氧气的集气瓶口上方
木条不复燃
O2能支持燃烧
A、A B、B C、C D、D二、非选择题(共48分)
-
15. Ⅰ.化学用语是学习化学的重要工具,请用正确的化学符号表示:(1)、3个钠离子;(2)、碳酸根离子;(3)、硫酸铁;(4)、某化合物只由N、O两种元素组成,且在该化合物中N的化合价为+5,该化合物的化学式是;(5)、Ⅱ.制笔行业中经常用到铂、钌(Ru)等金属。现有6种含钌元素的物质:Ru、Ru2O3、RuO2、RuCl3、K2RuO4、Ru2(SO4)3。回答下列问题:
RuO2读作。
(6)、上述6种物质中钌元素的化合价一共有种。(7)、从物质分类的角度看,K2RuO4属于____。(填选项)A、化合物 B、氧化物 C、混合物16. 测定空气中氧气含量的实验装量如下图。 (1)、Ⅰ.图1用红磷测定空气中氧气的含量,回答下面问题:
(1)、Ⅰ.图1用红磷测定空气中氧气的含量,回答下面问题:该实验的主要现象是
(2)、实验中红磷须过量,其目的是(3)、Ⅱ.小张同学利用镁条代替红磷,根据图2所示的实验装置测定空气中氧气的含量,在确保规范操作的前提下,所测得的空气中氧气的体积分数大于1/5。同时发现燃烧产物中还有一些黄色固体。查阅资料后得到以下信息:①氧化镁为白色固体;②镁能与氮气反应生成黄色的氮化镁(化学式为Mg3N2)固体;根据你所学过的知识,写出镁与氮气燃烧生成Mg3N2的符号表达式:
(4)、空气中N2与O2的体积比大约是 , 而镁条在空气中燃烧生成的MgO却远多于Mg3N2 , 可见镁更容易和氧气反应。请你作出合理的解释:(5)、Ⅲ.根据下图所示实验,并阅读小资料,回答下列问题。
图1中的反应现象为 ,
该化学的符号表达式为。
(6)、图2中的集气瓶中加入的液体可能是 ,写出该液体与硫燃烧产物反应的符号表达式。
17. Ⅰ.根据如图所示原子结构示意图及原子在周期表中的相关信息,回答下列问题: (1)、氧原子的相对原子质量是。(2)、过氧化氢(H2O2)能杀菌消毒,H2O2中氧元素的化合价是。(3)、氨气是一种重要的化工原料,如图2是氮气和氢气反应生成氨气的微观示意图。
(1)、氧原子的相对原子质量是。(2)、过氧化氢(H2O2)能杀菌消毒,H2O2中氧元素的化合价是。(3)、氨气是一种重要的化工原料,如图2是氮气和氢气反应生成氨气的微观示意图。①请写出此反应的符号表达式:。
②氨气分子中氮原子与氢原子的个数比为。
(4)、Ⅱ.根据下图,回答问题:(已知镁元素的质子数为12,氯元素的质子数为17)
如上图A、B、C、D四种粒子共表示种元素。
(5)、下列关于E粒子的说法中,你认为最恰当的是____(填选项)。A、阳离子 B、阴离子 C、原子 D、以上三种都有可能(6)、B元素的单质可在D元素的单质中燃烧,且发生化合反应,请写出该反应的符号表达式。18. 图1是实验室净化天然水的流程: (1)、原理分析:
(1)、原理分析:①请从“沉降”、“蒸馏”“蒸发”、“吸附”、“过滤”中选择合适的关键词填写在上述图1方框内A、B的空白处。A、B。
②自来水厂可利用明矾【KAl(SO4)2﹒12H2O】溶于水后生成的胶状物对杂质的吸附,使杂质沉降来达到净水的目的。请计算KAl(SO4)2中铝元素的化合价为;KAl(SO4)2﹒12H2O中含有的带电的原子团是(填离子符号)。
(2)、操作过程:在过滤后,同学们发现得到的滤液仍然浑浊,可能的原因是(写出一个即可)。(3)、电解水的实验装置示意图如图,试管(填“a”或“b”)中的气体能使燃着的木条燃烧更旺。电解水的符号表达式为 , 结合下面的电解水示意图,从微观角度补充填写完成图A和图B。宏观变化
微观解释

 19. 实验室制取气体是化学学习者的必备技能。实验室里现有高锰酸钾、二氧化锰,以及下列仪器:
19. 实验室制取气体是化学学习者的必备技能。实验室里现有高锰酸钾、二氧化锰,以及下列仪器: (1)、在上述仪器和药品的基础上,若补充一种仪器(填名称),再选择上述仪器中的(填编号)和药品制取氧气,反应的符号表达式为(2)、若用H2O2分解可制取O2 , 实验室通过测定收集一定体积O2所用的时间,来研究不同条件对H2O2分解速率的影响。
(1)、在上述仪器和药品的基础上,若补充一种仪器(填名称),再选择上述仪器中的(填编号)和药品制取氧气,反应的符号表达式为(2)、若用H2O2分解可制取O2 , 实验室通过测定收集一定体积O2所用的时间,来研究不同条件对H2O2分解速率的影响。实验
温度∕℃
H2O2溶液浓度
H2O2溶液体积∕mL
1g催化剂
时间∕s
1
20
5%
40
二氧化锰
37
2
20
10%
40
二氧化锰
14
3
20
a
40
二氧化锰
b
①上表中实验1、2探究对分解速率的影响,实验2、3探究不同催化剂对分解速率的影响,则浓度a为。
②H2O2分解可制取O2 , 该小组在反应开始后立即开始收集(集气瓶上方有少量空气),从而测定收集一定体积O2所用的时间。你认为该做法(填:“是”与“否”)合理。说出你的观点并阐述理由:。
(3)、分离液态空气是工业上制取氧气的重要途径,下图是工业上制氧气的流程图:
①氮气的沸点为-196℃,氧气的沸点为-183℃在蒸发的过程中(填“氮气”或“氧气”)先被蒸发出来。
②从微粒的角度分析,物质状态改变的原因是。
20. 材料是人类赖以生存和发展的物质基础。C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80—215℃时,又会分解放出H2。 (1)、①C60属于(字母序号)。
(1)、①C60属于(字母序号)。
A.混合物 B.氧化物 C.单质 D.化合物
②C60可用作吸氢材料是利用了其(填“物理”或“化学”)性质。(2)、二氧化碳是一种宝贵的资源。固定和利用二氧化碳的一个成功范例是:在高温高压下二氧化碳和氨气(NH3)可以合成尿素【CO(NH2)2】,同时生成水。该反应的符号表达式为(3)、CO(NH2)2的相对分子质量:;(4)、CO(NH2)2中氧元素和氮元素的质量比:;(5)、CO(NH2)2中氮元素的质量分数(精确到0.1%):。