科粤版初中化学九年级上册单元测试-第四单元 化学式与化学方程式(提升卷)
试卷更新日期:2025-10-19 类型:单元试卷
一、选择题(本题共10小题;每小题2分,共20分)
-
1. 如图表示 CH4和 CO2在 Ni 纳米催化剂作用下的反应。下列说法错误的是
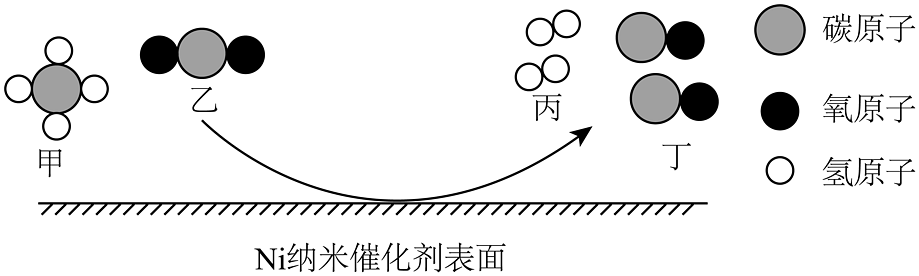 A、此反应可用于 CO2的储存与转换 B、CH4 + CO2= 2CO + 2H2 C、反应前后原子的种类不变 D、反应前后分子的种类改变2. 富马酸福莫特罗(化学式为C42H56N4O14)主要用于治疗支气管疾病,下列有关富马酸福莫特罗的说法正确的是A、一个分子含有1个N4分子 B、碳、氧元素的质量比为3:1 C、属于氧化物 D、氢元素和氮元素的质量分数相同3. 青铜中含有少量的锡,锡元素的有关信息如图所示。下列说法正确的是
A、此反应可用于 CO2的储存与转换 B、CH4 + CO2= 2CO + 2H2 C、反应前后原子的种类不变 D、反应前后分子的种类改变2. 富马酸福莫特罗(化学式为C42H56N4O14)主要用于治疗支气管疾病,下列有关富马酸福莫特罗的说法正确的是A、一个分子含有1个N4分子 B、碳、氧元素的质量比为3:1 C、属于氧化物 D、氢元素和氮元素的质量分数相同3. 青铜中含有少量的锡,锡元素的有关信息如图所示。下列说法正确的是 A、锡的核外电子数为50 B、锡的相对原子质量为118.7g C、二氧化锡的化学式为O2Sn D、Sn属于非金属元素4. 2024年央视春晚《山河诗长安》以诗歌、汉服、舞狮舞龙、沉香等形式的国潮表演,展示了我国优秀的传统文化。沉香中含有沉香螺醇(C15H26O),下列有关沉香螺醇的说法正确的是A、由碳、氢、氧三种元素组成 B、由碳原子、氢原子和氧原子构成 C、其中碳、氢元素的质量比为15:26 D、其中氢元素的质量分数最大5. 下列化学方程式的书写正确的是( )A、 B、 C、 D、6. 距今约8万-6万年的资阳濛溪河遗址入选2024年中国十大考古新发现,遗址中出土了多粒炭化的花椒种子,将人类对“麻”的追求提早几万年。花椒皮麻味来(C6H8NO)中C、H、O、N四种元素的质量比为( )A、16:25:1:1 B、36:4:8:7 C、12:1:16:14 D、192:25:14:167. 下列各图中
A、锡的核外电子数为50 B、锡的相对原子质量为118.7g C、二氧化锡的化学式为O2Sn D、Sn属于非金属元素4. 2024年央视春晚《山河诗长安》以诗歌、汉服、舞狮舞龙、沉香等形式的国潮表演,展示了我国优秀的传统文化。沉香中含有沉香螺醇(C15H26O),下列有关沉香螺醇的说法正确的是A、由碳、氢、氧三种元素组成 B、由碳原子、氢原子和氧原子构成 C、其中碳、氢元素的质量比为15:26 D、其中氢元素的质量分数最大5. 下列化学方程式的书写正确的是( )A、 B、 C、 D、6. 距今约8万-6万年的资阳濛溪河遗址入选2024年中国十大考古新发现,遗址中出土了多粒炭化的花椒种子,将人类对“麻”的追求提早几万年。花椒皮麻味来(C6H8NO)中C、H、O、N四种元素的质量比为( )A、16:25:1:1 B、36:4:8:7 C、12:1:16:14 D、192:25:14:167. 下列各图中 和
和 分别表示不同元素的原子,其中表示混合物的是 A、
分别表示不同元素的原子,其中表示混合物的是 A、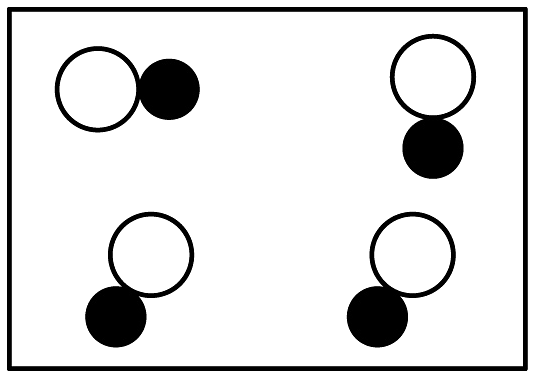 B、
B、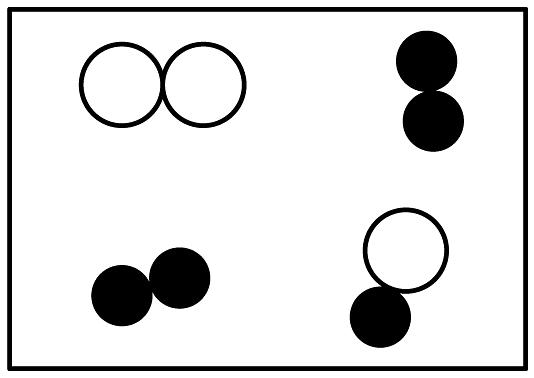 C、
C、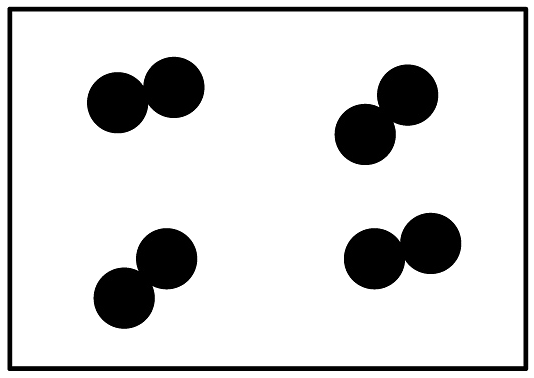 D、
D、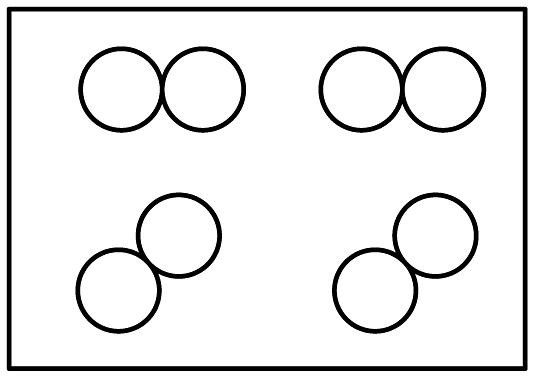 8. 中国春节已正式列入联合国教科文组织非物质文化遗产名录,2025年迎来了首个“非遗版”春节。阖家团聚,年年有余(鱼),烹饪时加入黄酒和食醋生成的乙酸乙酯 使鱼肉别具香味,下列关于乙酸乙酯的说法正确的是( )A、乙酸乙酯的相对分子质量为88g B、1个乙酸乙酯分子由 14个原子构成 C、乙酸乙酯分子由碳、氢、氧元素组成 D、乙酸乙酯中碳、氢、氧三种元素的质量比为2:4:19. 华东理工大学在钙钛矿太阳能电池研究领域取得重要突破,创新性地采用单层石墨烯与聚甲基丙烯酸甲酯的复合结构,相关成果处于国际领先水平。聚甲基丙烯酸甲酯的单体为甲基丙烯酸甲酯(化学式 , 结构如图所示),下列关于甲基丙烯酸甲酯()的说法正确的是
8. 中国春节已正式列入联合国教科文组织非物质文化遗产名录,2025年迎来了首个“非遗版”春节。阖家团聚,年年有余(鱼),烹饪时加入黄酒和食醋生成的乙酸乙酯 使鱼肉别具香味,下列关于乙酸乙酯的说法正确的是( )A、乙酸乙酯的相对分子质量为88g B、1个乙酸乙酯分子由 14个原子构成 C、乙酸乙酯分子由碳、氢、氧元素组成 D、乙酸乙酯中碳、氢、氧三种元素的质量比为2:4:19. 华东理工大学在钙钛矿太阳能电池研究领域取得重要突破,创新性地采用单层石墨烯与聚甲基丙烯酸甲酯的复合结构,相关成果处于国际领先水平。聚甲基丙烯酸甲酯的单体为甲基丙烯酸甲酯(化学式 , 结构如图所示),下列关于甲基丙烯酸甲酯()的说法正确的是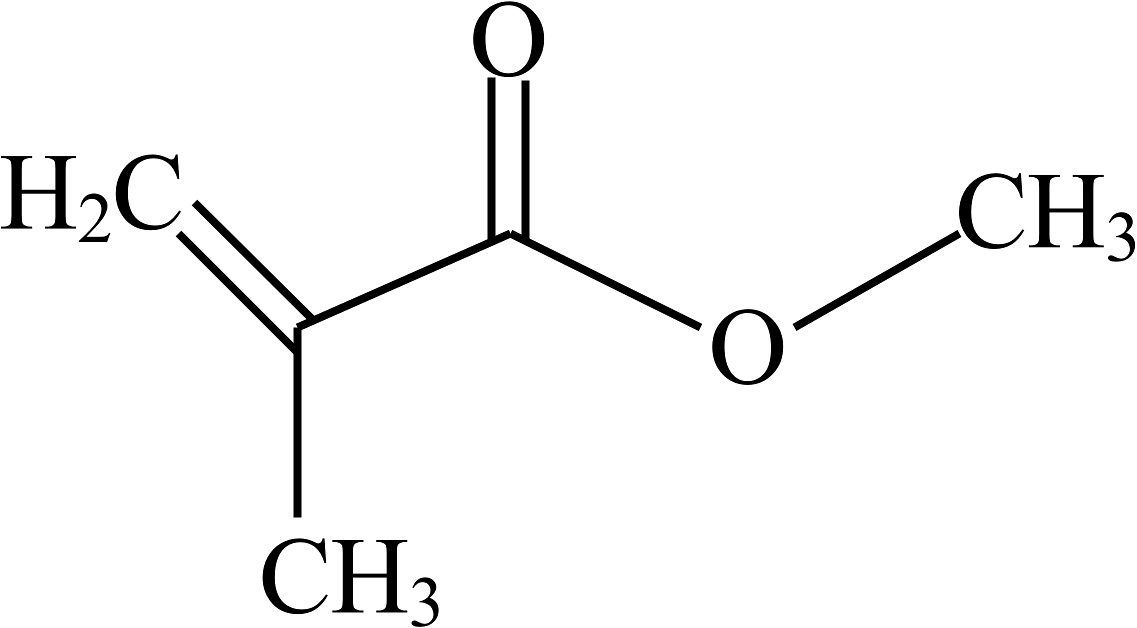 A、由15个原子构成 B、属于氧化物 C、氢元素的质量分数最大 D、碳、氧元素质量比为10. 甲烷与在催化作用下可得到合成气(和)。反应时催化剂表面同时存在积碳和消碳反应,如图。下列说法正确的是
A、由15个原子构成 B、属于氧化物 C、氢元素的质量分数最大 D、碳、氧元素质量比为10. 甲烷与在催化作用下可得到合成气(和)。反应时催化剂表面同时存在积碳和消碳反应,如图。下列说法正确的是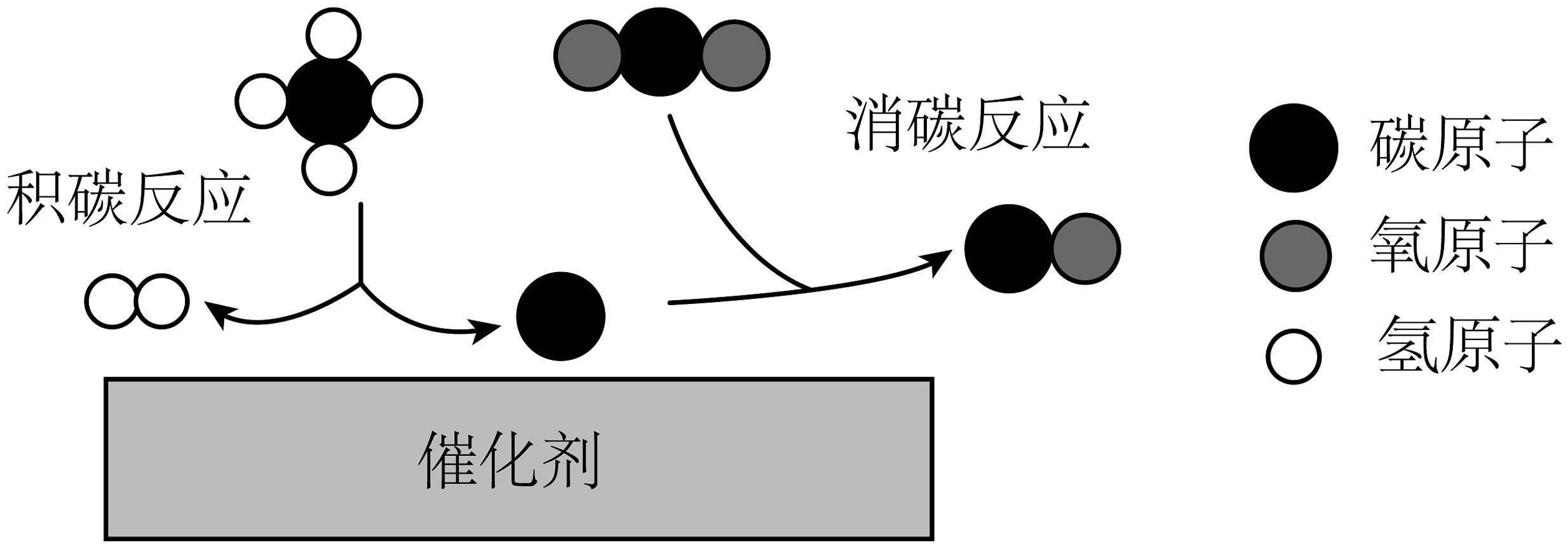 A、图中涉及的氧化物有3种 B、积碳反应为: C、为减少积碳,可加入稍过量的 D、反应结束若催化剂表面仍有积碳,则合成气中比多
A、图中涉及的氧化物有3种 B、积碳反应为: C、为减少积碳,可加入稍过量的 D、反应结束若催化剂表面仍有积碳,则合成气中比多二、简答题(本题共1小题;共10分)
-
11. 实验化学小组用如图所示装置进行实验探究。
 (1)、滴入过氧化氢溶液后,请书写试管内发生反应的化学方程式。(2)、在燃烧管下放置装有80℃热水的大烧杯,观察到白磷燃烧而红磷不燃烧,据此现象得出燃烧需要的条件是什么?(已知,白磷的着火点为40℃,红磷的着火点为240℃)
(1)、滴入过氧化氢溶液后,请书写试管内发生反应的化学方程式。(2)、在燃烧管下放置装有80℃热水的大烧杯,观察到白磷燃烧而红磷不燃烧,据此现象得出燃烧需要的条件是什么?(已知,白磷的着火点为40℃,红磷的着火点为240℃)三、填空题(本题共4小题;共32分)
-
12. 化学用语是学习化学的重要工具。请用化学用语表示。(1)、氖元素________;(2)、汞原子________;(3)、两个氮分子________;(4)、碳酸根离子________;(5)、五氧化二磷________;(6)、标出水中氧元素的化合价________。13. 炉甘石始载于《外丹本草》,主要成分为碳酸锌(ZnCO3)和碱式碳酸锌,炮制后主要成分氧化锌(ZnO)可作为外用药使用。(1)、碳酸锌中有种元素;其中锌、氧元素的原子个数比为 , 质量比为。(2)、氧化锌中锌元素的质量分数为________(结果保留0.1%)(3)、氧化锌、碳酸锌、碱式碳酸锌都有一定的抑菌活性,说明起抑菌作用的有效成分可能是___________(填字母)。A、锌分子 B、锌元素 C、锌单质 D、锌原子14. 春晚《满庭芳·国色》节目点燃了国人复古寻色的热潮,其中桃红、凝脂、缃叶、群青、沉香代表红、白、黄、青、黑传统五色。(1)、群青:是一种品贵的高级颜料,古代是用贵重的青金石中研磨制成的。青金石中含、O等元素,从原子结构的角度说明,这些元素最根本的区别是不同。(2)、桃红:用银朱调合,可以得到灿若桃花的颜色。银朱是用硫与汞加热制成的硫化汞,反应前后不变的微粒是(填化学符号)。(3)、凝脂:降低原料中含铁氧化物含量,实现从青瓷到凝脂似玉的白瓷。如图为铁元素的价类二维图,a点表示物质的类别是 , c点的化学式是。
 (4)、缃叶:取色自雌黄(),颜色类似硫磺,在空气中燃烧能产生剧毒的和一种刺激性气味的气体,该反应的化学方程式为。(5)、沉香:代表黑色,以下固体可能为沉香主要成分的是___________(填字母)。A、氧化镁 B、氧化铜 C、五氧化二磷 D、氧化铁(6)、孔雀石主要成分为 , 受热分解生成三种氧化物,其反应的化学方程式为。15. “宏观辨识与微观探析”’是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。金属钠在氯气中燃烧生成氯化钠,如图为氯化钠形成的示意图。
(4)、缃叶:取色自雌黄(),颜色类似硫磺,在空气中燃烧能产生剧毒的和一种刺激性气味的气体,该反应的化学方程式为。(5)、沉香:代表黑色,以下固体可能为沉香主要成分的是___________(填字母)。A、氧化镁 B、氧化铜 C、五氧化二磷 D、氧化铁(6)、孔雀石主要成分为 , 受热分解生成三种氧化物,其反应的化学方程式为。15. “宏观辨识与微观探析”’是化学学科核心素养之一,化学学习要让学生既能够“见微知著”,也能够“见著知微”。金属钠在氯气中燃烧生成氯化钠,如图为氯化钠形成的示意图。
根据所给信息,请回答:
(1)钠原子的核外电子层数是 , 在化学反应中易(填“得到”或“失去”)电子。
(2)元素的化学性质主要是由原子的决定的。
(3)化学反应前后,氯元素的化合价为。
(4)构成氯化钠的离子是(填微粒符号)。
四、实验探究题(本题共4小题;共31分)
-
16. 近年来,全球低糖食品的总体消费量持续增长。
I.糖类作用
(1)、人每天要摄入一定量的糖类以维持血液中一定浓度的葡萄糖,否则易造成 , 出现乏力、休克等症状;葡萄糖在体内发生缓慢氧化的反应方程式为。(2)、II.代糖生产代糖是一类替代蔗糖等天然糖的非营养性甜味剂,木糖醇是一种常见的代糖。木聚糖是生产木糖醇的原料,具有可燃性。科研人员研究用玉米芯膨化后辅助酶解法制备木聚糖,两组实验情况如下表。
序号
①组实验
②组实验
实验条件
膨化机内无水情况下,在不同压力下实验
膨化机内添加不同比例的水,在压力1.4MPa下实验
实验数据


从②组实验数据得出的结论是。
(3)、比较两组实验数据,推测进行①组实验时,压力提高至1.4MPa时木聚糖制得率下降的可能原因为:膨化机内物料的温度过高,打开膨化机接触空气,。(4)、III.代糖研究已知木糖醇中含有碳、氢、氧三种元素。兴趣小组取1.52g木糖醇按照如图装置测定木糖醇分子中原子个数比,测得B装置增重了1.08g,C装置增重了2.2g。(实验前已排尽装置内空气,使用药品均足量)

实验中观察到现象后停止加热。
(5)、木糖醇分子中碳、氢、氧原子个数比为。(6)、若装置A中缺少氧化铜,将导致测得的木糖醇中氧元素含量(选填“偏大”、“不变”或“偏小”)。(7)、IV.代糖应用某品牌可乐每罐含糖(核算成蔗糖)11.2g,该品牌甜度相当的无糖可乐用阿斯巴甜和安赛蜜为代糖,结合下表数据分析未选木糖醇的可能原因是;体重为50kg的人喝该种同体积罐装无糖可乐,每天不宜超罐(以整数计)。
名称
甜度(等质量比较)
价格(元/kg)
安全用量mg/(kg体重)/天
热量(kca/g)
蔗糖
1
9
未作具体规定
4
木糖醇
1
22
未作具体规定
2.4
阿斯巴甜
200
74
0-40
4
安赛蜜
200
50
0-15
0
17. 以下为某校化学兴趣小组开展的“空气中氧气含量的测定”实验活动:
 (1)、图1中仪器①的名称是。若实验中红磷量不足,可能导致所测值。(选填“偏大”、“偏小”或“不变”)(2)、图2为图1的改进装置,图3是通过压强传感器测得图2容器内压强随时间变化的曲线。
(1)、图1中仪器①的名称是。若实验中红磷量不足,可能导致所测值。(选填“偏大”、“偏小”或“不变”)(2)、图2为图1的改进装置,图3是通过压强传感器测得图2容器内压强随时间变化的曲线。①该反应的化学方程式为;与图1装置相比,该装置的优点是 , 可观察的不同现象是;
②关闭弹簧夹K,闭合电路,图3中-a段压强增大的理由是;a-b段压强减小的原因是。
18. 2023年杭州亚运会主火炬燃料为“零碳甲醇”,利用废气中的热催化加氢合成,实现了二氧化碳的减排和再生利用,其原理如图所示. (1)、Ⅰ.电解制氢
(1)、Ⅰ.电解制氢
光伏发电是将太阳能转化为能,电解水制取氢气的化学方程式为 .(2)、Ⅱ.捕集以石灰石为原料的钙循环捕集废气中的流程如图:

①图中,含量较低的是(填“A”或“B”)处.
②经多次循环后,作为吸附剂吸收效果会降低,固体结构变化如图所示.多次循环后,吸附剂效果降低的原因是 .
 (3)、Ⅲ.使用甲醇
(3)、Ⅲ.使用甲醇甲醇可以直接燃烧,也可以将甲醇转化为氢气再燃烧,甲醇转化为氢气通常有以下两种方案:
方案1:
方案2:
①对比上述两种方案,方案1的优点是(写1条即可).
②有关“零碳甲醇”燃料的理解正确的是(填字母).
A.甲醇燃料分子中不含碳原子
B.通过碳循环使碳排放无限接近零
C.生产燃料使用的原料不含碳元素
19. 呼吸自救器是人在缺氧环境或出现高浓度有毒有害气体环境中使用的一种安全防护装置,如图为某呼吸自救器示意图,其供氧装置由“初期生氧器”和“生氧罐”组成,同学们对其工作原理进行了如图探究: (1)、I.探究“初期生氧器”
(1)、I.探究“初期生氧器”
【查阅资料1】
①该自救器在工作初期,内部独立的“初期生氧器”首先启动,以解决初期供氧不足的问题。“初期生氧器”内有氯酸钾、二氧化锰、铁粉等物质。“初期生氧器”中铁粉通过“引发器”与氧气反应放出大量的热,从而使氯酸钾的分解反应能持续进行。
②Fe3O4能与硫酸反应,其反应方程式为Fe3O4+4H2SO4=Fe2(SO4)3+FeSO4+4H2O;Fe2(SO4)3溶液呈黄色。
“初期生氧器”依靠氯酸钾和二氧化锰反应制氧,其化学反应方程式为。(2)、小组成员为了解铁粉的变化展开如下探究。【实验探究1】
序号
实验步骤
实验现象
实验结论
①
取“初期生氧器”充分反应后的物质于纸上,将磁铁靠近粉末
有黑色物质被磁铁吸引
被吸引物质可能是Fe、Fe3O4或Fe和Fe3O4的混合物
②
取①中被磁铁吸引的物质于试管中,向其中加入足量稀硫酸
固体完全溶解,得到澄清的黄色溶液
被吸引物质中一定含有(填化学式)
(3)、Ⅱ.探究“生氧罐”【查阅资料2】
①该自救器主体是由“生氧罐”供氧,内部装有颗粒状超氧化钾作“制氧剂”,其反应原理为4KO2+2H2O=4KOH+3O2↑;4KO2+2CO2=2K2CO3+3O2。
②超氧化钾与硫酸反应的化学反应方程式为4KO2+2H2SO4=2K2SO4+3O2↑+2H2O。
③2KOH+H2SO4=K2SO4+2H2O;K2CO3+H2SO4=K2SO4+CO2↑+H2O;2NaOH+CO2=Na2CO3+H2O。
④浓硫酸常用于干燥气体。
【实验探究2】
同学们对超氧化钾变化情况展开探究。取出使用后的“生氧罐”内的颗粒状固体,称得样品69.3g。将样品按如图进行实验,实验结束后测得C装置增重2.2g,E装置内固体变黑色且增重19.2g(实验前已排尽装置内空气,使用的药品均足量)。

实验过程中一直需从A装置中通入N2至实验结束后一段时间,目的是。
(4)、E装置中发生反应的化学反应方程式为。(5)、实验结果:样品中反应了的超氧化钾和没有反应的超氧化钾的质量比为。五、计算题
-
20. 某炉具清洁剂的有效成分氢氧化钠,兴趣小组的同学想测定该清洁剂中氢氧化钠的含量,取炉具清洁剂倒入烧杯中,逐次加入质量分数为的稀硫酸,测出溶液的随加入稀硫酸的质量变化关系如图所示,完成下列问题:
 (1)、中硫元素与氧元素的质量比(填最简整数比)。(2)、计算该炉具清洁剂中氢氧化钠的质量分数。
(1)、中硫元素与氧元素的质量比(填最简整数比)。(2)、计算该炉具清洁剂中氢氧化钠的质量分数。
-